Упрощенная схема механизма реакции окисления глюкозы на платиновом катализаторе представлена Gallezot в работе [47]; аналогичный механизм был предложен Токаревым и др. для окисления лактозы [[51]]. Ключевыми стадиями являются дегидрирование полуацетальной формы субстрата на поверхности катализатора с образованием δ-лактона, который далее десорбируется, реагируя с гидроксид-ионом (Рис. 7). Несомненную важность гидроксид-ионов в процессе каталитического окисления подтверждает резкое падение скорости реакции при уменьшении pH среды (см. раздел 2.3).
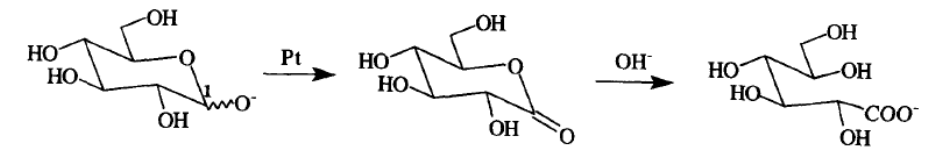
Рис. 7. Схема каталитического окисления глюкозы на платиновом катализаторе.
Многие детали механизма в настоящее время точно не установлены, например
природа частиц, адсорбированных на металлической поверхности (H
или H(-), OH или
OH(-), RCH2OH или RCH2O(-) или RCH2O·), зависящая от многих факторов, таких как pH, присутствие кислорода, концентрация сахара и природа
металлов [47].
3.1 Каталитическая активность золотых катализаторов
В последние несколько лет, начиная с открытия в 1997 году каталитической активности Au в реакции селективного окисления спиртов, интенсивно исследуется каталитическая активность золотых наночастиц в различных окислительных реакциях, в том числе и в окислении сахаров [[52]]. В работе [[53]] было показано, что удельная каталитическая активность катализатора Au/TiO2 в реакциях окисления пентоз (рибозы, ксилозы, арабинозы, ликсозы), гексоз (глюкозы, маннозы, галактозы, N-ацетил-глюкозамина, рамнозы), дисахаридов (мальтозы, лактозы, целлобиозы, меллибиозы) значительно превышает активность Pt/Al2O3 и Pd/Al2O3.
В силу большой практической значимости глюконовой кислоты в последние годы интенсивно исследуется реакция окисления глюкозы на золотых катализаторах. Каталитическая активность золотого катализатора Au/C в реакции селективного окисления глюкозы значительно выше, чем Pd/C, Pt/C, Pd-Bi/C и Pt-Pd-Bi/C [[54]]. Была показана высокая каталитическая активность коллоидного золота [[55], [56]], а также наночастиц золота, нанесенных на различные углеродные носители (activated carbon, black pearls, Vulcan) методом иммобилизации золя [54, [57], [58], [59], [60]], оксидные носители (Al2O3, TiO2, CeO2, ZrO2) методами пропитки [[61], [62]] и осаждения [61, [63], [64], [65]], ионообменные смолы методом ионного обмена [[66]]. Кроме выбора оптимального носителя, большой интерес исследователей вызывает выбор оптимальной дисперсности золотых катализаторов окисления глюкозы. Для коллоидных золотых частиц была найдена квазилинейная зависимость начальной удельной каталитической активности от обратного значения среднего диаметра частиц золя в диапазоне 2-7 нм, которая резко падает практически до нуля при укрупнении частиц золота до ~10 нм [55]. Удельная каталитическая активность катализаторов Au/C в реакции окисления глюкозы кислородом уменьшается при увеличении размера частиц от 2.5 нм до 6.5 нм пропорционально изменению площади удельной поверхности золота, а затем резко уменьшается практически до нуля при значении среднего размера частиц 10 нм [55]. В работе [[67]] рассмотрены золотые катализаторы на различных носителях, приготовленные методами solid grinding и DP, размер золотых частиц на которых варьировался в диапазоне 2-6 нм. Активность полученных катализаторов в реакции окисления глюкозы в значительной степени зависела от выбранного носителя и способа приготовления.
Значительный вклад в изучении процессов окисления лактозы на золотых катализаторах внесла группа под руководством Мурзина [28, 51, [68]]. Они продемонстрировали возможность высокоселективного окисления лактозы на золотых наночастицах, нанесенных на ряд носителей: Al2O3, TiO2, SiO2, Fe3O4, ZrO2 [69].
3.2. Качественный и количественный состав продуктов окисления
Окисление сахаров, содержащих альдегидную группу, как моносахаридов, так и дисахаридов на золотых катализаторах происходит с высоким выходом (до 99.5%) [53].
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.