ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
НОВОСИБИРСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
ПО ФИЗИЧЕСКОЙ ХИМИИ
Методическое пособие
Новосибирск
2007
Методическое пособие является электронной версией издания «Практикум по химической кинетике» из которого исключены работы К2 – К5, вошедшие в пособия «Кондуктометрия» и «Потенциометрия», а также работы К11 и К14.
Разработчиками и авторами приведенных здесь лабораторных работ являются основатель практикума по физической химии в НГУ Елисей Сергеевич Рудаков, а также преподаватели Ю. В. Бутенко, В. Н. Зудин, к.х.н. В. А. Иванченко, д.х.н. Г. А. Коваленко, к.х.н. В. А. Рогов, д.х.н. Е. П. Талзи и к.х.н. В. М. Тормышев. В работе по подготовке сборника к изданию участвовали сотрудники и преподаватели кафедры физической химии Н. В. Ложкина, В. П. Дубовицкая и П. Н. Калинкин.
Предназначено для студентов 3-го курса факультета естественных наук Новосибирского государственного университета.
Составители:
к.х.н. В. А. Рогов
д.х.н. Г. А. Коваленко
д.х.н. Е. П. Талзи
© Новосибирский государственный
университет, 2007
Задача К-6
К-6.1ИЗУЧЕНИЕ КИНЕТИКИ РЕАКЦИИ БИС(САЛИЦИЛАЛЬДЕГИДАДА) МЕДИ (II) С АНИЛИНОМ
ОПТИЧЕСКИМ МЕТОДОМ
Исследуемая реакция – типичный пример синтеза комплексов металлов с шиффовыми основаниями.
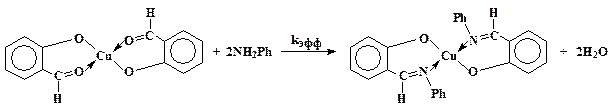
![]() (1)
(1)
Механизм реакции (1) достаточно сложен. Варьируя природу заместителей в
бензольном кольце альдегида, можно зафиксировать промежуточные стадии. Однако в
рассматриваемом случае удается измерить лишь ![]() суммарного
процесса.
суммарного
процесса.
Определение ![]() реакции (1) оптическим методом
реакции (1) оптическим методом
Оптическая плотность реакционного раствора на длине волны ![]() в момент времени t есть
в момент времени t есть
![]() (2)
(2)
где
![]() и С1(t) – коэффициент экстинции
и текущая концентрация исходного комплекса,
и С1(t) – коэффициент экстинции
и текущая концентрация исходного комплекса, ![]() и С2(t)
– соответствующие характеристики продукта, толщина кюветы l = 1 см, предполагается, что поглощение NН2Ph и Н2О на выбранной длине волны
отсутствует.
и С2(t)
– соответствующие характеристики продукта, толщина кюветы l = 1 см, предполагается, что поглощение NН2Ph и Н2О на выбранной длине волны
отсутствует.
При условии [NН2Рh] >> [Сu(Salald)2]
![]()
![]() (3)
(3)
где С0 – начальная концентрация Сu(Salald)2, t – время реакции.
Схема реакции (1) предполагает первый порядок по концентрации анилина, т.е.
![]() . (4)
. (4)
Однако механизм реакции может быть более сложным, поэтому в общем случае
![]() ,
,
где n – порядок реакции по анилину, который необходимо определить, k – константа.
Подставляя С1(t) и С2(t) из (3) в (2), получаем
![]() (5)
(5)
![]() , (6)
, (6)
где
![]() -
оптическая плотность раствора по завершении реакции.
-
оптическая плотность раствора по завершении реакции.
Из тангенса угла наклона зависимости ![]() от t определить kэфф.
Измерить kэфф при трех температурах 30, 40 и 50 0С,
определить Eа.
от t определить kэфф.
Измерить kэфф при трех температурах 30, 40 и 50 0С,
определить Eа.
Из тангенса угла наклона зависимости ln(kэфф) от ln[NН2Рh] определить порядок реакции.
Проведение эксперимента
Измерения кинетики проводят в 1 см кюветах на длине волны вблизи 27000 см-1, которая выбирается
исходя из оптического спектра Сu(Salald)2. Рабочую длину волны ![]() следует выбрать в области спектра, где
поглощение NН2Ph и Н2О отсутствует.
следует выбрать в области спектра, где
поглощение NН2Ph и Н2О отсутствует.
Вариант 1
Приготовить 50 мл 0,01 М раствора Сu(Salald)2 в хлороформе. Затем отобрать пробу этого раствора объемом 3 мл и добавить в нее анилин в таком количестве, чтобы концентрация анилина в пробе составляла 1,5 М. Перемешать, включить секундомер, заполнить оптическую кювету и проводить измерение оптической плотности в течение 30 мин при 20 0С. То же самое проделать при 30, 40 и 50 0С.
Для последующих расчетов должна быть измерена оптическая плотность раствора по завершении реакции. Определить энергию активации.
Вариант 2
Аналогично варианту 1 провести измерение kэфф при температуре 30 0С и пяти концентрациях анилина: 1,0; 1,3; 1,5; 2,0; 2,5 М.
Определить порядок реакции.
К-6.2ИЗУЧЕНИЕ КИНЕТИКИ РЕАКЦИИ САЛИЦИЛОВОГО АЛЬДЕГИДА С АНИЛИНОМ
МЕТОДОМ ЯМР
Изучаемая реакция – пример реакции образования оснований Шиффа
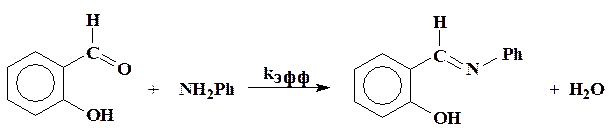
Согласно литературным данным реакции такого типа протекают через образование интермедиата – карбиноламина
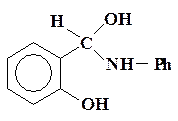
Однако в рассматриваемой системе удается наблюдать только начальный и конечный продукты и измерить эффективную константу скорости реакции kэфф.
Измерения проводят в четыреххлористом углероде.
Перед началом измерений записать спектр ЯМР 0.1 М раствора салицилового альдегида в ССl4. В качестве стандарта для внутренней стабилизации магнитного поля лучше использовать циклогексан. Отнести линии в спектре.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.