Подставляем
полученное значение ![]() в выражение для равновесной
степени превращения:
в выражение для равновесной
степени превращения:
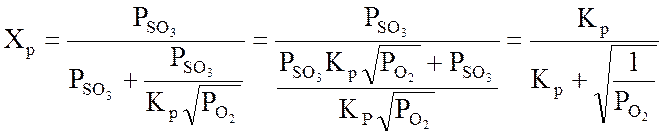 (1.7)
(1.7)
При общем давлении смеси Р, начальном содержание SO2 «а» об. % и начальном содержании O2 «b» об. %, парциальное давление кислорода в равновесной газовой смеси составит:
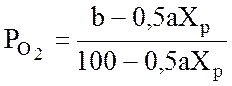 (1.8)
(1.8)
Отсюда равновесная степень превращения:
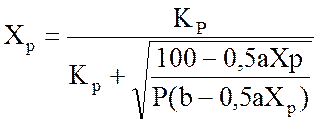 (1.9)
(1.9)
Размерность и численное значение константы равновесия зависит от размерности парциальных давлений компонентов в выражении (1.6).
Зависимость константы равновесия от температуры определяется уравнением:
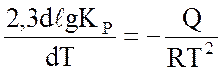 ,
(1.10)
,
(1.10)
где Q – тепловой эффект реакции (1.1) при постоянном давлении, отнесенный к 1 кмолю окисляемого SO2, кДж; R = 8,31 кДж/моль – универсальная газовая постоянная.
После подстановки выражения (1.2) для Q и интегрирования получаем следующую зависимость константы равновесия от температуры:
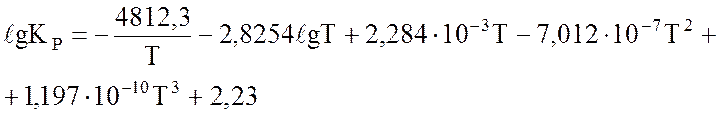 (1.11)
(1.11)
С достаточной точностью для интервала температур 400÷700 оС можно пользоваться упрощенным уравнением:
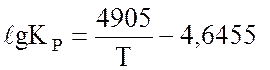 (1.12)
(1.12)
Размерность КР в уравнениях (1.11) и (1.12)
в атм0,5. Если давление в формуле (1.4.) выражать в Па, то значения
КР, полученные по уравнениям (1.11) и (1,12) следует умножить на
коэффициент пересчета, равный: 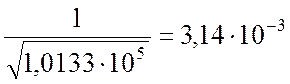
Уравнение (1.9) определяет Хр в неявном виде и решается либо методом последовательных приближений (обычно достаточно 2 – 3 приближения), либо с применением вычислительной техники.
Зная равновесную степень превращения, легко определить равновесный объемный состав газовой смеси:
%SO3 = aXP; % SO2 = a(1-XP); % O2 = b(1-0,5XP);
% N2 = 100- %SO3 - %SO2 - % O2
Цельработы:
Изучить влияние температуры, давления и состава исходной смеси на константу равновесия, равновесную степень превращения SO2 в SO3 и содержание SO3 в равновесной газовой смеси.
Порядок выполнения работы
Запустить имитатор лабораторной работы.
Пользуясь описанием имитатора к лабораторным работам, (см. приложение) установить, согласно заданию, значение давления, объемные концентрации диоксида серы, кислорода и азота на расходомерах, интервал и шаг изменения температуры на термометре. После того как все параметры будут установлены кнопка «Ok» загорится зеленым цветом, что говорит о готовности программы к выполнению расчетов. При наведении на нее курсора мыши появляется соответствующее всплывающее сообщение:
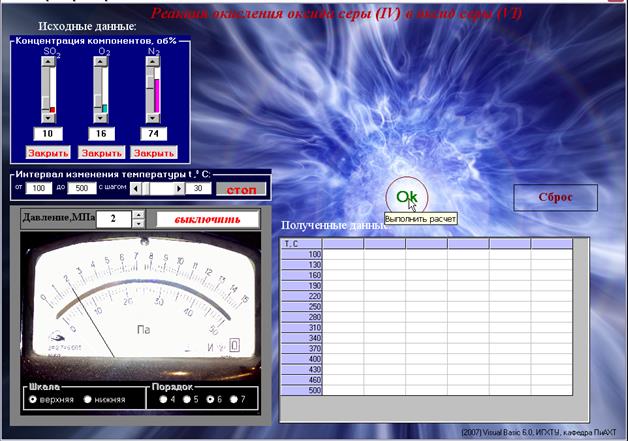
Рис. 1. Панель приборов, готовая к запуску имитатора, к лабораторной работе 1
При нажатии на кнопку «Ok», выполняется расчет заданного процесса по установленным значениям параметров. Кнопка блокируется.
Варианты заданий приведены в таблице 1.1.
Таблица 1.1.
Варианты заданий к лабораторной работе №1
|
№ |
Состав исходного газа, об.% |
Температура, оС |
Давление, МПА |
||||||
|
SO2 |
O2 |
N2 |
начальная |
конечная |
шаг |
||||
|
1 |
9 |
7 |
84 |
200 |
600 |
50 |
0,1 |
0,2 |
0,3 |
|
9 |
10 |
81 |
|||||||
|
9 |
13 |
78 |
|||||||
|
2 |
10 |
7 |
83 |
400 |
800 |
50 |
0,08 |
0,16 |
0,32 |
|
10 |
12 |
78 |
|||||||
|
10 |
15 |
75 |
|||||||
|
3 |
6 |
9 |
85 |
250 |
730 |
60 |
0,1 |
0,2 |
0,3 |
|
9 |
9 |
82 |
|||||||
|
12 |
9 |
79 |
|||||||
|
4 |
7 |
11 |
81 |
300 |
700 |
50 |
0,09 |
0,11 |
0,14 |
|
10 |
11 |
79 |
|||||||
|
13 |
11 |
76 |
|||||||
|
5 |
2 |
18 |
80 |
400 |
800 |
50 |
0,1 |
0,12 |
0,14 |
|
3,5 |
18 |
78,5 |
|||||||
|
5 |
18 |
77 |
|||||||
|
6 |
7 |
14 |
79 |
100 |
660 |
70 |
0,1 |
0,15 |
0,2 |
|
8 |
13 |
79 |
|||||||
|
9 |
12 |
79 |
|||||||
|
7 |
7,5 |
14 |
78,5 |
200 |
600 |
50 |
0,1 |
0,12 |
0,14 |
|
9 |
14 |
77 |
|||||||
|
11,5 |
14 |
74,5 |
|||||||
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.