В пространственной решетке молекул льда молекулы Н2О расположены вплотную друг к другу, но при этом образуют ажурную конструкцию, в которой имеются значительные внутренние пустоты. При плавлении расстояния между ближайшими молекулами Н2О увеличиваются, как и у других веществ, но ажурное строение кристалла ломается и за счет заполнения молекулами внутренних пустот общий объем вещества уменьшается. Поэтому вода оказывается плотнее льда.
Исследования показали, что после плавления в воде остаются отдельные части кристаллической решетки, в которых сохраняются пустоты. Они постепенно разрушаются лишь в процессе дальнейшего нагревания воды. Поэтому вода сжимается при нагревании до температуры 4°С. При 4°С процессы исчезновения пустот и увеличения расстояний между молекулами при нагревании компенсируются, и при дальнейшем нагревании вода начинает расширяться. При охлаждении воды все описанные процессы происходят в обратном порядке. Таким образом, вода имеет наибольшую плотность лишь при 4°С.
Эти свойства воды имеют огромное значение в природе. Расширение воды при замерзании ведет к разрушению горных пород, предохраняет водоемы от промерзания и т. п. (Подумайте, почему на дне рек и озер зимой сохраняется температура 4°С.)
Изменение объема металлов при плавлении и отвердевании имеет существенное значение в литейном деле.
Зависимость температуры и теплоты плавления от давления. Точка плавления
Опыт показывает, что изменение внешнего давления на твердое вещество отражается на температуре плавления этого вещества. В тех случаях, когда объем вещества при плавлении возрастает, увеличение внешнего давления, которое затрудняет процесс плавления, приводит к повышению температуры плавления. Если же объем вещества при плавлении уменьшается, то увеличение внешнего давления ведет к понижению температуры плавления этого вещества, так как повышенное давление в этом случае помогает процессу плавления. Отметим, что только очень большое увеличение давления заметно меняет температуру плавления вещества. Например, чтобы понизить температуру плавления льда на 1К, давление нужно повысить на 130 атм.
Температуру плавления вещества при нормальном атмосферном давлении называют точкой плавления вещества.
Оказывается, что удельная теплота плавления λ тоже зависит от давления. При больших внешних давлениях вещество в процессе расширения должно совершать заметную работу против сил внешнего давления. Поэтому у тех веществ, которые при плавлении расширяются, удельная теплота плавления при увеличении внешнего давления возрастает у льда, а висмута и галлия - убывает. Например, если при нормальном давлении для ртути λ Hg = 11,5-103 Дж/кг и для висмута λ вi = 54,5×10J Дж/кг, то при давлении 12 ×103атм λ Hg = 13,2×103 Дж/кг и λ вi = 54,5 × 103 Дж/кг.
Уравнение теплового баланса при плавлении и кристаллизации
Многие расчеты процессов теплообмена, в которых происходят плавление и отвердевание, проводят с помощью уравнения теплового баланса. В качестве примера рассмотрим, как составляется такое уравнение при определении удельной теплоты плавления льда с помощью калориметра.
Возьмем калориметр массой mg, в котором
находится некоторое количество воды mB при температуре Т1.
Чтобы определить λ льда. в калориметр кусочек тающего льда массой mл при температуре Тпл.
Допустим, что, когда весь лед растаял, в калориметре установилась температура ![]() . Тогда можно считать, что лед получал
теплоту, когда таял, а образовавшаяся из него вода – когда нагревалась до
температуры
. Тогда можно считать, что лед получал
теплоту, когда таял, а образовавшаяся из него вода – когда нагревалась до
температуры ![]() , то есть
, то есть
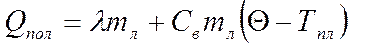
Отдавали же теплоту калориметр и находившаяся в нем вода.
Поэтому ![]() .
.
Так как Qполуч= Qотд, имеем
![]()
Из
последнего уравнения по результатам, полученным из опыта,
вычисляют удельную
теплоту плавления льда. Она равна
λ= 3,3 ×103Дж/кг.
Растворы и сплавы. Охлаждающие смеси
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.