Не оцененные по достоинству современниками исследования М. С. Цвета, более 20 лет остававшиеся невостребованными, послужили мощным стимулом к дальнейшему развитию хроматографии.
Термин «хроматография», введенный М. С. Цветом, сейчас, конечно, не отражает суть современных хроматографических методов. Хроматографической системой может быть не колонка, а лист бумаги, пластинка с тонким слоем сорбента, нить волокнистого материала и т. д. Разделяемые компоненты могут не поглощать в видимой области спектра и детектируются иными способами. Наконец, результат хроматографирования чаще всего представляет собой не цветную картинку, являющуюся моментальным отпечатком ситуации в хроматографической системе (первичная хроматограмма), а зависимость концентраций компонентов на выходе из хроматографической колонки (выходная кривая или вторичная хроматограмма). Однако термин «хроматография» утвердился как название всех методов, в основе которых лежит одно общее явление – динамическая сорбция.
Под сорбцией понимают самопроизвольное концентрирование частиц компонента в данную фазу, обусловленное стремлением системы к состоянию с минимумом свободной энергии. В хроматографических методах реализуются те же фазовые равновесия, что и в классических методах разделения, но одна фаза – сорбент (твердое вещество или жидкость) – неподвижна, а вторая (газ или жидкость), содержащая разделяемые компоненты, перемещается вдоль неподвижной фазы. Иными словами, распределение компонентов между фазами происходит в динамических условиях. Процесс сорбции обратим, и в каждой точке поверхности раздела фаз происходит многократное повторение равновесных (в идеальном случае) актов сорбции-десорбции. Вследствие этого даже малейшее различие в физических, физико-химических или химических свойствах разделяемых компонентов дает возможность успешного их разделения. Если вспомнить, что в классических методах желаемая степень разделения достижима лишь при достаточно большом различии констант (коэффициентов) распределения, а в противном случае приходится прибегать к многократному повторению стадий разделения, становится понятным, что хроматографическое разделение достаточно эффективно даже при небольших различиях этих констант. Итак, суть любого хроматографического процесса сводится к тому, что за счет различия в сродстве к сорбенту компоненты по-разному сорбируются (удерживаются) им и поэтому двигаются в системе с разной средней скоростью. Эту взаимосвязь в идеальном случае ясно отражает основное уравнение равновесной хроматографии:
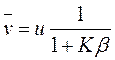 ,
(1)
,
(1)
где ![]() – средняя
скорость движения разделяемого компонента, u – скорость
движения молекул подвижной фазы, отношение объемов неподвижной и подвижной фазы
– средняя
скорость движения разделяемого компонента, u – скорость
движения молекул подвижной фазы, отношение объемов неподвижной и подвижной фазы
![]() называется фазовым отношением,
называется фазовым отношением, ![]() – коэффициент распределения, равный отношению
концентрации разделяемого компонента в неподвижной (Cs)
и подвижной (Cm) фазах.
– коэффициент распределения, равный отношению
концентрации разделяемого компонента в неподвижной (Cs)
и подвижной (Cm) фазах.
С выводом этого уравнения можно познакомиться, например, в руководстве [4]. Смысл же его предельно прост и прекрасно отражает качественную сторону любого хроматографического процесса – компонент с большим сродством к сорбенту движется с меньшей скоростью и наоборот: KA < KB , nA < nB. В предельных случаях K → ∞, ν → 0 (компонент вообще не движется) и K → 0, ν → u (компонент перемещается со скоростью подвижной фазы).
В результате разной скорости движения за одно и то же время компоненты проходят различные расстояния и занимают различные положения (зоны) в хроматографической системе или появляются на выходе из нее в разное время. Далее задача химика-аналитика сводится к грамотной обработке полученной хроматограммы, т. е. зависимости аналитического сигнала от времени или объема подвижной фазы, для определения качественного и количественного состава пробы.
Названия хроматографических методов обычно связаны с той или иной их классификацией. Существует несколько способов классификации хроматографических методов.
1. По агрегатному состоянию подвижной фазы и неподвижной фазы.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.