― фосфора — 0,157 – 0,022 = 0,135 кг
― серы — 0,027 – 0,016 = 0,011 кг
С учетом извести и шлака 1-го периода серы поступило в шлак 2-го периода
0,011 + 0,001 + 0,004 = 0,016 кг.
Необходимо внести изменения в таблицу 11 в связи с уточнением содержания в шлаке и металле примесей.
|
Элемент, оксид |
Количество окислившегося элемента, кг |
Потребное количество кислорода, кг |
Количество образовавшегося оксида, кг |
|
|
0,427 |
|
0,996 |
|
|
0,047 |
|
0,172 |
|
|
0,082 |
|
0,106 |
|
|
0,135 |
|
0,309 |
|
|
0,2 |
|
0,286 |
|
Итого |
|
0,978 |
|
|
* 0,011 – количество серы, удаленной из металла |
|||
Как видно, в таблице 12 изменилось только содержание MnO, Р2О5 и S. Поэтому новая сумма шлакообразующих без оксидов железа составит:
Мок = 6,542 – (0,364 + 0,852 + 0,013) + (0,285 + 0,833 + 0,011) = 6,442 кг
Определим уточненное количество шлака 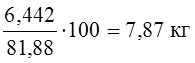 .
.
На основе полученных данных в таблице 11 и 12 определим уточненный состав шлака в конце продувки.
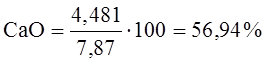
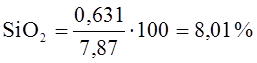
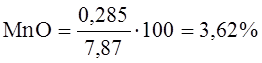
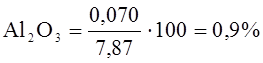
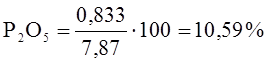
![]()
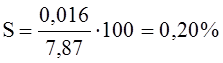
![]()
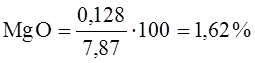
Итого сумма составляет 100%
Основность шлака 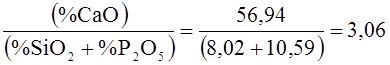
Коэффициенты распределения:
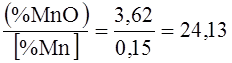
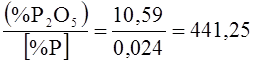
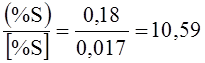
Баланс оксидов железа в шлаке
Исходными материалами вносится оксида железа (Fe2O3)и.м. = 0,361 кг. После скачивания шлака в шлаке остается Fe2O3 0,361 – 0,166 = 0,195 кг.
В шлаке должно быть
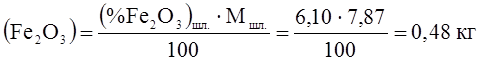 .
.
Следовательно, за счет горения железа должно образоваться
Fe2O3 = 0,48 – 0,195 = 0,285 кг.
Для этого должно окислится железа
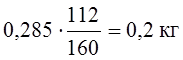
и потребуется кислорода 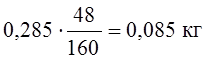 .
.
Исходными материалами вносится оксида двухатомного железа
(FeO)исх.м. = 0,148 кг.
После скачивания шлака останется
(FeO) = 0,148 – 0,388 = - 0,240 кг.
В шлаке должно быть
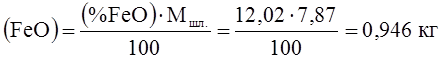 .
.
Следовательно, за счет окисления железа должно быть получено
(FeO) = 0,946 – (- 0,240) = 1,186 кг.
Для этого должно окислится железа
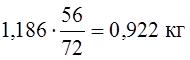
и потребуется кислорода 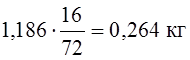 .
.
Итого на образование оксидов железа в шлаке должно окислится железа
0,2 + 0,922 = 1,122 кг,
для чего требуется кислорода 0,085 + 0,264 = 0,349 кг.
Расчет технического расхода кислорода
Всего необходимо кислорода на окисление примесей чугуна и железа до (Fe2O3)пыль (таблица 12) 0,978 кг, на окисление железа до FeO и Fe2O3 шлака 0,349 кг.
Некоторое количество кислорода растворится в металле (таблица 13).
|
[%С] |
0,05 |
0,10 |
0,15 |
0,20 |
0,30 |
0,40 |
0,70 |
|
[%О] |
0,065 |
0,055 |
0,045 |
0,035 |
0,030 |
0,027 |
0,022 |
Для данного расчета при [%С] = 0,17 содержание кислорода равно [%О] = 0,154.
Всего необходимо кислорода 0,978 + 0,349 + 0,154 = 1,481 кг.
Усвоение кислорода металлом колеблется в пределах 90-98%. Принимаем 96%.
Тогда расход кислорода составит 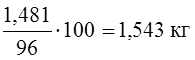 или
или 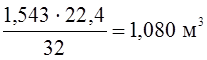 .
.
Чистота технического кислорода колеблется в пределах 98,5-99,8%. принимаем 99,6%.
Тогда его потребуется 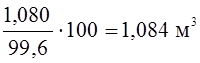 .
.
Вместе с кислородом поступит азота 1,084 – 1,080 =
0,004 м3 или 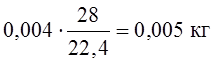 .
.
Из этого количества азота растворяется в металле 0,003 кг (обычно 0,003-0,006%) и уносится из конвертера 0,005 – 0,003 = 0,002 кг.
Всего технического кислорода требуется 1,543 + 0,005 = 1,548 кг.
Расчет количества и состава газов, выходящих из горловины конвертера
Считаем, что выделяющиеся при нагреве извести, известняка и шлака СО2 и Н2О не участвуют в окислении примесей металлической шихты.
Во время продувки образуется газов:
СО2 — от горения углерода — 0,172 кг
СО2 — из извести — 0,126 кг
СО2 — из известняка — 0,053 кг
СО2 — из шлака 1-го периода — 0,246 кг
Итого 0,597 кг
СО — от горения углерода — 0,996 кг
N2 — из дутья — 0,002 кг
Н2О — из извести — 0,014 кг
Н2О — из шлака 1-го периода — 0,021 кг
Итого Н2О 0,035 кг
О2 — из дутья — 1,543 – 1,481 = 0,062 кг
На основе выполненных расчетов уточним состав и количество газов (таблица 14).
|
Составляющие газы |
Количество газов |
Содержание, % |
||
|
кг |
м3 |
весовых |
объемных |
|
|
СО2 |
0,597 |
0,304 |
35,28 |
25,57 |
|
СО |
0,996 |
0,797 |
58,87 |
67,03 |
|
N2 |
0,002 |
0,002 |
0,12 |
0,16 |
|
Н2О |
0,035 |
0,043 |
2,07 |
3,62 |
|
О2 |
0,062 |
0,043 |
3,66 |
3,62 |
|
Итого |
1,692 |
1,189 |
100 |
100 |
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.