Металлическая связь в основном проявляется у элементов металлической группы. Образование устойчивых атомных групп при металлической связи происходит следующим образом. При конденсации металлических паров валентные электроны утрачивают связь с отдельными атомами и обобществляются на все количество атомов, содержащихся в объеме. В связи с тем, что атом при потере валентного электрона становится положительным ионом, металлической жидкое и твердое тело можно рассматривать как объем, состоящий из положительных ионов, погруженных в среду, образованную коллективными электронами.
Коллективные электроны могут свободно перемещаться в объеме металла, так как они не связаны с определенными атомами и образуют как бы своеобразный электронный газ, плотность которого будет возрастать с увеличением валентности металлического элемента. Связь в металлической решетке возникает вследствие взаимодействия положительных ионов с коллективными электронами. Свободные электроны, находящиеся между ионами, как бы стягивают их, стремясь уравновесить силы отталкивания между одноименно заряженными ионами.
Особенностью металлической связи по сравнению с другими видами является отсутствие у нее насыщения. При образовании металлической связи не все валентные электроны атомов принимают участие в образовании электронного газа, степень коллективизации зависит от прочности валентных электронов с ядром. Валентные электроны щелочных металлов наиболее слабо связаны с атомами, и поэтому они легко коллективизируются. В общем случае, чем правее и выше расположен элемент в Таблице Менделеева, тем сильнее силы связи валентных электронов с атомами и труднее происходит их коллективизация.
1.2. Классическая электронная теория металлов
Установление наличия в металлах свободных электронов позволило объяснить особенности атомного строения и свойства металлов и сплавов с позиций так называемой электронной теории. Эта теория имеет три направления развития: классическая, квантовая и зонная теории.
Согласно классической теории, металл описывается как совокупность сферически-симметричных ионов, окруженных электронным газом. Предполагается, что в металле электроны газа движутся свободно во всех направлениях, и это движение подчиняется законам классической кинетической теории газов.
Средняя кинетическая энергия движения электрона равна его средней кинетической энергии поступательного движения, следовательно
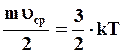
или
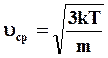 (1.1)
(1.1)
где m – масса электрона; k – постоянная Больцмана; T – абсолютная температура; υср – среднеквадратичная скорость беспорядочного теплового движения электрона.
В обычных условиях движение электронов хаотично, но при наложении электрического поля оно становится вполне определенным: от отрицательного полюса к положительному, порождая электрический ток в металле. Столкновение между ионами не позволяет электронам бесконечно увеличивать скорость под действием электрического поля. Поэтому при некотором значении напряженности электрического поля достигается устойчивый электрический ток, пропорциональный этой напряженности. Плотность этого электрического тока определится выражением
![]() (1.2)
(1.2)
где n – число свободных электронов в единице объема; e – заряд электрона; u – добавочная скорость, которую приобретает электрон в направлении силовых линий электрического поля в промежутках от одного столкновения до другого под действием поля за время τ.
Добавочная скорость может быть определена из выражения
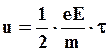 (1.3)
(1.3)
где Е – напряженность электрического поля.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.