В водных растворах этилацетат омыляется щелочью
CH3COOC2H5 + OH– ¾® CH3COO– + C2H5OH.
a–y b–y y y
Здесь
a и b – начальные концентрации эфира и щелочи, ![]() (глубина реакции). Реакция имеет второй
порядок:
(глубина реакции). Реакция имеет второй
порядок:
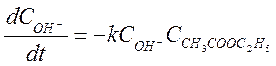 .
.
Вводя y, получаем
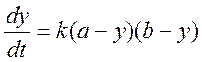 .
.
После интегрирования имеем
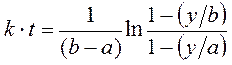 ,
(11)
,
(11)
где
![]() – текущая концентрация
– текущая концентрация ![]() .
.
Как видно из уравнения (11), для расчета константы скорости нужно знать начальную концентрацию щелочи b, начальную концентрацию этилацетата a и зависимость от времени глубины реакции y:
![]()
![]() (12)
(12)
Начальные концентрации щелочи и этилацетата известны. Кроме того, как будет видно из дальнейшего, они могут быть определены из измерений электропроводности c реакционного раствора.
В произвольный момент времени электропроводность c связана с концентрациями реагентов (выраженными в моль / м3) и ионными электропроводностями li следующим образом:
![]() . (13)
. (13)
Величина cconst – это вклад в электропроводность раствора, определяемый ионами Na+, концентрация которых постоянна в ходе реакции, а также вклад в электропроводность от растворенного углекислого газа.
Поскольку концентрация ацетат-ионов ![]()
![]() равна убыли
концентрации щелочи, то формулу (13) можно переписать, как
равна убыли
концентрации щелочи, то формулу (13) можно переписать, как
![]() .
.![]() (14)
(14)
Начальная электропроводность раствора (c0) равна
![]() .
(15)
.
(15)
Если этилацетат взят в избытке, то по окончании реакции щелочь израсходуется полностью и электропроводность раствора будет равна
![]() .
(16)
.
(16)
Комбинируя соотношения (14)–(16), находим
![]() ;
(17)
;
(17)
![]() .
(18)
.
(18)
Отсюда, разделив эти два равенства одно на другое, получаем простую формулу для расчета текущей концентрации щелочи:
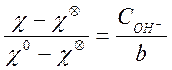 или
или 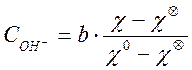 . (19)
. (19)
Подчеркнем,
что ![]() – это электропроводность раствора по
окончании реакции, в случае, когда этилацетат взят в избытке и щелочь
расходуется полностью.
– это электропроводность раствора по
окончании реакции, в случае, когда этилацетат взят в избытке и щелочь
расходуется полностью.
Если этилацетат взят в недостатке или начальные
концентрации щелочи и этилацетата равны, то формула (19) также применима для
расчёта текущей концентрации щелочи, однако, для её использования необходимо в
параллельном опыте измерить величину ![]() .
.
Конечную электропроводность раствора после завершения
реакции при недостатке этилацетата и неполном расходовании щелочи будем
обозначать, как ![]() . Величина
. Величина ![]() , как видно, не нужна для расчета текущей
концентрации щелочи и константы скорости реакции. Однако она весьма полезна для
определения начальной концентрации этилацетата. Действительно, заменяя в
формуле (19)
, как видно, не нужна для расчета текущей
концентрации щелочи и константы скорости реакции. Однако она весьма полезна для
определения начальной концентрации этилацетата. Действительно, заменяя в
формуле (19) ![]() на
на ![]() получаем
получаем
 . (20)
. (20)
Поскольку
![]() имеется возможность определить началь-ную
концентрацию этилацетата из кондуктометрических данных. Это становится существенным,
если количество добавленного этилацетата измерено только приблизительно. При
этом
имеется возможность определить началь-ную
концентрацию этилацетата из кондуктометрических данных. Это становится существенным,
если количество добавленного этилацетата измерено только приблизительно. При
этом ![]() и
и ![]() измеряются
в параллельных опытах при одинаковой начальной концентрации щелочи, но при
различной начальной концентрации этилацетата. Величина
измеряются
в параллельных опытах при одинаковой начальной концентрации щелочи, но при
различной начальной концентрации этилацетата. Величина ![]() измеряется
при недостатке этилацетата, а
измеряется
при недостатке этилацетата, а ![]() – при избытке.
– при избытке.
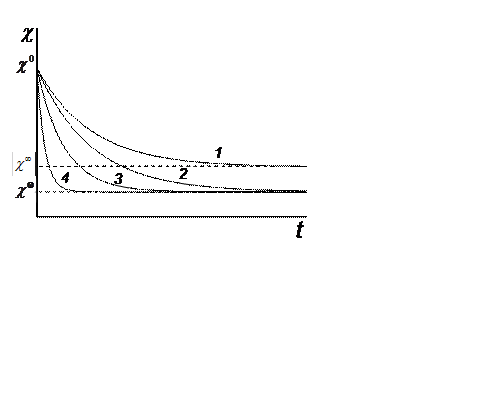

Рис. 7. Зависимость удельной электропроводности реакционной смеси от времени в серии опытов при различной начальной концентрации этилацетата (a) и одинаковой начальной концентрации щелочи (b): 1 – (a < b); 2 – (a = b); 3 – (a > b); 4 – (a >> b)
Проведение измерений и обработка результатов
Три колбы на 50 мл заполняют раствором 0.02М NaOH в воде и термостатируют их при 25 ± 1 оС.
К раствору в колбе №1 добавляют избыток
этилацетата (200 мкл), колбу закрывают, перемешивают и оставляют
в термостате на 2 ч. После завершения реакции измеряют электропроводность ![]() .
.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.