 |
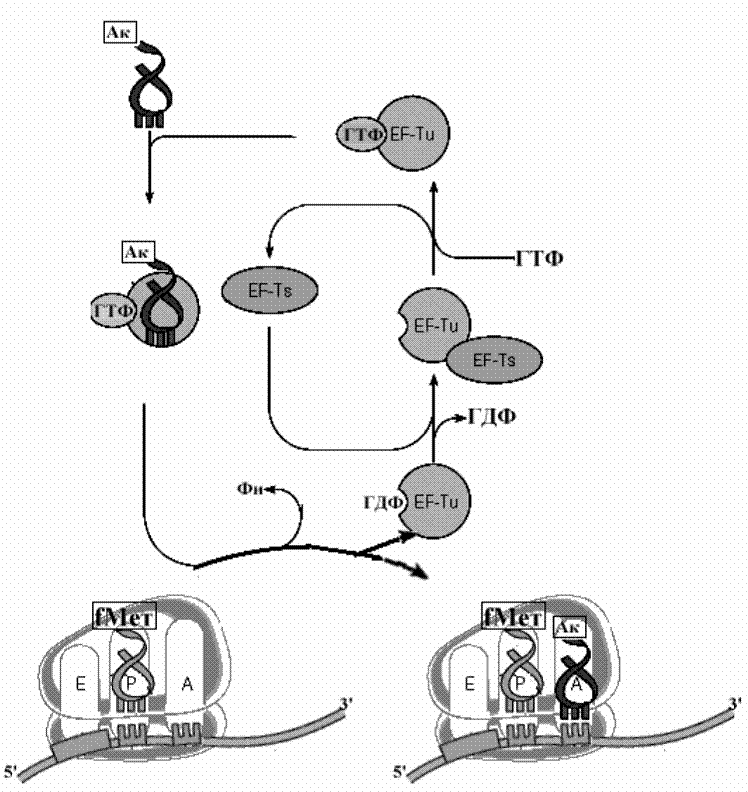
Рис..Схема механизма инициации трансляции у эукариот.
везде любая полипептидная цепь, синтезируемая на рибосоме, начинается с метионина. Лишь потом, в ходе трансляции или после нее, этот концевой метионин может отщепиться специальной протеазой, что и происходит в большинстве случаев
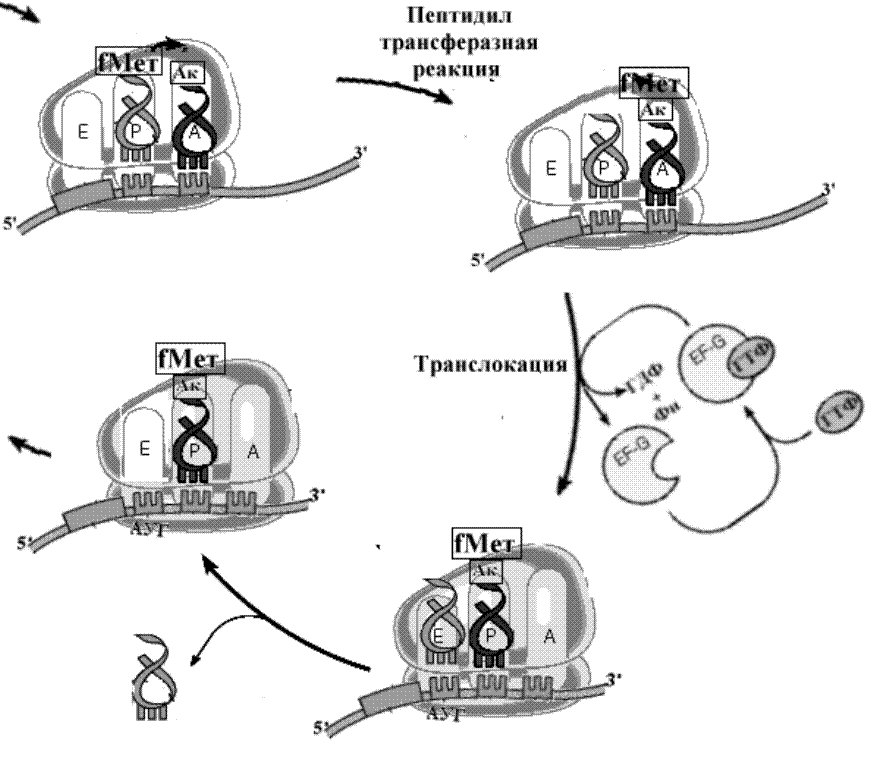 |
Рис. Схема реакций механизма элонгации процесса трансляции.
На этом этапе в процесс включается свободная большая рибосомная субъединица. Взаимодействуя с малой субчастицей и фактором IF2, большая суъединица активирует ГТФазную активность IF2, в результате чего ГТФ гидролизуется до ГДФ и ортофосфата, что приводит к снижению сродства IF2 к инициирующей метионил-тРНК и IF2 с ГДФ легко вытесняются из рибосомы. На большой субъединице формируется пептидильный участок (Р участок), на котором размещается инициирующая метионил-тРНК. Вытесняются одновременно и все другие факторы инициации, включая IF3 . В итоге образуется полная 70S [ у прокариот] или 80S [ у эукариот] рибосома с Р-участком, занятым инициирующей метионил-тРНК, и с вакантными А- и Е участками .
Этот завершающий шаг процесса инициации начинает образование и элонгацию пептида. На вакантный А-участок поступает первая аминоацил-тРНК в комплексе с фактором элонгации EF1(EF-Tu у прокариот) и ГТФ. После гидролиза ГТФ, EF1(EF-Tu) с ГДФ покидают рибосому, а аминоацил-тРНК, связанная на А-участке, получает возможность реагировать с инициирующей метионил-тРНК в реакции транспептидации, катализируемой большой субъединицей рибосомы. Фактор EF1 (EF-Tu) вновь подключается в процесс трансляции после замены ГДФ на ГТФ при участии факторов, стимулирующих этот обмен гуаниловых нуклеотидов. Так начинается элонгация.
Конкретные генетические функции малой рибосомной субъединицы в ходе инициации трансляции могут быть разделены на три группы процессов с участием - мРНК. Во-первых, малая рибосомная субъединица, связывая мРНК, служит первичным акцептором генетической информации для белоксинтезирующего аппарата. Во-вторых, она с участием факторов инициации обеспечивает узнавание инициирующего участка на иРНК путем непосредственного узнавания его структуры и присоединения [у прокариот], или путем сканирования цепи мРНК [у эукариот]. И, в-третьих, малая рибосомная субъединица обеспечивает кодон-антикодоновое взаимодействие инициирующего кодона иРНК с антикодоном инициирующей тРНК. Малая рибосомная субъединица таким образом, является главным " действующим лицом " всего сценария инициации .
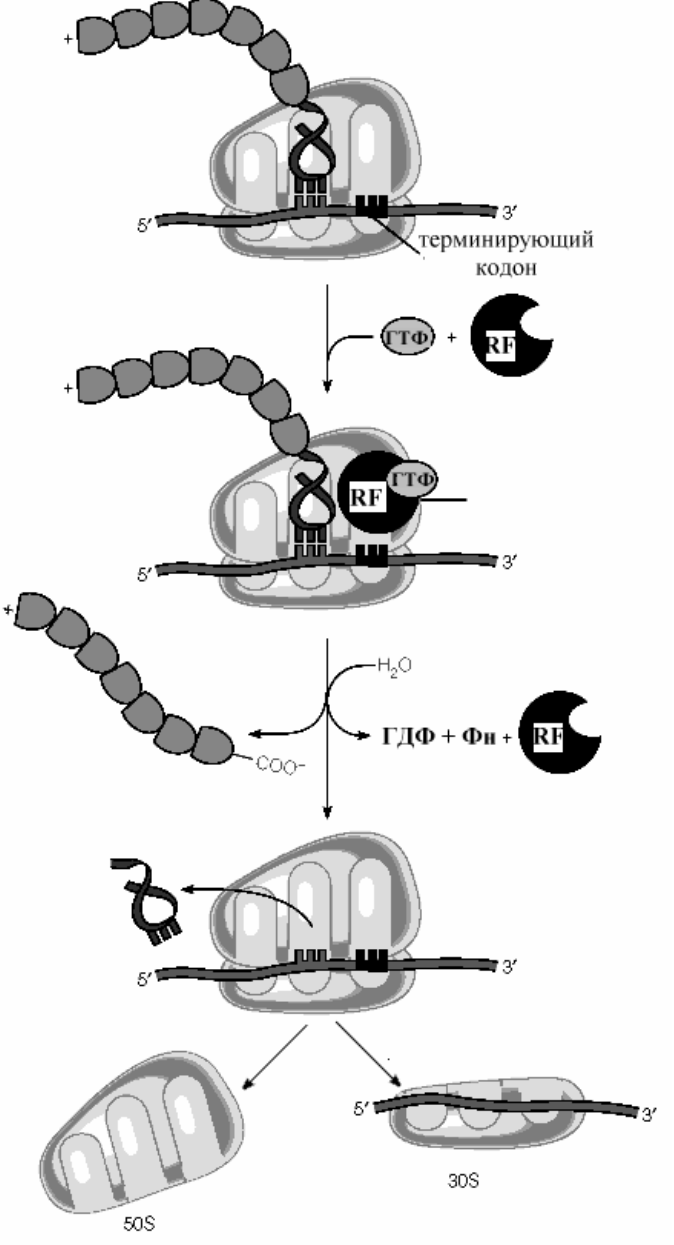
Большая рибосомная субчастица включается в процесс на завершающем этапе процесса инициации и в соответствии с указанным выше " разделением труда " исполняет биохимическую часть функций . Она индуцирует гидролиз ГТФ на факторе инициации IF2, вытесняет все факторы инициации с малой рибосомной субчастицы, надлежащим образом устанавливает субстраты - инициаторную метионил-тРНК и связывающуюся с А-участком аминоацил-тРНК - в своем пептидилтрансферазном центре и, наконец, катализирует реакцию транспептидации между субстратами . Итак, после включения механизма инициация Рис.10-10. Схема реакций фазы терминации в мезанизме трансляции. трансляции, рибосома обеспечивает прочный комплементарный контакт связанных с ней
 |
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.