2.2. Бимолекулярной является реакция: а) 2А®С;
б) А®С+Д;
в) А®В;
г) А+В+С®Д;
д) А®В+С+Д.
2.3.Мгновенная
скорость образования продукта реакций В : 2А®В, выражается
соотношением: а) ![]()
б) ![]()
в) ![]()
г) ![]()
д) ![]()
2.4.Зависимость скорости химической реакции от температуры (в небольшом интервале температур) описывает уравнение: а)Вант-Гоффа; б) Ле Шателье; в)Аррениуса; г)Гульдберга и Вааге; д)Максвелла- Больцмана.
2.5.Кинетическое уравнение реакции 1-го порядка в дифференциальной и интегральной формах:
а) ![]()
![]() ; б)
; б) ![]()
![]() ;
;
в) ![]()
![]() ; г)
; г) ![]()
![]() ; д)
; д) ![]()
![]()
2.6. Единицы измерения константы скорости реакции первого порядка: а)с-1;
б) дм3/(моль·с);
в) моль/(дм3 с);
г) дм3(моль2·с);
д) моль-1·с-1·дм-3
2.7.Зависимость скорости химической реакции от концентрации реагентов описывает закон:
а) Аррениуса;
б) Вант-Гоффа;
в) Бекетова;
г) Гульдберга и Вааге;
д) Бертолле.
2.8.Предэкспоненциальный множитель в уравнении Аррениуса определяет:
а) число активных столкновений в системе;
б) общее число столкновений в единице объема в единицу времени;
в) энергию активации реагентов; г) величину активационного барьера;
д) влияние температуры на химическое взаимодействие.
2.9.Скорость последовательной реакции
CO(г) + 2CuO(т) Û Cu2O(т) + CO2(г) (медленная стадия)
Cu2O(т) + 1/2O2(г) Û2CuO(т) (быстрая стадия)
в соответствии с законом действия масс выразиться уравнением:
а)![]()
б) ![]()
в) ![]()
г) ![]()
д) ![]()
2.10.Графическая зависимость ![]() для
реакции первого порядка:
для
реакции первого порядка:
а)![]()
![]()
![]()
![]()
![]() υ б)
υ в) υ г) υ
υ б)
υ в) υ г) υ
 |
 |
||||
 |
|||||
![]()
![]()
![]()
![]() с с
с с д)υ
с с
с с д)υ![]()
с
2.11.При повышении температуры на 20 градусов скорость химической реакции возросла в 4 раза; температурный коэффициент равен:
а) 2,
б) 4,
в) 20,
г) 5 (20:4),
д) 80 (20 · 4)
2.12.Константа равновесия химической реакции в газовой фазе не зависит от:
а) температуры; б) природы реагирующих веществ; в) теплового эффекта; г) присутствия катализаторов; д) энергии активации.
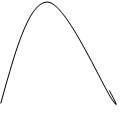
2.13. Изменение концентрации реагентов во времени для обратимой простой реакции АÛВ выражает графическая зависимость:
![]()
![]() С С
С С
С С
С С

![]()



![]()
![]() а) А
б) А в) А г) А
а) А
б) А в) А г) А
![]() В
В
![]()
![]()
![]()
![]() В0 t В0 t1/2 t В0
t 0 t
В0 t В0 t1/2 t В0
t 0 t
![]() д)С
д)С
А
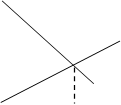
![]() В0 t1/2 t
В0 t1/2 t
2.14. Пероксидное окисление липидов протекает по механизму а) последовательных реакций; б) параллельных; в) сопряженных; г) цепных; д) обратимых.
2.15.Катализатор - вещество, изменяющее скорость химической или биохимической реакции путем:
а) увеличения числа реакционных центров; б) уменьшения энергии активации процесса;
в) участия в образовании продуктов реакции; г) увеличения теплового эффекта реакции;
д) уменьшения теплового эффекта реакции.
2.16. Механизм ферментативного катализа описывается следующей схемой: S + Е Û SЕ
SЕ Û Е + Р, где S - субстрат, Е - фермент, ЕS - фермент-субстратный комплекс,
Р - продукт, а скорость процесса определяется: а) скоростью подвода субстрата к ферменту; б) скоростью образования фермент-субстратного комплекса; в) скоростью превращения субстрата в продукт;
г) скоростью отвода продукта из сферы реакции; д) суммой скоростей подвода субстрата к ферменту и образования SE- комплекса.
2.17.
Время полупревращения τ1/2 для реакции первого порядка определяется
как а) ![]() ;
;
б) ![]()
в) ![]()
г) ![]()
д) ![]()
2.18. Величина константы равновесия Kc зависит от:
а) соотношения концентраций реагентов; б) соотношения активностей реагентов;
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.