Относительная нуклеофильность галогенид-ионов зависит от природы растворителя. В протонной среде она уменьшается в ряду I- > Br- > Cl- > F-, неполярной апротонной среде – в обратной последовательности. Реакции с наименее сольватируемым иодид-ионом быстрее протекают в ДМФА, чем в метаноле. Поэтому замещение атомов галогенов и нитрогруппы при взаимодействии с иодидами щелочных металлов предпочтительно проводить в апротонной среде. Например, неактивированный атом брома замещается атомом йода при обработке м-бромтолуола, о- и п-броманизолов избытком КI в присутствии CuI в качестве катализатора (иногда используют порошкообразный никель) в гексаметилтриамидофосфате при 150-160 °С в течение 5-6 часов (выходы продуктов – 60-80%) [14]. Но в препаративных целях подобные методы используют редко.
Из бромистых и хлористых арилмагниевых соединений, действуя на них раствором йода в эфире, можно получить соответствующие йодистые арилы. Например, из бромистого фенилмагния этим путём можно получить йодбензол с выходом 90%. [6]
Один из новых методов йодирования ароматических соединений состоит в действие йода на ртутьароматические соединения:
2 ArHgHCl + 2 I2
![]() 2 ArI + HgCl2 + HgI2
2 ArI + HgCl2 + HgI2
По этому методу выходы продуктов реакции уступают выходам, достигаемым по методу Зандмейера.
Суть последнего состоит в замещении диазогруппы атомом йода. Реакция протекает по механизму радикального нуклеофильного мономолекулярного замещения (SRN1):
ArN2+
+ I- ![]() Ar∙
Ar∙ ![]() ArI
ArI
Рассмотрим этот механизм подобнее. Помимо аринов, аренид-ионов и арил-катионов в качестве промежуточных частиц в реакциях нуклеофильного замещения, протекающих по типу отщепления-присоединения, могут выступать так же свободные радикалы. Их генерирование при нуклеофильном замещении происходит в результате распада анион-радикала, возникающего при переносе к субстрату одного электрона. Отщепляя замещаемый атом или группу атомов в виде аниона X-, анион-радикал трансформируется в свободный арильный радикал Ar∙, который быстро соединяется с нуклеофилом. Образующийся анион-радикал конечного продукта отдаёт электрон молекуле исходного соединения, завершая цикл и начиная новое звено цепи:
ArХ ![]() ArХ-∙
ArХ-∙ ![]() Ar∙
Ar∙ ![]() ArY-∙
ArY-∙ ![]() ArY + ArХ-∙
ArY + ArХ-∙
Зарождение цепи с генерированием анион-радикала происходит путём восстановления щелочным металлом, часто в жидком аммиаке (сольватированный электрон), электрохимическиили путём переноса электрона от нуклеофила при фотохимическом инициировании, а иногда без него.
Замещение по механизму SRN1 не требует присутствия в субстрате активирующих заместителей, протекает в мягких условиях самыми разнообразными нуклеофилами и часто с хорошим выходом. [14]
В рассматриваемом нами случае реакция замещения диазогруппы йодом проходит уже при добавлении раствора КI или NaI к кислому раствору сульфата или хлорида диазония. Так, при добавлении раствора КI к хлориду фенилазония главным получается йодбензол с выходом около 80%. [6] Положительное влияние на скорость и выходы продуктов реакции оказывает нитрогруппа, а так же галоид в орто- и пара-положении, в то время как наличие в том же положении группы –СН3 (а так же группы –ОСН3) и её аналогов отрицательно влияет на скорость реакции и её выход.
Таким образом, благодаря мужественным синтетикам, разрабатывающим новые методы получения разнообразных йодпроизводных ароматических соединений, органическая химия не стоит на одном месте! Ура, товарищи!!!
3. Общая часть.
Алкилирование кариофилленом различных фенолов исследовано в работе [15]. В ней показано что, подбирая соответствующий кислотный алюмосиликат, а также соответствующие условия проведения синтеза, можно добиться хорошей селективности реакции и высоких выходов целевого продукта.
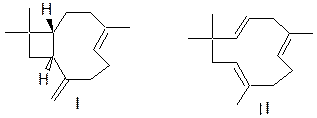 |
Реакцию алкилирования резорцина проводили смесью (-)-транскариофиллена (I) и гумулена (II), легко получаемой из нефенольной части гвоздичного масла.
Использование чистого кариофиллена, конечно, обеспечивает более высокие выходы РПК. Но очистка кариофиллена сама по себе является сложной процедурой, требующей …. И сопровождающейся большими потерями кариофиллена. В конечном итоге нижеуказанный способ получения РПК является более выгодным.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.