происходит нагревание. Если нагревание происходит при
постоянном объеме, то: 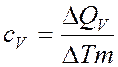 , где
, где ![]() , т.е. все сообщаемое количество теплоты
идет на изменение внутренней энергии системы. Изменение внутренней энергии
смеси газа определяется формулой:
, т.е. все сообщаемое количество теплоты
идет на изменение внутренней энергии системы. Изменение внутренней энергии
смеси газа определяется формулой: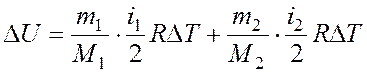 , где i1 и i2 – число степеней свободы
первого и второго газов.
, где i1 и i2 – число степеней свободы
первого и второго газов.
Окончательно получим: 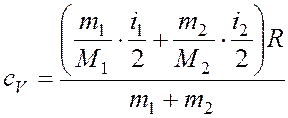 . (1)
. (1)
Если нагревание происходит при постоянном давлении, то
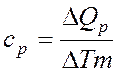 , (2)
, (2)
где ![]() , т.е. сообщаемое газу
количество теплоты идет не только на изменение внутренней энергии, но и на
работу по расширению газа. Работа при изобарическом расширении для каждого газа
равна:
, т.е. сообщаемое газу
количество теплоты идет не только на изменение внутренней энергии, но и на
работу по расширению газа. Работа при изобарическом расширении для каждого газа
равна: 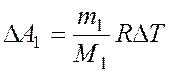 ;
; 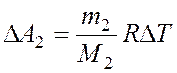 ,
поэтому:
,
поэтому:
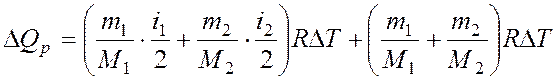 .
.
Подставляя это значение в уравнение (2), получим:
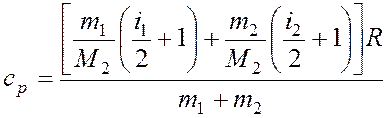 .
.
Произведем вычисления:
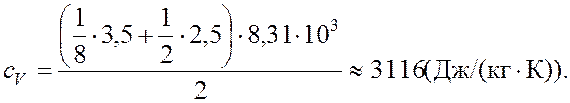
Ответ: 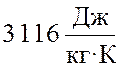 .
.
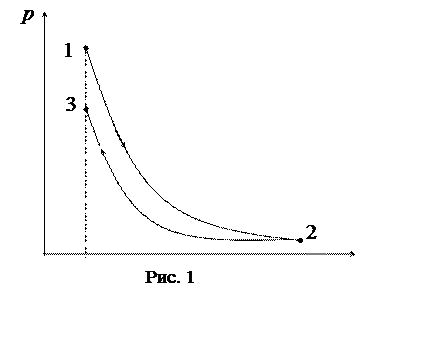
Задача 13. В цилиндре под поршнем находится водород, который имеет массу 0,02 кг и начальную температуру 27°С. Водород сначала расширился адиабатически, увеличив свой объем в 5 раз, а затем был сжат изотермически, причем объем газа уменьшился в 5 раз. Найти температуру в конце адиабатического расширения и работу, совершаемую газом. Изобразить процесс графически.
|
Дано: m = 0,02 кг Т1 = 27°С = 300 К М = 2 кг/кмоль
i = 5 |
Решение: При адиабатном процессе температура и объем газа
связаны соотношением:
|
|
T2 - ? А - ? |
постоянном давлении и постоянном объеме. Для водорода γ = 1,4.
Отсюда выражение для конечной температуры Т2 будет:
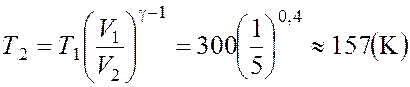 .
.
Работа А1 газа при адиабатическом расширении равна изменению внутренней энергии:
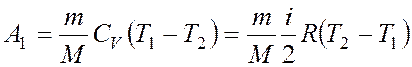 .
.
|
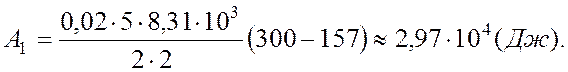
Работа А2 газа при изотермическом
процессе может быть выражена в виде: 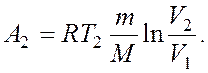
|
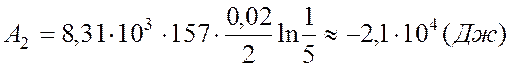 .
.
Знак «минус» показывает, что при сжатии газа работа совершается над газом внешними силами. Полная работа, совершенная газом при описанных процессах, равна:
|
График процесса приведен на рисунке 1.
 |
Ответ: 8,7 · 103 Дж.
Задача 14. Кислород массой m= 2 кг занимает объем V1= 1 м3 и находится под давлением р1= 0,2 МПа. Газ был нагрет сначала при постоянном давлении до объема V2= 3 м3, а затем при постоянном объеме до давления р3 = 0,5 МПа. Найти изменение ΔU внутренней энергии газа, совершенную им работу А и количество теплоты Q, переданное газу. Построить график процесса.
|
Дано: m = 2 кг М = 32 кг/моль V1= 1 м3 р1 = р2 = 2·105 Мпа V2= 3 м3 р3 = 5·105 Мпа R= 8,31·10 –3 Дж/(кмоль·К) |
Решение: Изменение внутренней энергии газа выражается формулой:
|
|
ΔU - ? А - ? Q - ? |
Начальную и конечную температуры найдем, используя уравнение Менделеева - Клайперона:
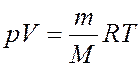 . (2)
. (2)
Решая его относительно Т,
получим: 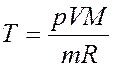 (3)
(3)
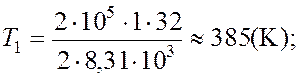
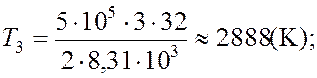
Подставляя
в выражение (1) числовые значения входящих в него величин, находим: 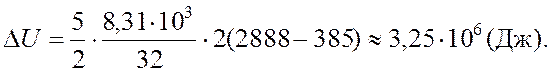
Работа расширения газа при постоянном давлении
выражается формулой: 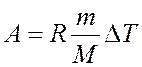 . Подставив числовые значения,
получим:
. Подставив числовые значения,
получим:
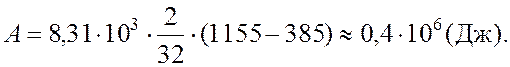
Работа газа, нагреваемого при постоянном объеме, равна
нулю, т.е. А2 = 0. Следовательно, полная работа,
совершенная газом, равна: ![]() . Согласно первому
началу термодинамики количество теплоты Q, переданное
газу, равно сумме изменения внутренней энергии ΔU и работы А:
. Согласно первому
началу термодинамики количество теплоты Q, переданное
газу, равно сумме изменения внутренней энергии ΔU и работы А: ![]() , следовательно:
, следовательно: ![]() .
.
График процесса приведен на рисунке 2.
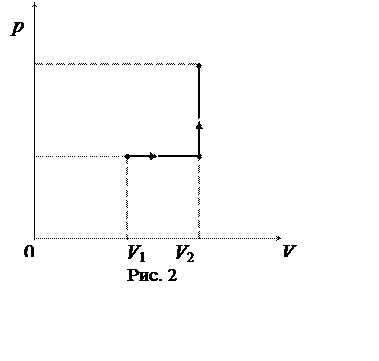 |
Ответ: 3,65 МДж.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.