Температура диссоциации при давлении 10–3 ат, °С 1980+50
Температура кипения, °С 2590
Твердость по шкале Мооса 6—7
Температура начала деформации под нагрузкой 2 кГ/см2, °С 650
Коэффициент линейного расширения, 1/град, в интервале температур, °С:
20—300 4,3––10–6
300—1100 3,0––10–6
Теплопроводность при 1100 °С, кал(сек•см•град) 38––10–4
Термостойкость Плохая до 320°С, отличная выше 320 °С
Химическая стойкость:
в восстановительной атмосфере Плохая к углероду » к кислым шлакам Хорошая к основным шлакам Плохая
Диэлектрическая проницаемость при комнатной температуре, ф/м. 4,6
Удельное электросопротивление, ом • см, при температуре, °С:
20 МО14
1300 5––10–3
Магнитная восприимчивость 0,45––10–6
Исследования показали [26; 27], что температура плавления кремнезема значительно снижается даже при наличии небольших количеств наиболее распространенных примесей глинозема. Из рассмотрения диаграммы равновесия (см. рис. 11) видно, что наиболее низкая точка плавления в этой системе соответствует температуре 1545 °С при содержании около 5 % А12О3. Установлено, что чем чище кремнезем, тем лучше он противостоит действию химических агентов. Чем меньше плотность и чем больше удельная поверхность, тем скорее растворяется кремнезем, например в щелочах, во фтористоводородной кислоте, и тем легче вступает в реакцию. Быстрее всего растворяется аморфная двуокись кремния и наиболее трудно — кристаллический кварц.
Окись магния (периклаз)
Окись магния выпускают двух марок: ЧДН и Ч по ГОСТ 4526—43. Это один из самых распространенных высокоогнеупорных окислов, который не подвержен кристаллическим модификационным превращениям. Существует только одна модификация окиси магния, называемая периклазом. Раньше предполагалось, что окись магния может существовать в виде двух кристаллических модификаций, отличающихся большой и малой плотностью, однако, как показали рентгеноструктурные исследовании, окись магния в кристаллографическом отношении остается без изменений.
В настоящее время многими исследованиями доказано, что изменение в свойствах обусловливается только различием в размерах кристаллов. Окись магния, обожженная при низких и высоких температурах, независимо от того, получена ли она при обжиге карбоната или гидроокиси, имеет простую кубическую структуру. Даже пары окиси магния при рассмотрении их в электронном микроскопе с увеличением в 50000 раз имеют кубическую структуру.
Периклаз с кубической решеткой можно получить как при химическом осаждении, так и при сплавлении. Строение кристаллической решетки MgO представлено на рис. 17, где черные кружочки изображают атомы магния, а белые — кислорода.
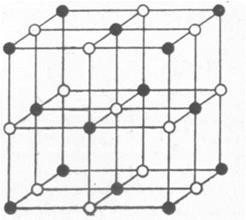
Рис. 17. Строение кристаллической решетки окиси магния
Изучение структуры периклаза позволяет установить плотность материала, определяемую из уравнения
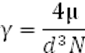
где γ— плотность, г/см3;
μ— молекулярная масса, г;
N— число Авагадро;
d—длина ребра элементарного куба (для периклаза d = 4,20Å).
По этой формуле плотность периклаза равняется 3,59 г/см3. Проведенные эксперименты [19] по взвешиванию в сухом виде и при погружении в воду кристалла периклаза, (рис. 17) показали значение γ =3,583 г/см3, Что подтверждает расчетную величину.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.