












Лекция 2. Межмолекулярные силы в жидкостях и их физико-химические свойства.
Сравнив плотности вещества в твердом, жидком и газообразном состояниях, можно судить о расстояниях между молекулами в этих веществах. При этом оказывается, что расстояния между молекулами в жидком и твердом состояниях мало отличаются — всего лишь на несколько процентов, а в газах расстояние между ними (при не очень больших давлениях) примерно в 10 раз больше. Поэтому говорят, что в жидком и твердом состояниях частицы вещества плотно упакованы. Плотная упаковка частиц приводит к тому, что жидкости и твердые тела сжимаются значительно слабее, нежели газы.
Пусть тело подвергается всестороннему сжатию или растяжению. В результате этого изменится его объем и, как следствие, его плотность. Обозначим через ε относительное изменение объема:
ε=DV/V =-Δρ/ρ; (1)
знак минус в этой формуле объясняется тем, что при возрастании объема тела его плотность при неизменной массе уменьшается. Избыточное по сравнению с атмосферным давление σ иногда называется напряжением:
σ=Δp. (2)
Сжимаемостью вещества β называется частное от деления относительного изменения объема на напряжение:
β =ε /σ =DV/ Δp V =--Δρ/ρ Δp
Обратная величина называется модулем объемного сжатия:
K=1/β. (4)
Из анализа данных о сжимаемости жидкостей и твердых тел, а также из анализа ряда других явлений, (прилипание друг к другу хорошо отшлифованных твердых тел, смачивание твердых тел жидкостями и т. п.), вытекает, что между молекулами действуют значительные по величине силы, называемые молекулярными силами. Эти силы обладают рядом интересных особенностей.
При удалении молекул друг от друга межмолекулярное взаимодействие проявляется в виде сил притяжения, при сближении на расстояния порядка линейных размеров самих молекул — в виде сил отталкивания. Следовательно, существует определенное расстояние dмежду молекулами, когда силы отталкивания и притяжения уравновешены и их равнодействующая равна нулю. Система молекул, расположенных на расстояниях dдруг от друга, находится в состоянии устойчивого равновесия, а энергия взаимодействия между молекулами в этом случае должна быть минимальной.
Молекулярные силы проявляются только в том случае, когда расстояния между молекулами весьма малы, порядка эффективных размеров самих молекул. При увеличении расстояния между ними в несколько раз силы становятся практически равными нулю.
Именно
этим объясняется тот факт, что при анализе явлений
в газах, где расстояния между молекулами примерно в 10 раз
больше, чем в жидкостях или твердых телах, можно в большинстве
случаев пренебречь действием молекулярных сил.
Величина молекулярных сил не зависит от общего числа молекул. Так, плотность или упругие свойства жидкостей и твердых тел, не зависят от размеров исследуемого образца; капля воды и вода в океане при одинаковой температуре и одинаковом внешнем давлении носят совершенно одинаковую плотность и сжимаемость. Этим молекулярные силы принципиально отличаются от гравитационных или кулоновских сил, где равнодействующая определяется действием всех тел, входящих в систему. Причина того, что молекулярные: силы действуют только между соседними молекулами, будет выяснена в следующих параграфах.
Тщательные исследования,· проведенные рядом ученых в первой половине XX века позволили: прийти к выведу, что молекулярные силы носят электрическое происхождение.
 |
Рис..1.
 взаимодействие
характерно только для заряженных тел. Однако известно, что электрическое взаимодействие возникает и между диполями — нейтральными частицами с
несимметрично расположенными
зарядами, равными, по величине, но противоположными по знаку. Это позволяет понять природу электрического взаимодействия между молекулами.
взаимодействие
характерно только для заряженных тел. Однако известно, что электрическое взаимодействие возникает и между диполями — нейтральными частицами с
несимметрично расположенными
зарядами, равными, по величине, но противоположными по знаку. Это позволяет понять природу электрического взаимодействия между молекулами.
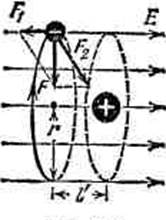
Молекулы ряда веществ имеют симметричное строение, как это схематически показано на рис.1. Здесь сфера, имеющая положительный заряд, изображает ядра атомов, входящих в молекулу, а отрицательно заряженная сфера — электронное облако этих атомов. Допустим, что молекула деформировалась так, как это изображено на рис.2. Такую деформированную молекулу можно в первом приближении рассматривать как нейтральную с некоторым моментом pе=ql. В этом случае молекула создает вне себя электрическое поле, напряженность которого равна электрическому полю диполя:
E =pe/ e0 r3
Поле этой молекулы вызовет деформацию близлежащих молекул. На положительное ядро молекулы действует сила отталкивания, направленная вдоль вектора напряженности, а на отрицательно заряженное электронное облако — силы, направленные в противоположную сторону. Эти силы и деформируют молекулу. Итак, молекула, имеющая дипольный момент ре, индуцирует (наводит) у соседних молекул дипольный момент р'е.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.