Изменения ![]() реакций
окисления различных сульфидов, кал/моль.
реакций
окисления различных сульфидов, кал/моль.
|
Номер реакции |
|
|||||
|
800 |
900 |
1000 |
1100 |
1200 |
1300 |
|
|
1.4 1.5 1.6 1.7 |
-89060 -107430 -66000 -94130 |
-88250 -104210 -63400 -91280 |
-86430 -100990 -60810 -88420 |
-84620 -97770 -58210 -75000 |
-82810 -94550 -55610 -82710 |
-81000 -91330 -53020 -79850 |
При одинаковых исходных условиях (концентрация и
температура) в первую очередь будет окисляться сульфид железа, затем цинка и,
наконец, меди. Такой порядок окисления справедлив для отдельных сульфидов. При
совместном их окислении возможно изменение указанного порядка в связи с
различной концентрацией сульфидов в концентрате. Соотношение между сульфидом
железа и сульфидами других металлов в перерабатываемом материале, при котором
будет возможно их одновременное окисление, можно определить, исходя из
равенства изменения энергии Гиббса реакции (1.4) окисления сульфида железа ![]() и реакций (1.6), (1.7) окисления сульфидов
и реакций (1.6), (1.7) окисления сульфидов
![]() меди и цинка:
меди и цинка: ![]() .
.
При взвешенной плавке окисление сульфидных частиц
совмещено с их расплавлением, поэтому изменения ![]() реакций
окисления могут быть определены с учетом активностей реагирующих веществ.
Приравнивая изменения энергии Гиббса реакций окисления
реакций
окисления могут быть определены с учетом активностей реагирующих веществ.
Приравнивая изменения энергии Гиббса реакций окисления ![]() и
и
![]() , получим:
, получим:
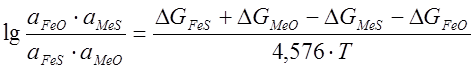 .
.
Учитывая ограниченную растворимость оксидов в сульфидах, можно принять активности оксидов равными единице, в этом случае получим:
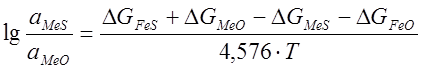 .
.
Если принять коэффициенты
активности сульфидов металлов в расплаве равными единице, то из уравнения можно
рассчитать соотношение концентраций сульфидов металлов и сульфида железа в
шихте, при котором будет происходить их одновременное окисление. Результаты
расчетов по этим уравнениям в интервале температур 800 – 1300![]() приведены
в табл. 2.
приведены
в табл. 2.
 |
Таблица 2
Соотношение концентраций ![]() в шихте для одновременного окисления сульфидов,
% (мол.)
в шихте для одновременного окисления сульфидов,
% (мол.)
|
Температура, |
|
|
|
800 900 1000 1100 1200 1300 |
7,94·104:1 4,27·104:1 2,53·104:1 1,61·104:1 1,09·104:1 7,79·103:1 |
13,3:86,6 22,1:77,9 31,8:68,2 41,4:57,6 51,4:48,6 59,5:40,5 |
Из данных табл. 2. следует, что для медных
концентратов порядок окисления сульфидов сохраняется и при совместном
окислении: сульфид железа, затем сульфиды цинка и меди. Для одновременного
окисления сульфида железа и, например, сульфида цинка при 1200![]() необходимо, чтобы содержание последнего в
концентрате было равно содержанию первого, что нереально для медного
концентрата. При полидисперсности концентратов и высокой скорости окисления
возможно, конечно, полное окисление сульфидов всех металлов, входящих в состав
тонкодисперсной частицы, но главным горючим составляющим концентратов при
взвешенной плавке является сульфид железа.
необходимо, чтобы содержание последнего в
концентрате было равно содержанию первого, что нереально для медного
концентрата. При полидисперсности концентратов и высокой скорости окисления
возможно, конечно, полное окисление сульфидов всех металлов, входящих в состав
тонкодисперсной частицы, но главным горючим составляющим концентратов при
взвешенной плавке является сульфид железа.
Сульфид железа может окисляться до закиси железа и магнетита. Небольшое количество шлакообразующих оксидов в медных сульфидных концентратах и несовершенство контакта сульфидных частиц с частицами флюса определяют преимущественное окисление сульфида железа до магнетита. На это указывают большее изменение энергии Гиббса (см. табл. 1) и больший тепловой эффект реакции окисления сульфида до магнетита, чем до закиси железа. Образование магнетита при взвешенной плавке зависит от состава концентратов и степени десульфуризации. Чем беднее концентрат по меди и богаче по железу, тем выше степень десульфуризации для получения штейна заданного состава и тем больше развито образование магнетита. Количество магнетита в жидких продуктах плавки определяется развитостью процесса восстановления его сульфидами, зависящего от состава расплавов, газовой фазы и температуры.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.