При расчете теплового баланса необходимо вычислить тепло, приносимое в печь исходными материалами и образующимися при протекании экзотермических реакций, а также тепло, выносимое из печи конечными материалами, уносимое газовой фазой, шлаком и штейном, а также поглощаемое эндотермическими реакциями.
Тепловые эффекты реакций рассчитываются как разность сумм произведений тепловых эффектов образования конечных продуктов реакции на их количество (число молей) и произведений тепловых эффектов образования начальных продуктов реакции на их количество. Тепловые эффекты образования химических веществ при заданной температуре рассчитываются по формуле:
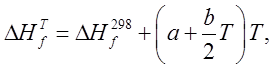
где ![]() -
тепловые эффекты образования химических веществ при температуре 298 К,
-
тепловые эффекты образования химических веществ при температуре 298 К, ![]() ;
;![]() – термодинамические
коэффициенты мольной теплоемкости,
– термодинамические
коэффициенты мольной теплоемкости, ![]() ;
; ![]() – абсолютная температура,
– абсолютная температура, ![]() .
.
Чтобы рассчитать тепловой эффект
реакции, в которой участвуют определенные массы реагентов, необходимо умножить
величину ![]() на коэффициент
на коэффициент 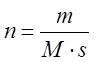 , где
, где ![]() – масса одного из веществ, участвующих в
химической реакции,
– масса одного из веществ, участвующих в
химической реакции, ![]() ;
; ![]() –
молярная масса этого вещества,
–
молярная масса этого вещества, ![]() ;
; ![]() – стехиометрический коэффициент вещества в
уравнении химической реакции.
– стехиометрический коэффициент вещества в
уравнении химической реакции.
Принимаем, что химические реакции,
протекающие в процессе плавки во взвешенном состоянии идут при температуре 1600![]() (1873
(1873![]() ).
Величины
).
Величины ![]() ,
, ![]() ,
, ![]() для каждого соединения находятся по
химическому справочнику термодинамических величин [3].
для каждого соединения находятся по
химическому справочнику термодинамических величин [3].
1.![]() .
.
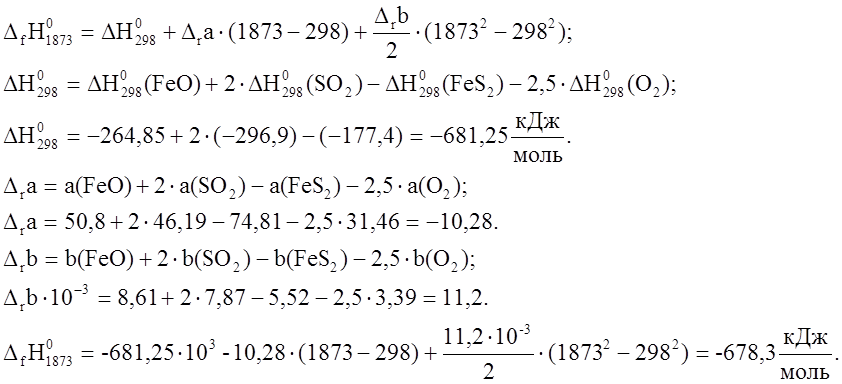 Это тепло выделится при
образовании 1 моля
Это тепло выделится при
образовании 1 моля ![]() . В результате этой реакции
образовалось 0,4
. В результате этой реакции
образовалось 0,4 ![]() .
.
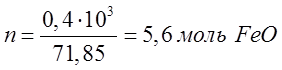 .
.
Таким образом, количество тепла выделившегося в ходе реакции будет:
![]()
![]() .
.
2.![]() .
.
1. 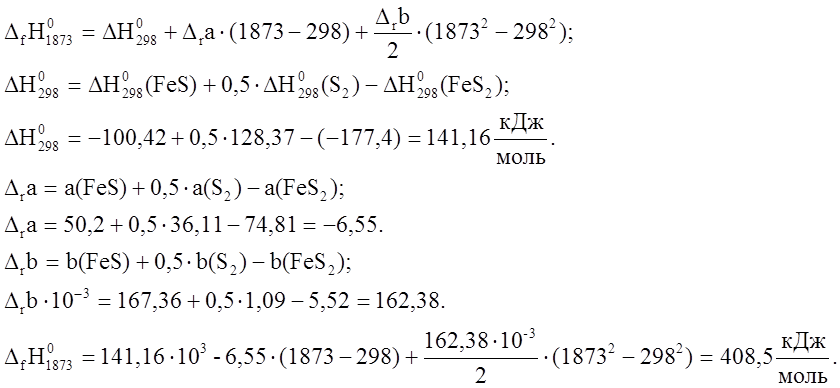
2.
Такое
количество тепла потребуется для вступления в реакцию 1 моля ![]() . В реакцию вступило 2,8
. В реакцию вступило 2,8 ![]() .
.
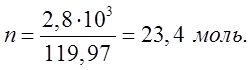
![]()
![]() .
.
3. ![]() .
.
Т.к. в справочнике не представлено
никаких данных о ![]() заменяем их значениями для
заменяем их значениями для ![]() .
.
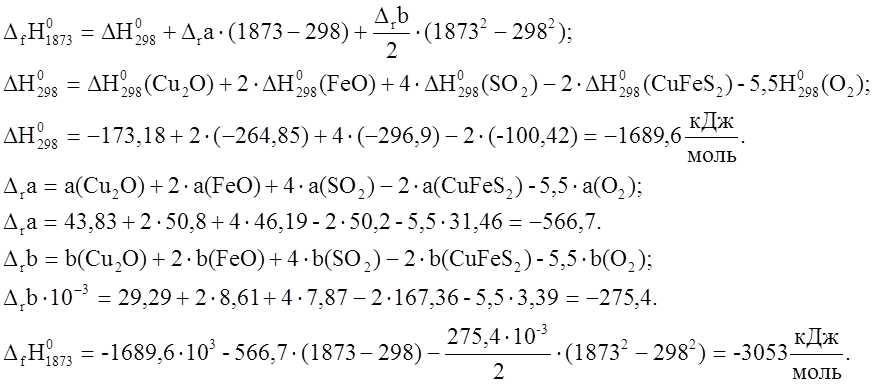 Такое количество тепла выделится при
образовании 1 моля
Такое количество тепла выделится при
образовании 1 моля ![]() . В результате реакции выделилось
17,65
. В результате реакции выделилось
17,65 ![]()
![]() .
.
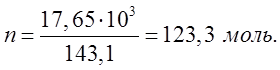
3. ![]()
![]() .
.
4. ![]() .
.
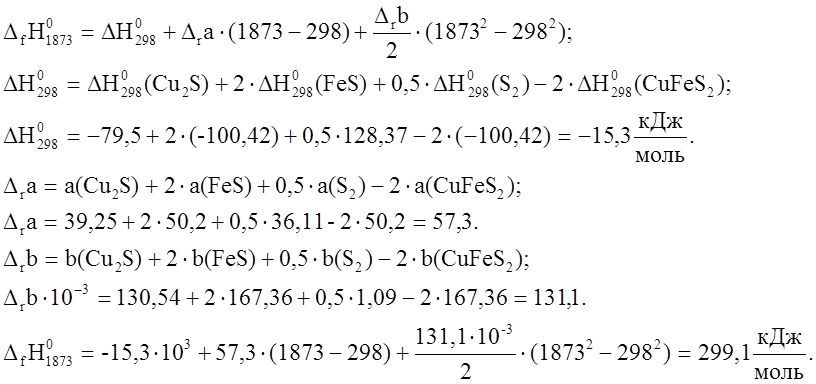
4. Такое количество тепла
потребуется для вступления в реакцию 2 молей ![]() . В
реакцию вступило 26,9
. В
реакцию вступило 26,9 ![]() .
.
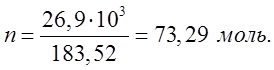
![]()
![]()
5. ![]() .
.
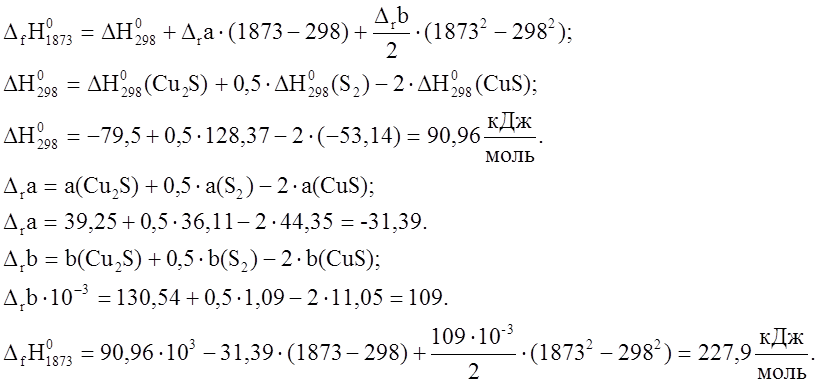 Такое количество тепла
потребуется для вступления в реакцию 2 моля
Такое количество тепла
потребуется для вступления в реакцию 2 моля ![]() . В
реакцию вступило 9,033
. В
реакцию вступило 9,033 ![]() .
.
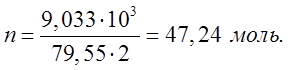
![]()
![]() .
.
6. ![]() .
.
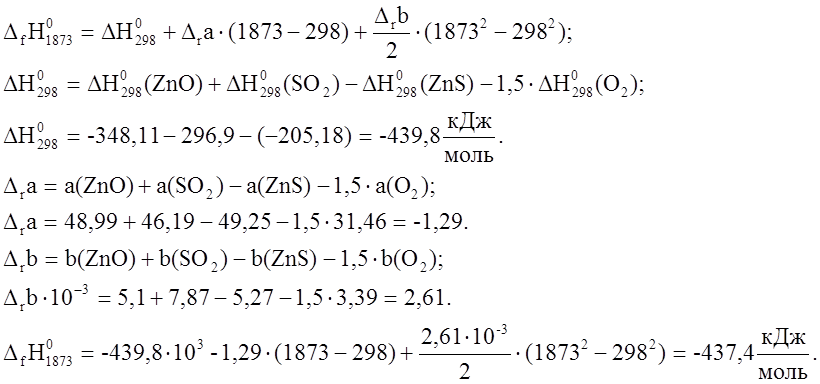 Такое количество тепла
выделится при образовании 1 моля
Такое количество тепла
выделится при образовании 1 моля ![]() . В результате реакции
образовалось 13,42
. В результате реакции
образовалось 13,42 ![]() .
.
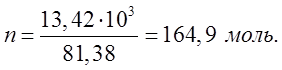
![]()
![]() .
.
7. ![]()
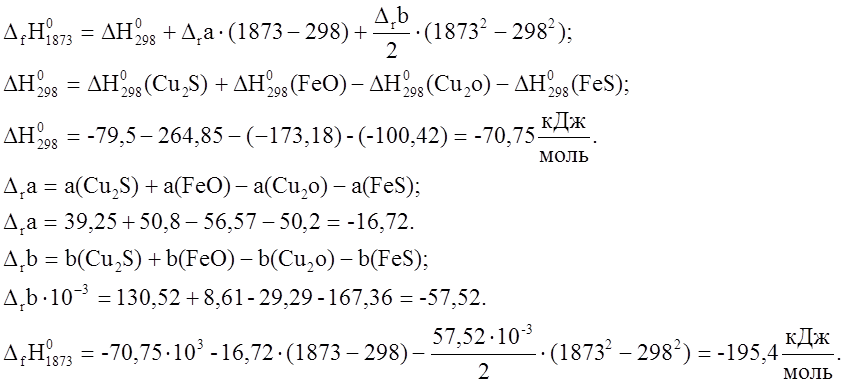 Это количество тепла выделится при образовании 1 моля
Это количество тепла выделится при образовании 1 моля ![]() .
В результате реакции образовалось 19,6
.
В результате реакции образовалось 19,6 ![]() .
.
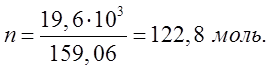
![]()
![]() .
.
8. ![]() .
.
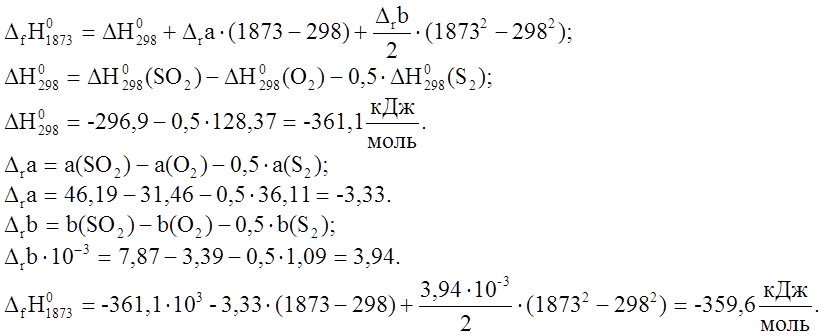 Такое количество тепла
выделится при окислении 0,5 моля
Такое количество тепла
выделится при окислении 0,5 моля ![]() . В реакцию вступило
23,81
. В реакцию вступило
23,81 ![]() .
.
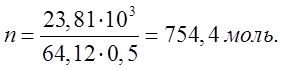
![]()
![]() .
.
9. ![]() .
.
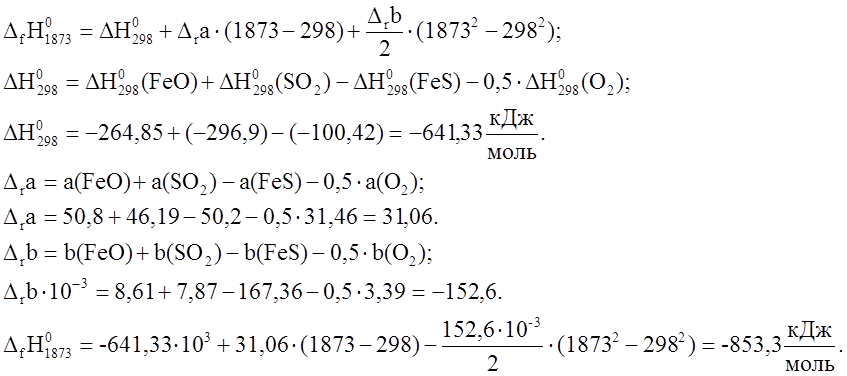 Это количество тепла выделится при
образовании 1 моля
Это количество тепла выделится при
образовании 1 моля ![]() . В результате этой реакции
образуется 7,47
. В результате этой реакции
образуется 7,47 ![]() .
.
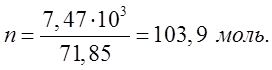
![]()
![]() .
.
10. ![]()
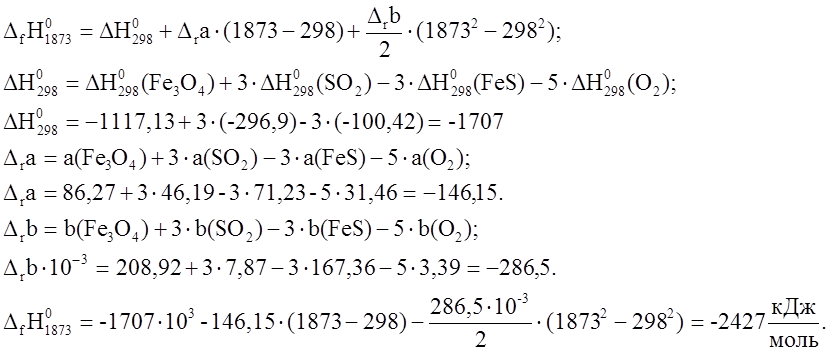 Тепло выделяется при
образовании 1 моля магнетита. В результате реакции образовалось 4,33
Тепло выделяется при
образовании 1 моля магнетита. В результате реакции образовалось 4,33 ![]() магнетита.
магнетита.
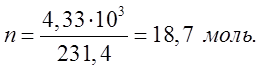
![]()
![]() .
.
Суммарный тепловой эффект от протекания данных реакций:
![]() =-3799,5+9555,6-376558+21920,7-23996-171282-88714,7-45414,5=-678290
=-3799,5+9555,6-376558+21920,7-23996-171282-88714,7-45414,5=-678290
![]() .
.
В результате проведённых расчётов по материальному балансу подтвердилась возможность проведения плавки во взвешенном состоянии в автогенном режиме. Выход основных продуктов составил: штейна – 31,62%, шлака – 32,72%. При этом штейн очень богат медью – содержание меди в штейне 50%.
Расчёты теплового баланса потвердели, что выбранная высокая степень десульфуризации (72%) так же позволила провести плавку в автогенном режиме.
Помимо этого, применение дутья, обогащенного кислородом,
обеспечило получение газов с высоким содержанием ![]() (81,47%).
А это играет немаловажную роль с экономической точки зрения, т. е. уменьшает
затраты на дальнейшую переработку на элементарную серу и серную кислоту.
(81,47%).
А это играет немаловажную роль с экономической точки зрения, т. е. уменьшает
затраты на дальнейшую переработку на элементарную серу и серную кислоту.
[1] Ю.П. Купряков. Автогенная плавка медных концентратов во взвешенном состоянии, М., Металлургия, 1979.
[2] Л.А. Синев, В.Ф. Борбат. Плавка сульфидных концентратов во взвешенном состоянии, М., Металлургия, 1979.
[3] Н.В. Гудима, Я.П. Шейн. Краткий справочник по металлургии цветных металлов, М., Металлургия, 1975.
[4] Н.Е. Бобин, Ю.А. Эист, В.Р. Лангнер и др. Л., 1987.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.