Токсикологические характеристики глиоксаля не установлены. Разнообразное промышленное применение глиоксаля вызвано повышенной реакционной способностью его молекулы и способностью образовывать макромолекулы сетчатой структуры. Текстильная промышленность использует это свойство глиоксаля для придания целлюлозным и смесовым тканям несминаемости, повышения их износостойкости. Бисульфитный продукт глиоксаля служит для выравнивания температур при крашении полиамидов кислотными красителями и целлюлозных волокон смешанными красителями.
Бумажная, фотографическая, табачная отрасли промышленности также используют глиоксаль как сшивающий агент полимерных материалов и целлюлозы на стадии образования бумажного листа и для улучшения его водостойкости. Он находит применение при изготовлении офсетной бумаги, обоев, вступая в реакцию с такими веществами, как крахмал, поливиниловый спирт, целлюлоза, полиакриламид.
Водостойкость адгезивов на основе полиакрилатов и винилацетата повышается при взаимодействии их молекул с глиоксалем. Композиции глиоксаля с Na2SiO3 используют для замедления отверждения цемента, гипса, литьевых форм, а также для закрепления почвы при земельных работах.
Очень важные перспективы применения глиоксаля открываются в фармацевтической промышленности. Широкий спектр производных глиоксаля представлен сульфаниламидными, противотуберкулезными и бактерицидными препаратами.
1 ЛИТЕРАТУРНЫЙ ОБЗОР
1.1 Общие сведения о глиоксале
Глиоксаль (этандиал, диформиль, щавелевый альдегид) — простейший диальдегид.
Несмотря на простое строение и химический состав глиоксаля, встречающиеся модификации этого соединения отличаются большим многообразием, обусловленным, прежде всего, высокой реакционной способностью его молекулы. Глиоксаль взаимодействует с представителями большинства классов органических соединений.
Глиоксаль может существовать в одном из трех физических состояний: твердом, жидком или газообразном. Мономерный глиоксаль с температурой плавления 15 оС имеет формулу:
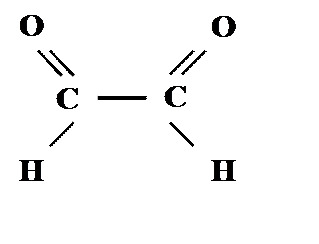
и при температурах ниже температуры плавления представляет собой желтые призматические кристаллы с запахом формальдегида.
Желтый цвет обусловлен наличием в молекуле двух карбонильных высокосопряженных групп —С=О и характерен для всех карбонильных соединений с подобным строением.
При соприкосновении с охлажденной поверхностью или в присутствии даже незначительных следов влаги расплавленный глиоксаль образует твердый белый тример. Превращение, очевидно, представляет собой сочетание фазового перехода с химической реакцией:
3(С2Н2О2)ж → (С2Н2О2)3 тв(1.1)
При температуре 20 °С глиоксаль — это жидкость зеленого цвета (d20, — 1,14 г/см; nD20 = 1,3826; молекулярная масса М = 58,04; Т ш = 50,4 оС при атмосферном давлении).
Теплота образования глиоксаля составляет ∆fHоgas = —212.0 ± 0.79 кДж/моль. Зависимость удельной теплоемкости глиоксаля (Сp.gas при постоянном давлении) от температуры приведена в таблице 1.1 [1]:
Таблица 1.1 – Удельная теплоемкость глиоксаля
|
Температура, К Cp gas,Дж/моль·К |
50 36.36 |
100 41.42 |
150 45.95 |
200 50.49 |
273.15 57.63 |
|
Температура, К Cp gas,Дж/моль·К |
298.15 60.23 |
300 60.43 |
400 71.21 |
500 81.43 |
600 90.12 |
|
Температура, К Cp gas,Дж/моль·К |
700 97.05 |
800 102.44 |
900 106.61 |
1000 109.86 |
1100 112.44 |
|
Температура, К Cp gas,Дж/моль·К |
1200 114.52 |
1300 116.22 |
1400 117.63 |
1500 118.8 |
Свойства глиоксаля, как товарного продукта, зависят от того, в какой сфере промышленного производства он используется. В мировом промышленном производстве глиоксаль выпускается в основном либо в виде 40%-ного водного раствора (таблица 1.2) [1], либо в поликристаллическом виде (полиглиоксаль).
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.