Используя реакцию нуклеофильного замещения, можно получать из галогеналканов не только спирты, но и другие классы органических соединений (нитрилы, амины, нитросоединения). Во всех этих реакциях в молекулу нового соединения вводится алкил, поэтому галогенпроизводные являются алкилирующими реагентами.
2.Реакции β-элиминирования (Е1 и Е2).
Отщепление галогеноводородов
Галогенопроизводные способны также отщеплять галогеноводороды с образованием олефинов. Отщепление происходит под действием на галогеналканы спиртовых растворов щелочей:
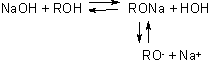

Элиминирование происходит по ионным механизмам Е1 и Е2.
Реакции, протекающие по Е1 – механизму, не требуют каких – либо реагентов, но необходим ионизирующий растворитель. Стадией определяющей скорость реакции, является образование интермедиата – карбкатиона, который переходит в стабильное состояние (олефин), отщепляя протон под действием появляющегося в реакционной смеси более основного алкоксил – иона (RO-).
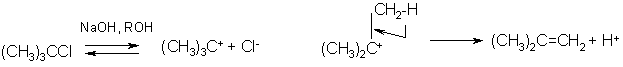
эта стадия протекает быстро
Реакции отщепления Е1 обычно сопровождаются процессами замещения SN1.
Разветвленность алкильной группы способствует увеличению выхода олефина.
Реакции отщепления, протекающие по бимолекулярному механизму Е2, требуют присутствия основания. Отрыв протона и потеря галогена происходят одновременно (без промежуточного соединения), через переходное состояние, в котором нуклеофил образует связь с протоном в той мере, в какой происходит отщепление галогена:
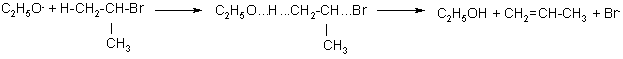
изопропилбромид переходное состояние
Скорость Е2 реакции пропорциональна концентрации обоих реагентов. Обычно на ряду с отщеплением происходит и нуклеофильное замещение по механизму SN2. Для первичных алкилгалогенидов преобладают реакции замещения, а для третичных – реакции элиминирования, причем в продуктах реакции всегда содержатся более замещенные алкены, энергетически более выгодные (правило Зайцева).
Активность оснований в реакциях, протекающих по механизму Е2, изменяется в том же направлении, что и их сила:
-NH2>C2H5O->-OH>CH3COO-
При обоих механизмах скорость отщепления Н – Х убывает в ряду: третичные > вторичные > первичные и I >Br > Cl.
Кроме указанных реакций нуклеофильного замещения (SN1 и SN2.) и β – элиминирования (Е1 и Е2) для галогенопроизводных характерны и другие превращения.]
3. Замещение атомов галогена водородом.
Это происходит при каталитическом гидрировании галогенопроизводных или действии на них водородом в момент выделения, а также иодоводородом:
H2,
катализатор
RI → RH + HI
C2H5I + HI → C2H6 + I2
4. Взаимодействие с солями галогеноводородной кислоты.
При этом если заменяют хлор бромом или иодом, то следует вести реакцию с солями щелочных металлов, хлориды которых труднее растворимы, чем бромиды и йодиды. При замещении галогена с большей атомной массой галогеном с меньшей массой необходимо применять соли серебра, т.к. иодид серебра менее растворим, чем бромид и особенно хлорид:
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.