Теория кристаллического поля рассматривает примесный ион как свободный ион, помещенный в электростатическое поле окружающего его кристалла. При этом считается, что величина и симметрия поля определяется ближайшими ионами другой полярности, которые называются лигандами. В этом приближении считается, что электронные орбитали примесного иона и лигандов не перекрываются. Т.е. роль лигандов заключается только в создании постоянного во времени электрического потенциала. Симметрия потенциала в позиции примесного иона целиком определяется расположением вокруг него лигандов – координационным числом (к.ч.) примесного иона. Основным эффектом влияния кристаллического поля на состояние свободного иона является штарковское расщепление его энергетических уровней. Центральной задачей в теории кристаллического поля является определение характера этого расщепления. Качественно она решается с помощью теории групп на основе классификации спектральных термов иона по неприводимым представлениям группы симметрии центра, в котором находится примесный ион. Решение этой задачи дает число расщепленных уровней. Величина же расщепления и энергетическое положение уровней в запрещенной зоне кристалла находятся полуэмпирически из сравнения результатов теоретического анализа с экспериментом. Такой подход оказался плодотворным при интерпретации структуры оптических спектров примесных ионов особенно переходных d и f-элементов. Характерной особенностью этих элементов является пространственная экранировка внутренних электронов, находящихся в частично заполненных d и f-оболочках, электронами из внешних s и p-оболочек. Из-за этой экранировки волновые функции (орбитали) внутренних d и f-электронов почти не перекрываются с волновыми функциями лигандов. Поэтому квантовые переходы внутри этих оболочек (d«d, f«f) с хорошей точностью можно рассматривать как переходы внутри самого примесного иона, возмущенного электростатическим полем лигандов.
Энергетические уровни свободного иона являются 2L+1-кратно вырожденными по квантовому числу ML. Это связано со сферической симметрией поля свободного иона. При введении иона в кристалл симметрия внешнего поля изменяется. Вследствие этого частично снимается вырождение по квантовому числу ML и происходит штарковское расщепление уровней, зависящее от квадрата квантового числа ML. Полный гамильтониан примесного иона в кристалле записывается в виде
![]() . (1)
. (1)
Здесь Hnc – кулоновское взаимодействие электронов с ядром, Vee – электростатическое взаимодействие электронов друг с другом, Vso – спин-орбитальное взаимодействие и Vcr – потенциал, создаваемый лигандами, который можно рассматривать как возмущение. Влияние кристаллического поля зависит от соотношения между тремя последними членами уравнения (1). По этому соотношению кристаллическое поле принято делить на три типа:
Слабое
![]()
Среднее
![]() (2)
(2)
Сильное
![]() .
.
Случай слабого поля реализуется для ионов редкоземельных элементов и актинидов, у которых внутренние оптически активные электроны из не полностью заполненных 4f и 5d оболочек, соответственно, заэкранированы пятью или шестью электронами из внешних s, p и d оболочек. В частности, электронные конфигурации нейтральных атомов редкоземельных элементов (TR) имеет вид
![]() .
.
При вхождении атомов в кристалл экранирующие 5s25p6 полностью заполненные оболочки остаются неизменными и «защищают» от кристаллического поля глубже лежащие 4f –электроны. Химическая связь может обеспечиваться только внешними 6s2-электронами – в этом случае образуются двухзарядные ионы TR2+. Дополнительная химическая связь может обеспечиваться единственным 5d1 электроном, который имеется только у атомов Ce, Lu и Ga, при этом образуются трехзарядные ионы этих элементов. Трехзарядные ионы остальных редкоземельных элементов TR3 образуются в том случае, когда на дополнительную связь уходит один электрон из 4f-оболочки. Для некоторых ионов TR отмечаются четырех зарядовые состояния, когда из 4f-оболочки уходят на связь два электрона.
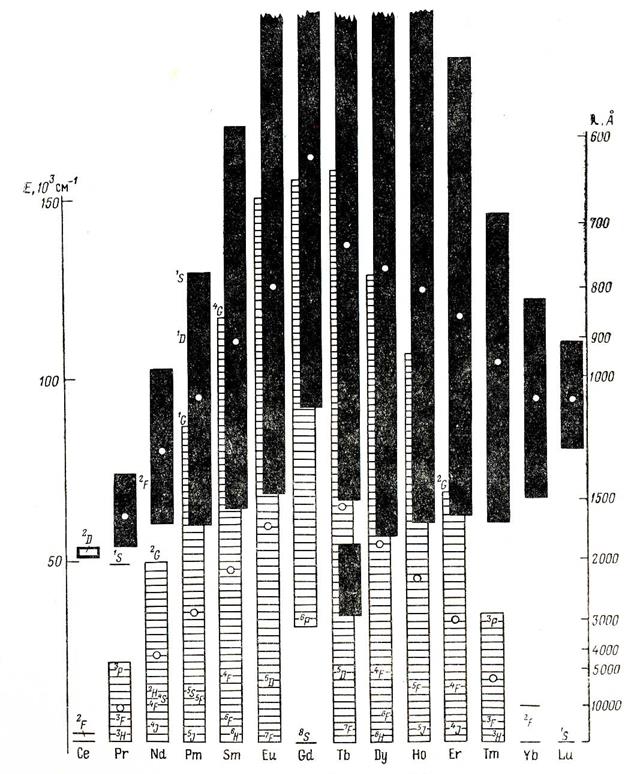
Рис.6. Схема расположения термов 4fk (белое) и 4fk-15d (черное) конфигураций для трехвалентных ионов TR3+
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.