глава IV. Кристаллизационные процессы формирования
отливок
При переходе сплава из жидкого состояния в твердое происходит формирование кристаллической структуры. Структуру сплава в отливках рассматривают на трех уровнях: макроскопическом, микроскопическом и субмикроскопическом. На макроуровне рассматривают размер и геометрические формы литого зерна – кристаллита, которые выявляются при травлении макрошлифа или на фрактографиях – изломах образцов или отливок. Размер и формы кристаллита оценивают невооруженным глазом или при небольшом увеличении (´24). На микроуровне изучению подвергают структурные составляющие и фазы сплава отливки, выявляемые под микроскопом на шлифах, подвергнутых шлифованию и полировке с последующим травлением кислотными или щелочными растворами. На субмикроскопическом уровне изучается кристаллическая решетка металла и ее дефекты под электронным микроскопом.
Для литейной технологии и оценки качества литого металла обычно ограничиваются двумя первыми уровнями: макро-уровнем, где оценивают геометрические формы и размеры кристаллитов; а также микроуровнями с целью анализа структурных составляющих и фаз в структуре сплава отливки.
|
|
|
Рис. 57. Изменение свободной энергии в зависимости от температуры для твердого (2) и жидкого (1) металла |
Процесс кристаллизации рассматривают с различных подходов и физических моделей. С позиции термодинамики температуру кристаллизации чистого металла оценивают на основе сопоставления величины изменения свободной энергии жидкой и твердой фаз. С ростом температуры свободная энергия и жидкого, и твердого металла снижается, но интенсивность снижения свободной энергии твердого металла меньше чем жидкого (рис. 57). Точка пересечения двух кривых соответствует температуре кристаллизации металла.
В термодинамической теории кристаллизации используют два понятия: 1) скорость возникновения центров кристаллизации или скорость зарождения – Vзар; 2) скорость роста зародившихся кристаллов – Vр. Соотношение этих двух скоростей определяет качественно величину формирующихся кристаллитов. Если Vзар > Vр, то формируется мелкозернистая структура (зарождаются кристаллиты быстрее, чем растут). При другом неравенстве скоростей Vр > Vзар образуется более крупнозернистая структура (кристаллиты растут быстрее, чем зарождаются новые).
Следующее понятие термодинамической теории кристаллизации – переохлаждение жидкого металла. Для того чтобы скорости зарождения и скорости роста отличались от нуля, температура расплава (Т) должна быть несколько ниже температуры кристаллизации:
![]() .
.
Здесь DТп – величина переохлаждения, необходимая для кристаллизации металла. От величины переохлаждения зависит формирующаяся структура, в частности скорость зарождения и скорость роста зерен. Увеличение скорости зарождения кристаллитов с возрастанием переохлаждения объясняют следующим обстоятельством. Строение жидких металлов представляется как квазитвердое, в котором имеются группы атомов с упорядоченным взаимным расположением, подобным кристаллической решетке твердого металла (кластеры, ячейки, сиботоксические группы, флуктуации …). По вероятностному закону с понижением температуры расплава размер таких групп возрастает, и некоторые из них могут достичь размеров кристаллического зародыша. Оценим величину кристаллического зародыша количественно в зависимости от величины переохлаждения.
Будем считать кристаллический зародыш сферической формы, и тогда величина изменения свободной энергии образования твердого кристаллита радиусом «r» выразится:
![]() , где Fжид – свободная
энергия жидкого металла; Fтв –
свободная энергия твердого металла.
, где Fжид – свободная
энергия жидкого металла; Fтв –
свободная энергия твердого металла.
По термодинамике
![]() , где DН – изменение
энтальпии; DS
– изменение энтропии.
, где DН – изменение
энтальпии; DS
– изменение энтропии.
Для равновесных условий DF = 0 (скорость кристаллизации равна скорости плавления кристаллитов) и тогда
![]() .
.
Отсюда выразим 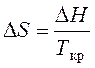 . Подставим величину DS в выражение
свободной энергии и получим:
. Подставим величину DS в выражение
свободной энергии и получим:
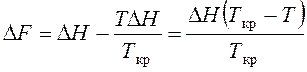 .
.
Для процесса кристаллизации величину изменения энтальпии можно принять равной удельной теплоте кристаллизации по абсолютной величине, но с обратным знаком, так как при выделении теплоты теплосодержание снижается:
![]() .
.
А разность ![]() представляет величину
переохлаждения.
представляет величину
переохлаждения.
Тогда 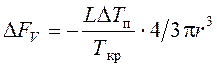 для сферического зародыша
кристаллита.
для сферического зародыша
кристаллита.
В термодинамике свободная энергия оценивается и как работа образования кристаллического зародыша, поэтому может быть представлена работой, затраченной на образование сферической поверхности:
![]() , где s – величина межфазного
натяжения на границе раздела металлический расплав – твердая фаза.
, где s – величина межфазного
натяжения на границе раздела металлический расплав – твердая фаза.
Изменение общей свободной энергии
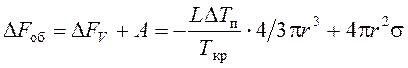 .
.
Проанализируем функцию ![]() на экстремум, взяв
первую производную по «r» и приравняв ее к нулю.
на экстремум, взяв
первую производную по «r» и приравняв ее к нулю.
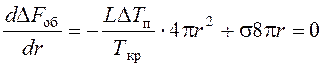 .
.
|
|
|
Рис. 58. Зависимость величины изменения свободной энергии от радиуса кристаллического зародыша |
Отсюда 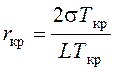 .
.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.