1.7. Основные положения жидкого состояния металлов
Отличительным свойством жидких металлов, как и всех жидкостей, является их способность приобретать форму того сосуда, в который они помещены. Именно на этом основано существо литейной технологии и возможность изготовления деталей и изделий сложнейшей геометрической конфигурации.
Если в твердом состоянии металлы и сплавы имеют четко выраженное кристаллическое строение, то при переходе в жидкое состояние кристаллическое строение нарушается. Однако сопоставление целого ряда свойств жидких и твердых металлов показывает на большую вероятность близости строения жидких металлов с твердыми. Так плотность, удельная теплоемкость, теплопроводность, электропроводность жидких металлов лишь незначительно отличаются от аналогичных свойств твердых металлов. В то же время у этих двух состояний металлов есть и существенные различия, относящиеся, прежде всего к реологическим свойствам. Так у жидких металлов реологические свойства радикально отличаются от твердых. Предельное напряжение сдвига, модуль сдвига жидких металлов имеют минимальные значения, близкие к нулю, а у твердых металлов эти величины составляют сотни мега-паскалей.
Таким образом, у твердых и жидких металлов следует ожидать как схожести, так и различий в их строении. Получила распространение гипотеза о наличии дальнего и ближнего порядка атомов в твердом состоянии и о сохранении в жидком состоянии только ближнего порядка атомов (исчезновение дальнего порядка атомов). В первом приближении чисто геометрически ближний и дальний порядок отвечает клеткам шахматной доски; а сохранение ближнего порядка при исчезновении дальнего отвечает расположению камней на булыжной мостовой. Каждый камень имеет четыре соседних, как и шахматная клетка соседствует с четырьмя другими клетками, но порядка в горизонтальном и вертикальном направлениям по линиям нет.
Для количественной оценки взаимного расположения атомов относительно
друг друга применяют ряд методик теоретического и экспериментального изучения
строения жидких металлов. В физике металлов сделаны попытки теоретического
расчета взаимного расположения атомов в жидких металлах. Для расплава металла
объемом V, состоящего из N-атомов,
определим фиксированное положение каждого атома в трехмерном пространстве: х1,
у1, z1; х2,
у2, z2, … хi, уi,
zi, … хN, уN,
zN. Заданный ряд положений атомов определяет
конфигурацию всей системы – R. Для любой
конфигурации R соответствует своя отображающая
точка, относительно которой определяются координаты всей системы, состоящей из N-атомов. Пространство, занимаемое отмеченными атомами,
называется конфигурационным. Расположение атомов в конфигурационном
пространстве, несомненно, обусловлено силовым межатомным взаимодействием.
Потенциальная энергия конфигурации обусловлена кулоновским взаимодействием
атомов. Если допустить, что потенциальная энергия складывается из парного
взаимодействия атомов, то полная потенциальная энергия конфигурации выразится 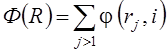 , где
, где ![]() –
потенциальная энергия изолированной пары атомов:
–
потенциальная энергия изолированной пары атомов: ![]() , а
, а ![]() .
.
В действительности же на потенциальную энергию системы оказывает влияние не только взаимодействие между двумя соседними атомами, но и действие третьего, четвертого и т.д. атома. Приближенно для типичных конфигураций атомов жидких металлов можно считать, что силы связи между атомами равны силам межатомной связи в кристаллической решетке.
Тогда все основные термодинамические свойства жидкого металла определим через статистическую функцию Z, зависящую от температуры и конфигурационного интеграла Q:
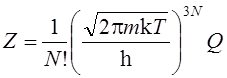 , где m – масса атома металла; k – постоянная Больцмана (
, где m – масса атома металла; k – постоянная Больцмана (![]() Дж/град);
h – постоянная Планки (
Дж/град);
h – постоянная Планки (![]() Дж×с).
Дж×с).
Конфигурационный интеграл ![]() ,где dR – элемент 3N-мерного
конфигурационного пространства.
,где dR – элемент 3N-мерного
конфигурационного пространства.
Свободная энергия системы при постоянном объеме определится: ![]() , а далее могут определены и другие термодинамические
величины.
, а далее могут определены и другие термодинамические
величины.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.