В технике металлы используются преимущественно не в чистом виде, а в виде сплавов. Сплав представляет собой многокомпонентный материал, содержащий кроме основного металла легирующие компоненты. Так сталь представляет сплав железа с углеродом, марганцем, кремнием и другими элементами. Сплавы алюминия содержат в своем составе Si, Mg и другие элементы в количестве до нескольких процентов по массе. Физико-механические и другие свойства сплавов определяются как основным металлом, так и легирующими элементами.
Свойства сплавов рассматриваются на так называемых диаграммах состояния, в которых свойства сплавов являются функцией состава. Для литейной технологии, а также в металловедении и металлургии рассматривается важное свойство – температура фазовых переходов, в том числе температура перехода из жидкого состояния в твердое и обратно (затвердевание – плавление).
Диаграммы зависимости температуры фазовых переходов от состава получили название фазовых диаграмм состояния сплавов. Лучше всего изучены двойные диаграммы состояния, представляющие собой плоское графическое изображение – для двух компонентов сплава.
Рассмотрим основные типы двойных фазовых диаграмм состояния металлических сплавов, наиболее типичные для литейных сплавов. Наиболее простой в графическом изображении является диаграмма состояния с неограниченной растворимостью в жидком и твердом состояниях. Примером такой двойной диаграммы служит сплав Ni-Cu (рис. 10). Жидкая фаза представляет жидкий раствор меди в никеле любой концентрации от 100 % Ni до 100 % Cu. Твердая фаза представляет b-твердый раствор замещения – атомы никеля и меди перемешаны друг с другом в узлах решетки ГЦК (рис. 11). На трех гранях куба атомы никеля замещены атомами меди. Естественно, что параметры кристаллической решетки претерпевают изменения и искажения, обусловленные различиями в геометрических размерах атомов Ni и Cu.
|
|
|
|
Рис. 10. Диаграмма сплава Ni-Cu |
Рис. 11. Кристаллическая решетка твердого раствора замещения |
Для изучения свойств сплавов типа твердых растворов очень важно глубокое понимание природы происходящих превращений. Рассмотрим основное фазовое превращение – переход из жидкого состояния в твердое и связанные с этим переходом соотношение фаз и изменение химического состава. Рассмотрим в увеличенном масштабе диаграмму состояния двух металлов А и Б, образующих неограниченный твердый раствор (рис. 12).
|
|
|
Рис. 12. Диаграмма состояния двух металлов, образующих неограниченный твердый раствор |
Рассмотрим сплав произвольного состава "Со" с более высоким процентным содержанием компонента "А".
Для этого сплава температура начала затвердевания – Тлик
– температура ликвидус; а конца затвердевания – Тсол –
температура солидус. При температуре Т1, меньшей температуры
ликвидус, но большей температуры солидус (внутри интервала затвердевания) в
сплаве одновременно присутствует и жидкая и твердая фаза. Химический состав
твердой фазы, выделяющейся при температуре Т1 соответствует
концентрации С1, а состав жидкой фазы соответствует концентрации
С2. Соотношение между относительными количествами твердой и
жидкой фаз определяется в соответствии с так называемым "правилом
рычага". При температуре Т1 относительная доля (по
массе) твердого сплава равна ![]() , а относительная доля
жидкого сплава соответственно
, а относительная доля
жидкого сплава соответственно ![]() . Это соотношение
несложно выводится из следующего логического анализа. При температуре Т1
обозначим массу жидкого сплава mL, а
массу твердого сплава mS. Тогда масса
элемента Б в жидком сплаве будет равна
. Это соотношение
несложно выводится из следующего логического анализа. При температуре Т1
обозначим массу жидкого сплава mL, а
массу твердого сплава mS. Тогда масса
элемента Б в жидком сплаве будет равна ![]() , а
масса этого элемента в твердом –
, а
масса этого элемента в твердом – ![]() . Составим уравнение
материального баланса по элементу Б:
. Составим уравнение
материального баланса по элементу Б:
![]() .
.
Проведем алгебраические преобразования:
![]()
и далее
![]() .
.
Представим массовые доли твердой и жидкой фаз в виде отношения:
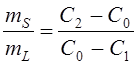
или по буквенным обозначениям отрезков ![]() ,
, ![]() . Тогда
. Тогда 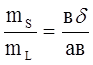 .
.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.