Экспериментальная часть.
1. Определение меланоидинов.
Реактивы:
10 г аминокислоты (глицин)
10 г глюкозы
100 мл этилового спирта
100 мл ацетона
100 мл диэтилового эфира
Оборудование и приборы:
Обратный холодильник, перегонная колба, цилиндр 100мл, аналитические весы, ФЭК, ступка, пестик, песочная баня, фильтр под вакуумом, мерная колба на 25 мл – 6 шт.
Метод состоит в предварительном получении «стандартной смеси меланоидинов» путем термической обработки смеси чистых аминокислот и глюкозы.
На 10 г аминокислоты (в перерасчете на сухое вещество) берем 10 г глюкозы и 60 мл дистиллированной воды. Смесь кипятим с холодильником на песочной бане в течение 10 часов. Нагревание должно проводиться осторожно во избежание образования нерастворимых форм меланоидинов.
После охлаждения желеобразную массу растираем в ступке и 10 – 20 минут взбалтываем с 5 – кратным количеством этилового спирта. Жидкую часть отсасываем на фильтре под вакуумом и производим 3 раза ее дегидратацию ацетоном. Затем полученный зернистый продукт(из жидкой части) обрабатываем диэтиловым эфиром. Эфир сливаем, следы органических растворителей удаляем под вакуумом. Получен продукт в виде темно – коричневого порошка. Количественно взвешиваем продукт на аналитических весах:
Фильтр с порошком – 0,27180 г
Фильтр (после взвешивания с порошком) – 0,13165 г
Полученная масса навески – 0,14015 г
Разводим полученную навеску в мерной колбе на 25 мл 5% раствором спирта.
Концентрация раствора – 0,005606 г/мл.
Готовим рабочий (стандартный) раствор – 5,0 мг/мл.
В мерную колбу на 25 мл вносим 22,30 мл раствора с концентрацией – 0,005606г/мл и доводим до метки 5% - м раствором спирта.
Полученный раствор используем для приготовления серии растворов необходимой концентрации и на спектрофотометре определяем их оптическую плотность при максимальной длине поглощения растворов.
Серия растворов.
|
№ раствора |
V стандартного раствора, мл |
Концентрация мг/мл |
Длина волны,λ |
Оптическая плотность,D |
|
холостая |
0 |
0 |
520 |
0 |
|
1 |
0,5 |
0,1 |
520 |
0,202 |
|
2 |
1,0 |
0,2 |
520 |
0,393 |
|
3 |
2,5 |
0,5 |
520 |
0,991 |
|
4 |
4 |
0,8 |
520 |
1,986 |
По данным измерений строим калибровочный график.
2.Определение окислительно – восстановительной способности пива.
Сущность метода заключается в измерении оптической плотности раствора по истечению 60 с после прибавления 2,6 – дихлорфенол – индофенола. Редуктоны восстанавливают его красные кислые или голубые щелочные растворы в бесцветные лейкосоединения:
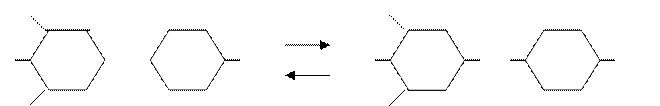
2,6 - дихлорфенол – индофенол 2,6 -дихлорфенол – индофенол
(натриевая соль) (лейкоформа)
Реактив имеет синюю окраску при рН 6,которая при рН 5,5 переходит в красную.
Приготовление реактивов
Определение концентрации готового раствора 2,6 – дихлорфенол – индофенола.
(С12НСl2NО2Nа).
Реактивы и оборудование:
50 мл 2 % раствора Н2SО4
КI несколько кристаллов
1 % раствор крахмала
КIО3 0,001 н раствор
Микробюретка
Цилиндр 50 мл
Пипетка Мора на 5 мл
Мерная колба 2 шт.
Ход определения:
1) В 50 мл 2 % - ного раствора серной кислоты растворяем несколько кристаллов аскорбиновой кислоты (1 – 1,5 мг). 5 мл раствора титруем из микробюретки раствором 2,6 - дихлорфенол – индофенола до появления розового окрашивания.
Результат титрования: 0,14; 0,13; 0,135
2) Снова берем той же пипеткой в другую колбу 5 мл раствора аскорбиновой кислоты, добавляем несколько кристаллов йодистого калия (КI), 2 – 3 капли 1% - ного раствора крахмала и титруем 0,001 н раствором иодноватокислого калия (КIО3) до появления голубого окрашивания.
Результата титрования: 0,019; 0,019.
Титр раствора 2,6 - дихлорфенол – индофенола Х вычисляем (при расчетах берем во внимание, что 1 мл 0,001 н раствора КIО3 эквивалентен 0,088 мг аскорбиновой кислоты) по формуле:
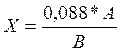
Где А – количество миллилитров 0,001 н раствора иодноватокислого калия, израсходованное на титрование раствора аскорбиновой кислоты; В - количество миллилитров раствора 2,6 - дихлорфенол – индофенола, пошедшее на титрование.
(0,088 * 0,019) / 0,135 = 0,0123 г/мл (титр)
0,0123 * 1000 = 12,385 г/л
12,385 г/л – концентрация готового раствора 2,6 - дихлорфенол – индофенола.
Ход определения
Для данного опыта используем два сорта пива:
Светлое:
1. Балтика № 3
2. Живое не фильтрованное
Темное:
1. Балтика №6 (портер)
2. Живое фильтрованное
Пиво перед анализом выдерживаем при 20о С. В пробирку вносим 10 мл дегазированного пива и с помощью микропипетки осторожно по краю пробирки приливаем 0,25 мл 12,385М раствора 2,6 - дихлорфенол – индофенола. Содержимое дважды энергично встряхиваем и включаем секундомер. По истечении 60 с смесью наполняем кювету на 1 см и определяем оптическую плотность раствора при длине волны 520 нм.
Параллельно проводим холостой опыт, внося в пробирку вместо пива 10 мл фосфатного буферного раствора. При исследовании пива рН буферного раствора должен быть 4,35 – 4,40.
Окислительно – восстановительную способность определяем по формуле:
![]()
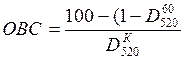
Где ![]() - оптическая плотность образца пива.
- оптическая плотность образца пива.
![]() - оптическая
плотность холостого раствора при соответствующем рН.
- оптическая
плотность холостого раствора при соответствующем рН.
|
Наименование образца |
Т, оС |
рН |
ЕН |
||
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.