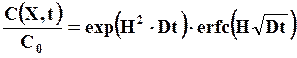 (7.20)
(7.20)


Рис. 7.5. Концентрационные кривые для полубесконечных образцов:
а – состояние образцов до нагрева; б – состояние образцов после нагрева;
с – кривая распределения концентрации диффузанта (t1 < t2 < t3).
Обратная задача – диффузия из среды с постоянной концентрацией в полуограниченное тело с нулевой концентрацией при граничных условиях (7.18). Решение представляет следующее выражение
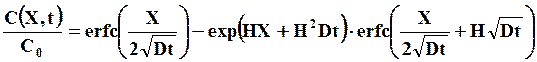 (7.21)
(7.21)
Количество вещества, прошедшее через единичную площадь поверхности за время t можно определить как
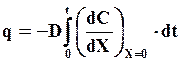 (7.22)
(7.22)
На основании решения уравнений диффузии можно построить диффузионную диаграмму процесса, позволяющую прогнозировать состав диффузионной зоны, выбирать режимы процесса диффузионного отжига и т.п. Типовая диффузионная диаграмма представлена на рис. 7.6.
В первом квадранте изображено распределение концентрации диффузанта в зависимости от относительной глубины. В третьем квадранте представлено семейство гиперболических кривых, отображающих активность диффузионного процесса через обратную величину диффузионного пробега. Характер представленных кривых определяется температурой и длительностью процесса, при этом с повышением температуры и длительностью процесса обратная величина диффузионного пробега уменьшается. Во втором квадранте приведено семейство лучей, определяющих расположение различных уровней в пределах относительной диффузионной ширины.
Диффузионные диаграммы применяются при решении следующих задач. На рис. 7.6. пунктирной линией показан алгоритм определения температуры и длительности диффузионного процесса при заданной концентрации диффундирующего элемента на определенном уровне относительно границы, через которую осуществляется диффузия. Возможно решение обратной задачи, когда требуется определить концентрацию диффундирующего элемента на определенной глубине при заданных условиях диффузионного процесса.
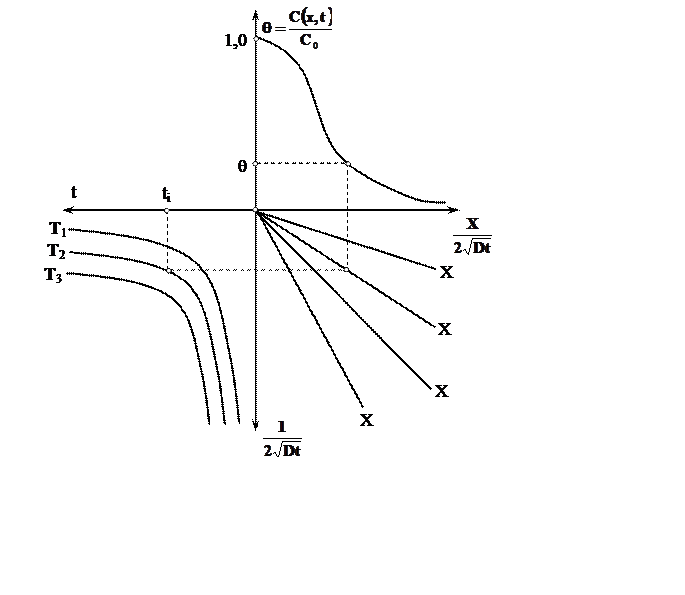
Рис. 7.6. Типовая диффузионная диаграмма
7.7. Роль диффузии в некоторых физико-химических процессах
Рассмотрим некоторые физико-химические процессы, в которых диффузия играет наиболее важную роль.
7.7.1 Диффузия как контролирующая гетерогенного процесса
Большинство процессов в конденсированных системах являются гетерогенными, т.е. происходят в различных фазах, отделенных друг от друга поверхностью раздела. К таким процессам в металлургии и материаловедении можно отнести:
- восстановление твердых оксидов газами или углеродом;
- распределение элементов между металлом и шлаком;
- растворение и выделение газов из металла и шлака;
- растворение твердых тел в жидкостях;
- превращения в металлах и сплавах, сопровождающиеся диффузионным переносом вещества;
- процессы химико-термической обработки;
- рекристаллизация и др.
Характерной особенностью гетерогенных процессов является их многостадийность, но обязательно включающих три основных последовательных этапа: диффузионный подвод вещества к границе раздела фаз, химическую реакцию или адсорбцию на границе раздела и отвод продуктов превращения, носящий, как правило, диффузионный характер. Суммарная скорость протекания гетерогенного процесса определяется скоростью самой медленной стадии, которая и является контролирующей. В большинстве случаев медленным является подвод вещества к поверхности и отвод продуктов реакции. Рассмотрим один из типичных примеров.
Пусть область x < 0 (от внешней области) осуществляет диффузионный подвод вещества к поверхности x = 0, на которой происходит химическая реакция первого порядка. Тогда при всех x < 0
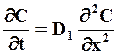 (7.23)
(7.23)
где D1 – коэффициент диффузии во внешней области.
Примем, что в слое толщиной Δ, прилегающей к поверхности х =0, установилось стационарное состояние, причем C(-Δ,t) = C0, а С(0,t) = C1. Тогда количество вещества, приходящего в единицу объема у поверхности х = 0 в единицу времени равно
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.