- кулоновское отталкивание электронных облаков присоединённых атомов;
- кулоновское и обменное отталкивание между связями типа О-Н;
- участие (2s)2-электронов кислорода в образовании связи (гибридизация), что приводит к упрочнению связи и увеличению валентного угла;
- некоторая вероятность других типов спаривания (кроме основного), приводящих к понижению энергию системы.
9.3. Приближение полного электронного спаривания.
После описания локализованных МО рассмотрим метод ВС в применении к многоатомным молекулам. Смысл локализации связи А-В в методе ВС заключается в том, что спаривание не зависит от других возможных спариваний в других частях молекулы. Как было установлено ранее для двухатомных молекул с одинаковыми ядрами значения энергии, соответствующие симметричной и антисимметричной волновым функциям, таковы:
Е± = 2Е0
+ 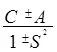 .
(9.1)
.
(9.1)
Если молекула состоит из разных атомов, то 2ЕО = ЕА + ЕВ. Пренебрегая интегралами S (он обычно мал) и С (для большинства молекул С » 0.15А, где А - обменный интеграл), получим:
Е± = 2Е0 ± А. (9.2)
Энергия
системы Е+ соответствует синглету, а Е- – триплету. Как указывалось ранее, синглету
соответствует одна симметричная орбитальная волновая функция ![]() , умноженная на антисимметричную спиновую
волновую функцию
, умноженная на антисимметричную спиновую
волновую функцию ![]() , а триплету три полных волновых
функций, получаемых перемножением антисимметричной орбитальной волновой функции
, а триплету три полных волновых
функций, получаемых перемножением антисимметричной орбитальной волновой функции
![]() на три типа симметричных спиновых волновых
функций (a(1)a(2); a(1)b(2) + a(2)b(1); b(1)b(2)). Если спины принимают
ориентацию совершенно случайно, то любая из указанных возможностей
равновероятна. Следовательно, из 4 способов корреляции
на три типа симметричных спиновых волновых
функций (a(1)a(2); a(1)b(2) + a(2)b(1); b(1)b(2)). Если спины принимают
ориентацию совершенно случайно, то любая из указанных возможностей
равновероятна. Следовательно, из 4 способов корреляции ![]() 3
приводят к антипараллельному, а 1 к параллельному расположению спинов. Поэтому
средняя энергия взаимодействия
3
приводят к антипараллельному, а 1 к параллельному расположению спинов. Поэтому
средняя энергия взаимодействия
(+ А/4) + (- 3A/4) = - A/2. (9.3)
Полученная энергия локальной связи в первом приближении определяется интегралом А - обменным интегралом. Т.о. и в методе ВС решающую роль в образовании связи играет критерий максимального перекрывания волновых функций, участвующих в образовании связи.
Используя метод ВС, рассмотрим подробнее угловую зависимость валентных связей на примере радикала ОН. Величина обменного интеграла будет зависеть от угла между связями
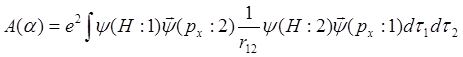 . (9.4)
. (9.4)
В
соответствии со схемой, представленной на рис.9.3, векторный характер функции ![]() позволяет представить её в виде:
позволяет представить её в виде:
![]() .
(9.5)
.
(9.5)
H
![]() рe
рe

![]()
![]() Xa O
Xa O
рh
Рис.9.3.
К вычислению обменного интеграла![]() .
.
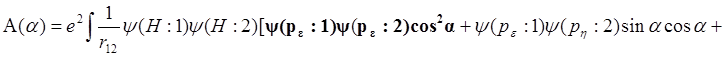
![]() .
(9.6)
.
(9.6)
Первый из выделенных членов есть обменный интеграл с составляющей по линии О-Н; второй - с составляющей под углом 90O к линии О-Н. Члены, содержащие sinacosa, исчезают в силу ортогональности yeyh. Поэтому получаем:
А(a) = А(0O)×cos2a + А(90O)sin2a. (9.7)
Соотношение 9.7 имеет большое значение. В конкретном случае радикала Н-О А(0O) = - 2.0 эВ, А(90O) = + 0.6 эВ. Следует отметить, что при спаривании орбиталей О(2рх) и Н(1s) в величину обменной энергии вносит вклад не только А(a) от указанных орбиталей (хотя и основной), но и обменная энергия от орбитали О(2рy). Значение последней будет равно
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.