В системе
которая поддерживается при постоянных температуре и давлении, имеется
пропорциональная зависимость между произвольно выделенным объёмом и суммарным
количеством находящихся в нём частиц V ~ nS. Подобно этому, объёмная скорость
реакционной смеси пропорциональна суммарному потоку частиц в любом сечении
реактора ![]() ~
~ ![]() . Поэтому для данной реакции
. Поэтому для данной реакции
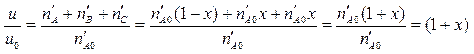 . (6)
. (6)
Откуда следует
![]() .
.
Пример 5.
Реакция второго порядка с уменьшением числа частиц 2А ¾® В.
В этом случае вместо уравнений (4), (5) и (6) имеем
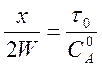 , (7)
, (7)
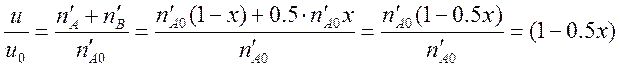 ,(8)
,(8)
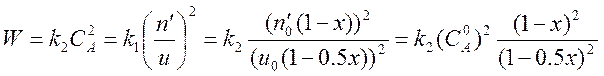 .(9)
.(9)
Подставляя выражение (9) в уравнение (7), получаем уравнение для нахождения х.
I. Реактор идеального вытеснения.
Пусть реакция
протекает в реакторе идеального вытеснения, который можно рассматривать как
последовательность реакторов полного смешения. Будем считать, что
«элементарный» реактор полного смешения имеет объём ![]() , поток
реагента «А» на входе в объём dV обозначим
, поток
реагента «А» на входе в объём dV обозначим ![]() , на выходе из него –
, на выходе из него – ![]() . Обозначения
. Обозначения ![]() и
и ![]() вводятся аналогично. Степень превращения
вещества А к моменту, когда оно попадает в объём dV,
равна х.
вводятся аналогично. Степень превращения
вещества А к моменту, когда оно попадает в объём dV,
равна х.
![]()
![]()
![]()
![]()
![]() [моль/с]
[моль/с]
![]()
![]()
![]()
![]() [л/с]
[л/с]
Применяя к реактору с объёмом dV уравнение (1) получаем
![]() .
.
![]()
![]() .
.
Отсюда 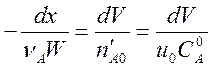 .
.
Интегрируя, получаем 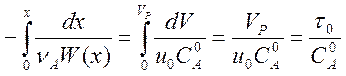 .
.
Окончательно получаем
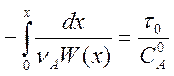 . (10)
. (10)
Остаётся установить вид зависимости W от x и провести интегрирование.
Интересно сопоставить это уравнение с уравнением (3а) для реактора полного смешения.
Пример 6. Реакция первого порядка, протекающая с увеличением числа частиц А ¾® В + С.
Зависимость W от x для этого случая уже получена выше
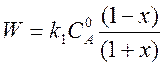 .
.
Подставляя эту зависимость в уравнение (10) с учётом того, что nА = – 1 получаем:
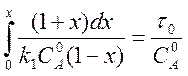 .
.
Интегрирование несложно и выполняется следующим образом
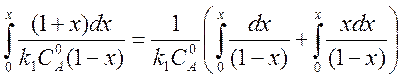 ,
,
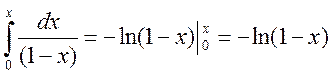 ,
,
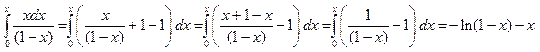 .
.
В результате получаем
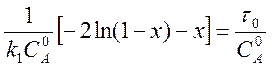 ,
,
![]() .
.
Получилось трансцендентное уравнение. Оно может быть решено численно, например, методом подбора решения на калькуляторе.
Пример 7. Реакция первого порядка, протекающая без изменения общего числа частиц.
С этого примера мы начинали рассмотрение для реактора полного смешения. Важно отметить, что в понятие «общее число частиц» включаются не только реагенты и продукты, но также молекулы растворителя или газа-разбавителя. Поэтому в случае, когда в исходной реакционной смеси реагенты находятся в небольшой концентрации в атмосфере инертного газа или растворителя, объёмная скорость u на входе и выходе реактора будет одинакова. При этом для реакции первого порядка всегда будет справедливо соотношение
![]() .
.
После подстановки этого соотношения в уравнение (10) и интегрирования получаем
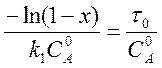 ,
,
откуда
![]()
или
![]()
Выражение такого же вида получается при рассмотрении реакции первого порядка в закрытой системе при постоянном объёме.
Рогов Владимир Алексеевич,
Лузгин Михаил Владимирович
Практикум по физической химии
ХИМИЧЕСКОЕ РАВНОВЕСИЕ И НЕОБРАТИМАЯ РЕАКЦИЯ В ОТКРЫТОЙ СИСТЕМЕ. ГАЗОВАЯ ХРОМАТОГРАФИЯ
Методическое пособие
Ответственный редактор В. Н. Пармон
Редактор С. Д. Андреева
Оригинал-макет Н. В. Ложкиной
Подписано в печать
Формат Офсетная печать.
Уч.-изд. л. 1. Тираж 150 экз.
Заказ № .
Лицензия ЛР № 021285 от 6 мая 1998 г.
Редакционно-издательский центр НГУ
630090, Новосибирск-90, ул Пирогова, 2
* Приведены значения скорости потока газа-носителя и тока детектора, которые используются в данной работе.
[1] Программ – две. Основная программа управления установкой называется HimLab3.exe. Программа, задающая для конкретного опыта последовательность переключения кранов, уставки температур и потоки газов, имеет расширение TMR, пишется оператором и может называться как угодно, например, 220.TMR или qwerty.TMR.
[[i]] Kraus, M. In Handbook of Heterogeneous Catalysis; Ertl, G., Knozinger, H., Weitkamp, J., Eds.; Wiley-VCH: Weinheim, Germany, 1997; Vol. 5, pp 2159-2165.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.