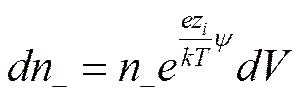
а число положительных
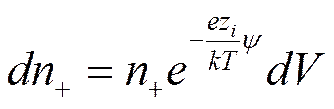
Заряд элемента объема будет равен тогда
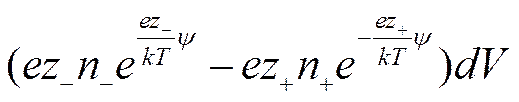
а плотность заряда
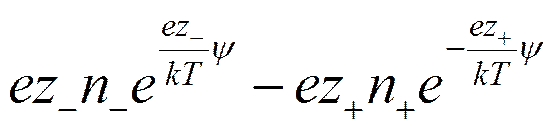
Учитывая, что в растворе находятся различные сорта ионов, и приписывая валентности иона знак, отвечающий его заряду, можно написать, что
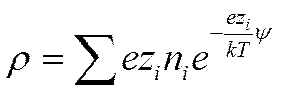 (I I -35)
(I I -35)
Подставим величину ρ из выражения (II-35) в уравнение Пуассона
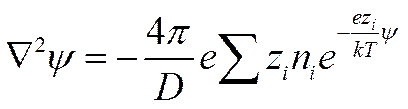 (I I-36)
(I I-36)
Уравнение (II-36) в его общем виде трудно для решения. Чтобы упростить его, Дебай и Гюккель предположили, что еzi ψ << kT, т. е. что электростатическое взаимодействие мало по сравнению с термической энергией. Разложив показательную функцию в ряд
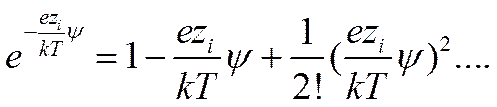 (I I - 37)
(I I - 37)
они ограничились только двумя его первыми членами, получив для ρ следующее уравнение:
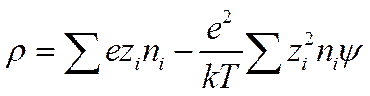 (I I-38)
(I I-38)
Первый член правой части уравнения (II-38) по закону электронейтральности равен нулю, откуда
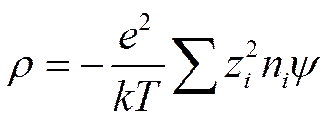
и, следовательно,
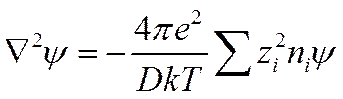 (I I-39)
(I I-39)
или
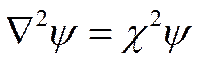 (I I -40)
(I I -40)
если ввести обозначение
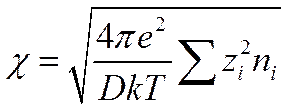 (I I -41)
(I I -41)
Величина χ, точнее 1/ χ, имеет, как это будет показано ниже, большое значение в теории растворов электролитов. Учитывая шаровую симметрию ионной атмосферы, можно вместо V2 ψ написать
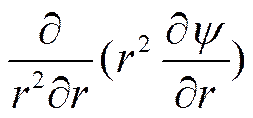 (I I-42)
(I I-42)
и, подставив это значение V2 ψ в уравнение (II-42), получить
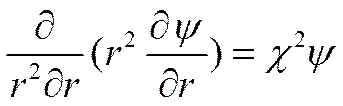 (I I-43)
(I I-43)
где r— расстояние от центрального иона до места определения потенциала ψ
Общим решением этого дифференциального уравнения будет
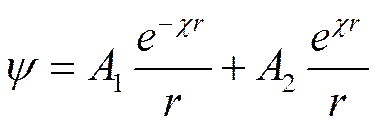 (I I-44)
(I I-44)
Константы интегрирования A1 иA2находят из граничных условий. Как следует из основных законов электростатики, при r->oo ψ -> 0, что является первым граничным условием. Это условие выполняется в том случае, если А2 = 0, так как иначе с удалением от центрального иона ψ будет стремиться к бесконечности (е χr—величина более высокого порядка, чем r). Следовательно, при А2 = О
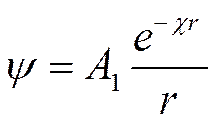 (I I -45)
(I I -45)
Для определения константы интегрирования a1в первом приближении теории Дебая — Гюккеля предполагается, что ионы можно отождествить с материальными точками, обладающими определенным зарядом. В этом случае при г -> 0 потенциал ψ должен стремиться к потенциалу самого иона ψiт. е.
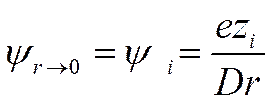 (I I-46)
(I I-46)
Если е -χr разложить в ряд, то
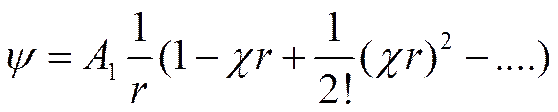
При r -> 0 всеми членами ряда можно пренебречь по сравнению с единицей. Тогда
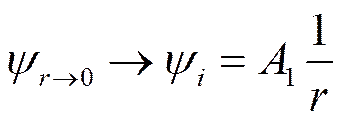
и, следовательно,
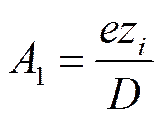 (I I-47)
(I I-47)
откуда, а также из (II-45),
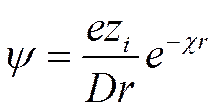 (I I-48)
(I I-48)
Величина ψ в уравнении (II-48) представляет собой среднее значение потенциала в точке r, создаваемого ионной атмосферой и центральным ионом. Для реальных растворов специфическим является потенциал ионной атмосферы ψia, который находят по правилу суперпозиции потенциалов как разность ψ и ψi
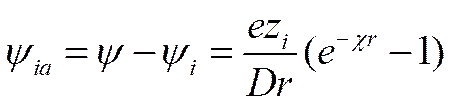
Для вычисления энергии взаимодействия необходимо определить потенциал ионной атмосферы в точке нахождения центрального иона, т. е. найти предел ψia при r->0. Используя вновь тот же прием, т. е. разлагая показательную функцию в ряд и пренебрегая высшими членами разложения, находим, что
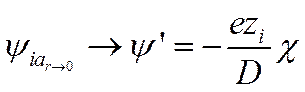 (I I-49)
(I I-49)
Величину ψ’ в соответствии с уравнением (II-49) можно рассматривать как потенциал, создаваемый в точке нахождения центрального иона другим ионом с противоположным знаком и находящимся от центрального иона на расстоянии 1/χ. Величина 1/ χ называется характеристической длиной. Так как потенциал создается не единичным ионом, а всей ионной атмосферой, то 1/ χ можно отождествить с радиусом ионной атмосферы. Величину χ , а следовательно, и характеристическую длину 1/ χ можно рассчитать по уравнению (II-41).
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.