При некоторой температуре,
которую назовем ![]() , вода закипит
, вода закипит
(см. рис. б). Обозначим объем, занимаемый
при этой температуре, через ![]() .
.
И далее сколько бы мы не сообщали тепла воде, температура кипящей воды (при данном постоянном давлении) не изменится.
Температура ![]() называется температурой
парообразования. Из
сказанного следует, что данному давлению Р1 соответствует
единственная и вполне определенная температура парообразования
называется температурой
парообразования. Из
сказанного следует, что данному давлению Р1 соответствует
единственная и вполне определенная температура парообразования ![]() .
.
Другими словами – это есть температура насыщения при данном давлении.
Отложим на диаграмме V-P на расстоянии от оси объемов Р1 объем![]() , при котором начинается процесс кипения
воды (процесс нагрева воды отображается линией а1–
, при котором начинается процесс кипения
воды (процесс нагрева воды отображается линией а1–![]() ).
).
Дальнейшее повышение температуры кипящей воды при сообщении тепла не происходит, но зато вода будет превращаться в пар до тех пор, пока в сосуде не испарится последняя капля воды.
Процесс парообразования сопровождается существенным увеличением объема, занимаемого рабочим телом, и неизменностью температуры и давления, так как вес поршня в цилиндре оставался постоянным.
Таким образом, рассматриваемый процесс парообразования является одновременно изобарным и изотермическим.
Обозначим объем пара, соответствующий
концу парообразования, через ![]() (рис. в) и
отложим этот объем на диаграмме V-P на продолжении прямой линии а1–
(рис. в) и
отложим этот объем на диаграмме V-P на продолжении прямой линии а1–![]() . Отрезок
. Отрезок ![]() –
– ![]() характеризует полное приращение объема в
процессе парообразования при Р=соnst и t = cоnst.
характеризует полное приращение объема в
процессе парообразования при Р=соnst и t = cоnst.
Пар в состоянии
окончания процесса парообразования, имеющий удельный объем ![]() и температуру парообразования
и температуру парообразования ![]() называется сухим насыщенным паром.
называется сухим насыщенным паром.
Процесс парообразования в диаграмме T-S
Раньше мы уже рассмотрели, что процесс превращения воды в перегретый пар складывается из трех процессов:
1) процесса нагрева воды (до температуры кипения при Р=соnst);
2) процесса парообразования (при t = cоnst и Р=соnst);
3) процесса нагрева пара (при Р=соnst и изменяющейся температуре).
Теперь рассмотрим процесс нагрева воды в диаграмме S-T.
Для более полного исследования термодинамических процессов и облегчения исследований и расчетов в термодинамику был введен математически немецким физиком Р. Клаузиусом еще один параметр состояния газа (шестой) – энтропия S.
Энтропия, ккал/(кг×град), выражается формулой:
Sв = 2,303 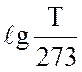 .
.
Для воды и водяного пара мы условимся вести отсчет от 0 оС, это значит, что и энтропия при этом будет равна 0, т.е. при t = 0 оС или Т = 273 оК имеем
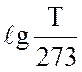 =
= 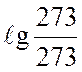 =
=![]() .
.
Зависимость Sв в T-S координатах выражается логарифмической кривой.
Задаваясь различными значениями Т, находим по формуле для Sв различные значения S. На рис. 4 строится кривая а–к.
Вначале процесс идет чисто изобарный (Р=соnst), при этом температура возрастает, затем при какой-то температуре наступит состояние кипения, т.е. данному давлению будет соответствовать своя температура насыщения (допустим т. b1). Здесь процесс переходит в изобарно-изотермический (Р=соnst и Т=соnst) и изображается горизонтальной прямой (b1–с1).
Из диаграммы мы можем заключить, что чем выше давление, тем выше будет температура кипения при этом давлении. Вот мы и получим ряд точек b1, b2, b3 и т.д. до точки К.
Кривая (а–к) представляет собой геометрическое место точек начала кипения воды при различных давлениях, т.е. в точке b1 будет соответствовать давление Р1, точке b2– давление Р2 и т.д.
Кривая (а–к) является кривой жидкости или нижней пограничной кривой.
Процессы нагрева воды при давлениях Р2, Р3 и т.д., которым соответствуют температуры парообразования (кипения) Тн2, Тн3 и т.д., будут отображаться соответственно отрезками (а–b2), (а–b3) и т.д. нижней пограничной кривой.

Рис. 4. Процесс парообразования в T-S диаграмме
При дальнейшем сообщении тепла кипящей воде при Р1 она начнет испаряться и, следовательно, начнется процесс парообразования, который на T-S диаграмме при давлениях Р1, Р2, Р3 и т.д. отобразится горизонтальными отрезками (b1–с1), (b2–с2) и т.д.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.