Министерство образования Российской Федерации
Российский Государственный Университет
нефти и газа имени И.М. Губкина
Задание №1
Расчет абсолютной энтропиихимических соединений в различных агрегатных состояниях.
Вариант 37.
Кафедра физической и каллойдной химии.
Выполнил студент гр. ХТ-04-3
Молоканов А.А.
Проверил: Стыценко В.Д.
Москва
2006
Исходные данные:
NC(CH2 )CN-сукциннонитрил.
Тпп=233.31 К, ∆Нпп=1481,7 кал/моль;
Тпл=331,2 К, ∆Нпп=885.1 кал/моль;
Рнп331.2 =0.177 атм;
∆Н 298 сублим =16730 кал/моль;
Рнп298 =9.7*10-6 атм;
Таблица исходных данных.
|
№ |
T |
Cp |
|
1 |
5,00 |
0,026 |
|
2 |
6,80 |
0,097 |
|
3 |
10,71 |
0,480 |
|
4 |
14,60 |
1,081 |
|
5 |
20,09 |
2,253 |
|
6 |
28,15 |
4,241 |
|
7 |
37,15 |
6,396 |
|
8 |
47,09 |
8,439 |
|
9 |
55,11 |
9,837 |
|
10 |
72,56 |
12,330 |
|
11 |
86,52 |
13,990 |
|
12 |
96,84 |
15,010 |
|
13 |
117,84 |
16,910 |
|
14 |
128,35 |
17,820 |
|
15 |
144,83 |
19,200 |
|
16 |
163,90 |
20,760 |
|
17 |
180,75 |
22,180 |
|
18 |
196,41 |
23,480 |
|
19 |
205,74 |
24,400 |
|
20 |
224,35 |
26,220 |
|
21 |
233,31 |
27,096 |
|
22 |
233,31 |
32,110 |
|
23 |
241,38 |
32,400 |
|
24 |
267,78 |
33,350 |
|
25 |
286,36 |
34,160 |
|
298,00 |
34,160 |
|
|
26 |
304,41 |
35,150 |
|
27 |
322,49 |
36,380 |
|
28 |
326,42 |
36,940 |
|
29 |
328,32 |
40,050 |
|
30 |
331,20 |
44,764 |
|
31 |
331,20 |
38,223 |
|
32 |
334,05 |
38,320 |
|
33 |
340,82 |
38,550 |
|
34 |
347,55 |
38,750 |
|
35 |
350,00 |
38,823 |
Задание:
Вычислите абсолютную энтропию сукцинонитрила в жидком состоянии при температуре 350 С .
Решение:
Для нахождения энтропии мы будим использовать следующую формулу:
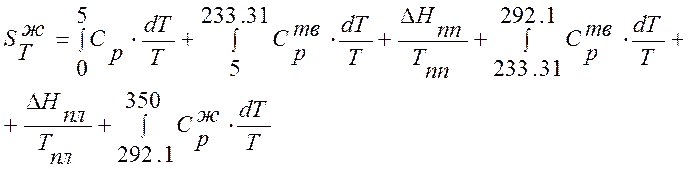
Величину первого интеграла определяют, используя уравнение зависимости теплоемкости твердых кристаллических тел вблизи абсолютного нуля Сp=aT3
0,0026=a*5,003
a=0,000208
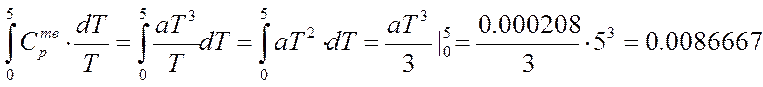
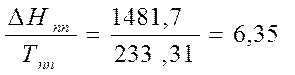 кал/моль*К
кал/моль*К
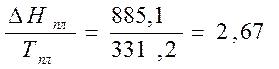 кал/моль*К
кал/моль*К
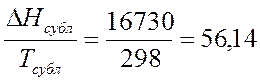 кал/моль*К
кал/моль*К
Интегралы 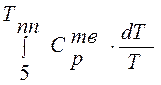 ;
;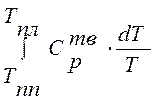 ;
; 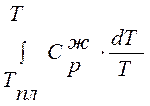 ,
, определяются графически, строя зависимость Ср/T от
Т – вычисляют по методу прямоугольной трапеции.
,
, определяются графически, строя зависимость Ср/T от
Т – вычисляют по методу прямоугольной трапеции.
Определяем методом экстраполяции теплоемкости при температурах фазовых переходов и Т=350.
1. Тпп=233,31К
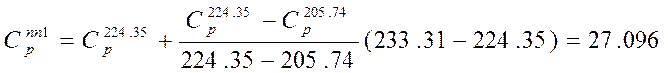 кал/моль*К
кал/моль*К
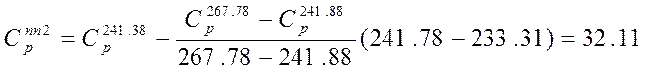 кал/мольК
кал/мольК
2. Тпл=292,1 К
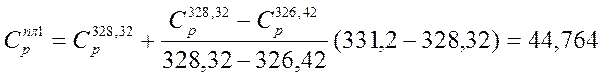 кал/моль*К
кал/моль*К
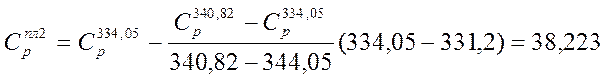 кал/моль*К
кал/моль*К
3. Т=350 К.
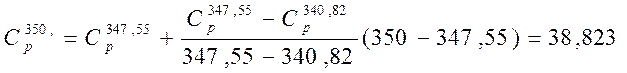 кал/моль*К
кал/моль*К
Полученные результаты внесём в таблицу 2.
Вычислим значения (Ср/Т),(lnT) и полученные результаты внесём в таблицу 2.
Экспериментальные значения теплоёмкости(Ср),(Ср/Т),(lnT),(S),(S2) для ацетонитрила при различных температурах.
Таблица 2.
|
№ |
T |
Cp |
Cp/T |
lnt |
S |
S2 |
|
1 |
5,00 |
0,026 |
0,005 |
1,609438 |
||
|
2 |
6,80 |
0,097 |
0,014 |
1,916923 |
0,018 |
0,019 |
|
3 |
10,71 |
0,480 |
0,045 |
2,371178 |
0,116 |
0,131 |
|
4 |
14,60 |
1,081 |
0,074 |
2,681022 |
0,231 |
0,242 |
|
5 |
20,09 |
2,253 |
0,112 |
3,000222 |
0,511 |
0,532 |
|
6 |
28,15 |
4,241 |
0,151 |
3,337547 |
1,059 |
1,095 |
|
7 |
37,15 |
6,396 |
0,172 |
3,614964 |
1,453 |
1,475 |
|
8 |
47,09 |
8,439 |
0,179 |
3,852061 |
1,746 |
1,759 |
|
9 |
55,11 |
9,837 |
0,178 |
4,009331 |
1,434 |
1,437 |
|
10 |
72,56 |
12,330 |
0,170 |
4,284414 |
3,040 |
3,049 |
|
11 |
86,52 |
13,990 |
0,162 |
4,460376 |
2,315 |
2,316 |
|
12 |
96,84 |
15,010 |
0,155 |
4,57306 |
1,634 |
1,634 |
|
13 |
117,84 |
16,910 |
0,143 |
4,769328 |
3,134 |
3,132 |
|
14 |
128,35 |
17,820 |
0,139 |
4,854761 |
1,484 |
1,484 |
|
15 |
144,83 |
19,200 |
0,133 |
4,975561 |
2,236 |
2,236 |
|
16 |
163,90 |
20,760 |
0,127 |
5,099256 |
2,472 |
2,471 |
|
17 |
180,75 |
22,180 |
0,123 |
5,197115 |
2,101 |
2,101 |
|
18 |
196,41 |
23,480 |
0,120 |
5,280204 |
1,897 |
1,897 |
|
19 |
205,74 |
24,400 |
0,119 |
5,326613 |
1,111 |
1,111 |
|
20 |
224,35 |
26,220 |
0,117 |
5,413207 |
2,191 |
2,192 |
|
21 |
233,31 |
27,096 |
0,116 |
5,452368 |
1,044 |
1,044 |
|
22 |
233,31 |
32,110 |
0,138 |
5,452368 |
0,000 |
0,000 |
|
23 |
241,38 |
32,400 |
0,134 |
5,486372 |
1,097 |
1,097 |
|
24 |
267,78 |
33,350 |
0,125 |
5,590166 |
3,416 |
3,412 |
|
25 |
286,36 |
34,160 |
0,119 |
5,65725 |
2,265 |
2,264 |
|
298,00 |
34,160 |
0,115 |
5,697093 |
1,361 |
1,361 |
|
|
26 |
304,41 |
35,150 |
0,115 |
5,718375 |
0,737 |
0,738 |
|
27 |
322,49 |
36,380 |
0,113 |
5,776072 |
2,064 |
2,064 |
|
28 |
326,42 |
36,940 |
0,113 |
5,788185 |
0,444 |
0,444 |
|
29 |
328,32 |
40,050 |
0,122 |
5,793989 |
0,223 |
0,223 |
|
30 |
331,20 |
44,764 |
0,135 |
5,802722 |
0,370 |
0,370 |
|
31 |
331,20 |
38,223 |
0,115 |
5,802722 |
0,000 |
0,000 |
|
32 |
334,05 |
38,320 |
0,115 |
5,811291 |
0,328 |
0,328 |
|
33 |
340,82 |
38,550 |
0,113 |
5,831354 |
0,771 |
0,771 |
|
34 |
347,55 |
38,750 |
0,111 |
5,850909 |
0,756 |
0,756 |
|
35 |
350,00 |
38,823 |
0,111 |
5,857933 |
0,272 |
0,272 |
|
SΣ |
45,060 |
45,185 |
По результатам табл.1 построим зависимости Ср/Т=f(Т) (рис2) и Ср/Т=f(lnT) (рис3).
рисунок 2
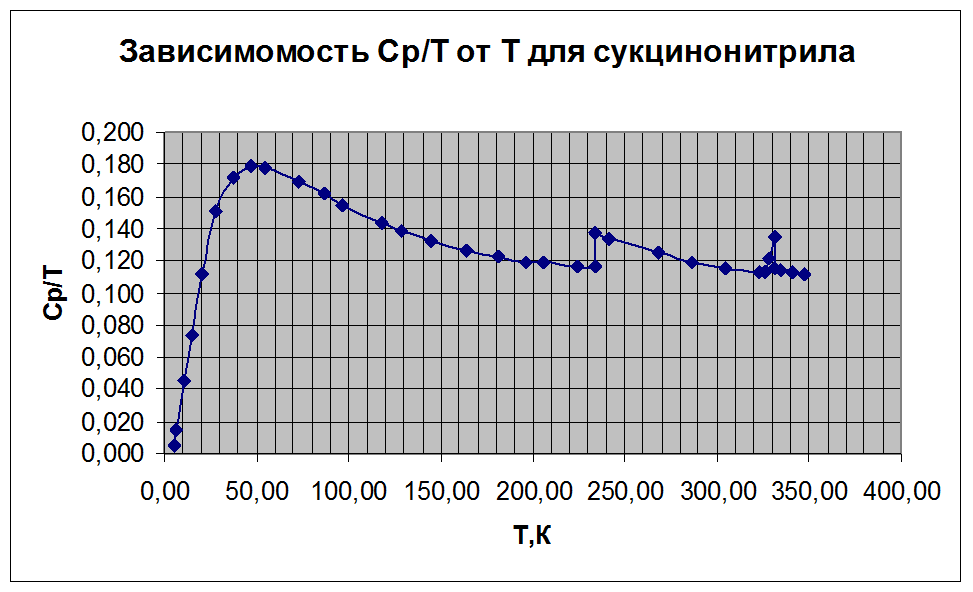
Из рисунка 2 видно, что в области ф.п. функция Ср/Т претерпевает разрыв. Для точного интегрирования используем метод Симпсона-Томпсона.
Площади трапеций находим по формуле:
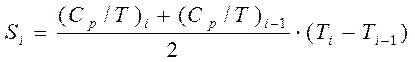
S1=(0,005+0,014)*(6,80-5,00)/2=0,02
S2=(0,014+0,045)*(10,71-6,80)/2=0,12
S3=(0,045+0,074)*(14,60-10,71)/2=0,23
S4=(0,074+0,112)*(20,09-14,60)/2=0,51
S5=(0,112+0,151)*(28,15-20,09)/2=1,06
S6=(0,151+0,172)*(37,15-28,15)/2=1,45
S7=(0,172+0,179)*(47,09-37,15)/2=1,75
S8=(0,179+0,178)*(55,11-47,09)/2=1,43
S9=(0,178+0,170)*(72,56-55,11)/2=3,04
S10=(0,170+0,162)*(86,52-72,56)/2=2,31
S11=( 0,162+0,155)*(96,84-86,52)/2=1,63
S12=( 0,155+0,143)*(117,84-96,84)/2=3,13
S13=( 0,143+0,139)*(128,35-117,84)/2=1,48
S14=(0,139+0,133)*(144,83-128,35)/2=2,24
S15=(0,133+0,127)*(163,90-144,83)/2=2,47
S16=(0,127+0,123)*(180,75-163,90)/2=2,10
S17=(0,123+0,120)*(196,41-180,75)/2=1,90
S18=(0,120+0,119)*(205,74-196,41)/2=1,11
S19=(0,119+0,117)*(224,35-205,74)/2=2,19
S20=(0,117+0,116)*(233,31-224,35)/2=1,04
S21=(0,116+0,138)*(233,31-233,31)/2=0,00
S22=(0,138+0,134)*(241,38-233,31)/2=1,10
S23=(0,134+0,125)*(267,78-241,38)/2=3,42
S24=(0,125+0,119)*(286,36-267,78)/2=2,27
S25=(0,119+0,115)*(304,41-286,36)/2=2,12
S26=(0,115+0,113)*(322,49-304,41)/2=2,06
S27=(0,113+0,113)*(326,42-322,49)/2=0,44
S28=(0,113+0,122)*(328,32-326,42)/2=0,22
S29=(0,122+0,135)*(331,20-328,32)/2=0,37
S30=(0,135+0,115)*(331,20-331,20)/2=0,00
S31=(0,115+0,115)*(334,05-331,20)/2=0,33
S32=(0,115+0,113)*(340,82-334,05)/2=0,77
S33=(0,113+0,111)*(347,55-340,82)/2=0,76
S34=(0,111+0,111)*(350,00-347,55)/2=0,27
Сумма площадей трапеций равна 45,079. Полученные результаты внесём в таблицу 2.
Вычисляем энтропию жидкого состояния при 350 С
Sж = 0.009+6.35+2.67+45,079= 54,111кал/моль;
рисунок 3
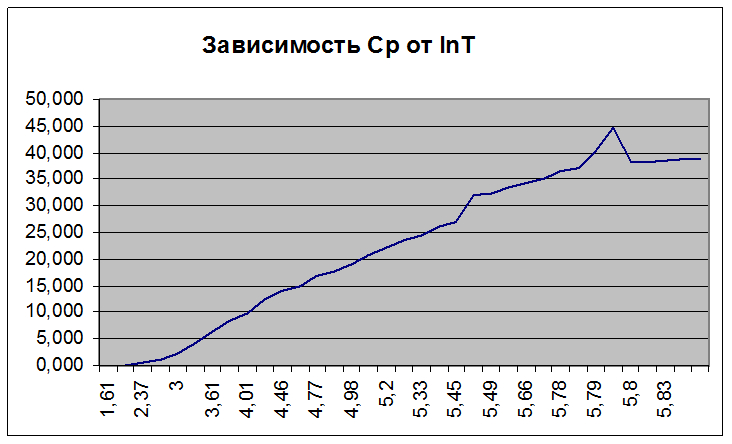
Из рисунка 3 видно, что в области ф.п. функция Ср/Т претерпевает ска. Для точного интегрирования используем метод Симпсона-Томпсона.
Площади трапеций находим по формуле:
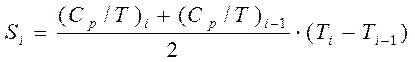
Полученные результаты внесём в таблицу 2.
Расхождение в величине энтропиижидкого состояния, вычисленное с применением рис2 и рис3 сосавляет 0.125единицы. Расхождение минимально.
Sж = 0.009+6.35+2.67+45,079= 54,111кал/моль;
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.