Домашняя работа №1
Вариант 7
N2O Закись азота
|
№ |
T |
Cp |
Cp/T |
|
1 |
15 |
0,7 |
0,05 |
|
2 |
25 |
2,5 |
0,10 |
|
3 |
50 |
6,8 |
0,14 |
|
4 |
75 |
8,6 |
0,11 |
|
5 |
100 |
9,8 |
0,10 |
|
6 |
125 |
10,7 |
0,09 |
|
7 |
150 |
12,0 |
0,08 |
|
8 |
175 |
13,6 |
0,08 |
|
пл |
182,3 |
14,1 |
0,08 |
|
11,0 |
0,06 |
||
|
кип |
184,6 |
11,0 |
0,06 |
|
7,9 |
0,04 |
||
|
9 |
250 |
8,69 |
0,03 |
|
298 |
9,25 |
0,03 |
|
|
10 |
300 |
9,27 |
0,03 |
|
11 |
400 |
10,25 |
0,03 |
|
12 |
500 |
11,03 |
0,02 |
Определяем методом экстраполяции теплоемкости при температурах фазовых переходов и Т=298.
1. Тпл=182,3 К
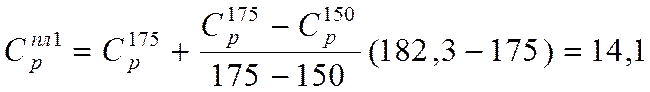 кал/моль*К
кал/моль*К
Так как между точкой плавления и точкой кипения нет значений Ср,
то для упрощения рассчитаю теплоемкость жидкости при Т=182,3 как среднюю величину между теплоемкостью закиси азота в твердом состоянии при Т=182,3 и в парообразном при Т=184,6.
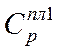 =11,0 кал/моль*К
=11,0 кал/моль*К
2. Ткип=184,6 К
 =11,0 кал/моль*К
=11,0 кал/моль*К
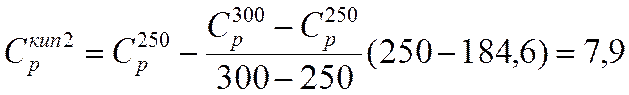 кал/моль*К
кал/моль*К
3. Т=298 К.
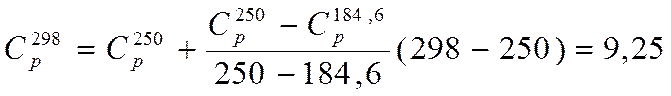 кал/моль*К
кал/моль*К
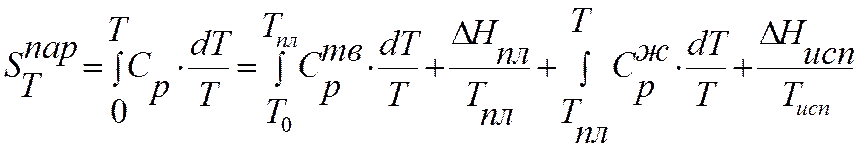
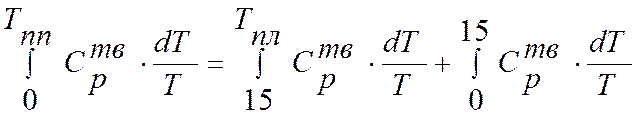
При малых температурах Сp=aT3
0,7=a*153
a=2,07*10-4
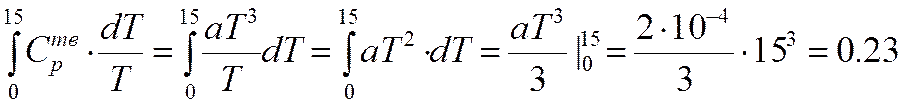
Интегралы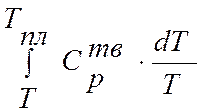 ;
; 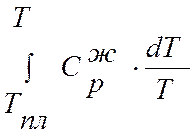 ,
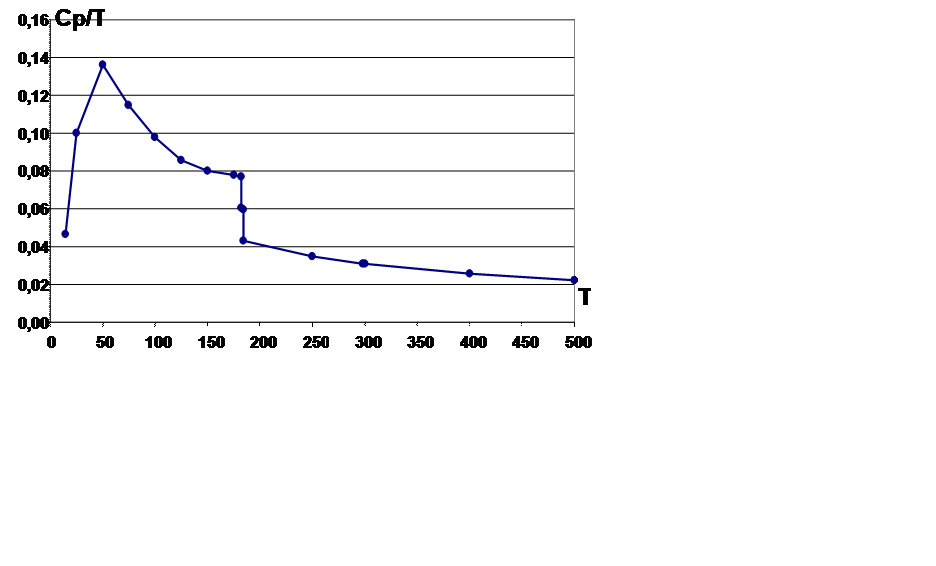
определяются графически, строя зависимость Ср/T от Т –
вычисляют по методу прямоугольной трапеции.
,
определяются графически, строя зависимость Ср/T от Т –
вычисляют по методу прямоугольной трапеции.
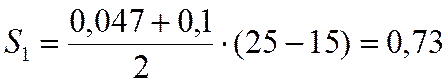
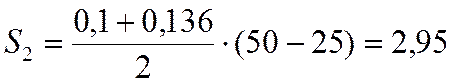 и
тд.
и
тд.
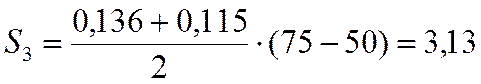
И так далее.
S1=0,73
S2=2,95
S3=3,13
S4=2,66
S5=2,30
S6=2,07
S7=1,97
S8=0,57
S10=0,14
S12=2,54
S13=1,58
Сумма площадей трапеций равна 20,64.
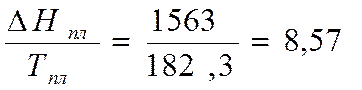 кал/моль*К
кал/моль*К
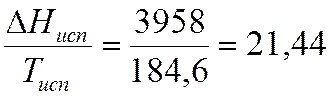 кал/моль*К
кал/моль*К
Sпар= 20,64+ 0,23+ 8,57+ 21,44=50,88 кал/моль*К
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.