На рис. 5.10 приведена температурная зависимость коэффициентов самодиффузии Ag по поверхности, по границам зерен и по объему зерен.
Хорошо известно, что Th, ,локально адсорбированный на вольфрамовой нити, при нагревании быстро покрывает всю ее поверхность, не проникая в заметном количестве внутрь металла.
§ 5.3. Диффузия в поле градиента
концентраций
Коэффициенты самодиффузии
элементов, образующих растворы замещения, различны. Если соединить два
полубесконечных образца, содержащих два элемента в различных количествах, то
можно определить один коэффициент диффузии ![]() (с),
который полностью описывает процесс гомогенизации. В связи с этим возникает
задача нахождения связи между
(с),
который полностью описывает процесс гомогенизации. В связи с этим возникает
задача нахождения связи между ![]() (с), отвечающего данному
составу, и коэффициентами самодиффузии при том же составе. Величину
(с), отвечающего данному
составу, и коэффициентами самодиффузии при том же составе. Величину ![]() часто называют химическим коэффициентом
диффузии.
часто называют химическим коэффициентом
диффузии.
Впервые различия потоков диффундирующих навстречу друг другу компонентов были обнаружены в 1947 г. Смигельскасом и Киркендалом.
Эффект Киркендала. Прямоугольный пруток латуни обматывали тонкой молибденовой проволокой (молибден не растворим в меди и латуни), а затем покрывали слоем меди. Такой образец последовательно отжигали. После каждого отжига от прутика отрезали кусок, в котором определяли расстояние между молибденовыми проволочками. Оказалось, что расстояние между ними уменьшается со временем. Расстояние между проволочками может измениться только в том случае, если поток атомов цинка из латуни заметно превосходит поток атомов меди внутрь через ту же плоскость. Аналогичный эффект впоследствии был обнаружен для различных металлов. Таким образом, эффект Киркендалаимеет совершенно общий характер.
Анализ Даркена. В основу теории эффекта Киркендала Даркен
(1948 г.) положил представление о перемещении границы - раздела между латунью и медью. Если скорость перемещения и, то перенос масс компонентов через границу составит
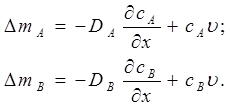 (5.37)
(5.37)
Но, так как 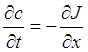 , то могу быть получены следующие
соотношения:
, то могу быть получены следующие
соотношения:
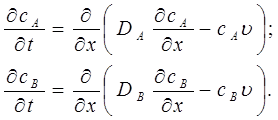
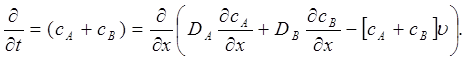
значение, то имеем
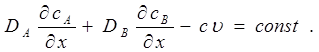 |
На бесконечности градиенты концентраций и uобращается в нуль, поэтому const = 0 и
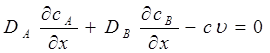 |
Поскольку 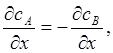
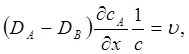 или, вводя молярные
доли, получаем
или, вводя молярные
доли, получаем 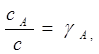 получаем
получаем
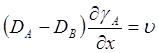 (5.38)
(5.38)
Из (5.38) следует, что υ пропорционально DA-DB. Подставляя выражение для υ в одно из исходных уравнений и дифференцируя его по х, имеем
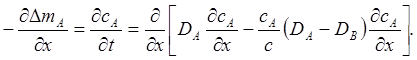
После упрощения получаем
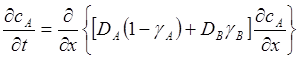 . (5.39)
. (5.39)
Из сопоставления (5.39) со вторым законом Фика (5.2) следует, что коэффициент взаимной диффузии равен
![]() (5.40)
(5.40)
или
![]()
так как 1-γА=γВ. Из
эксперимента определяют значение ![]() . Для нахождения DА
и DB необходимо второе уравнение, связывающее их с какой-либо
экспериментально определяемой величиной. Например, со скоростью перемещения
проволочек или другой какой-либо метки, т. е.
. Для нахождения DА
и DB необходимо второе уравнение, связывающее их с какой-либо
экспериментально определяемой величиной. Например, со скоростью перемещения
проволочек или другой какой-либо метки, т. е.
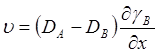 . (5.41)
. (5.41)
Многочисленными работами установлено, что расстояние, пройденное метками от исходного положения, выражается квадратичной зависимостью от времени. В диффузионной паре такого типа область любого заданного состава сдвигается как tl/2, поэтому состав области, окружающей метки, не меняется. Значение v находят дифференцированием зависимости хт от t. Таким образом, эксперимент позволяет определить DA и DB для изотермической диффузии в бесконечном образце.
Используя эти соображения, Даркен вычислил, что при содержании в латуни 22,5% Zn DСu=2,2*10-9 см2/с, Dzn=5,1*10-9 см2/с. Следует отметить, что эти значения коэффициентов диффузии нельзя приравнивать к коэффициентам диффузии, полученным в результате эксперимента с мечеными атомами в отсутствие градиента концентрации.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.