y = f(x1, x2, x3, …) (1)
где y - какое-либо свойство (вязкость, теплопроводность и т.д.), xi - параметры состояния (давление, температура и т.д.).
Влияние давления на свойства газов оценено с помощью уравнения Ли-Кеслера. Свойства газовых смесей вычислены с помощью методов Джосси-Стила-Тодоса, Линдсея-Бромли и правила Вильке.
Равновесие реакций выражается через константу равновесия Кр:
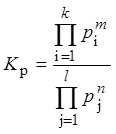 (2)
(2)
где р - парциальные давления.
Для учета недостижения равновесия использован метод приближения к равновесию по температуре.
Процессы конденсации описаны с помощью уравнения:
yi×Fi×P = gi×xi×Pнас,i×Fs,i×Пi (3)
где y - мольная доля компонента в газовой фазе, рассчитанная для нормальных условий; F - коэффициент фугитивности компонента в газовой смеси; Р – общее давление в системе; g - коэффициент активности компонента в жидкой фазе; x – мольная доля компонента в жидкой фазе; Рнас – давление насыщенных паров компонента при заданной температуре без учета влияния давления; Fs - коэффициент фугитивности жидкости; П – поправка Пойнтинга, учитывающая влияние давления на объем сконденсировавшейся жидкости.
Процессы теплопередачи рассчитывали по уравнениям:
Q = K×F×Dtср (4)
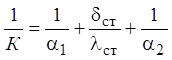 (5)
(5)
Коэффициенты теплоотдачи a1, a2 определялись по известным критериальным уравнениям.
При поверочных расчетах теплообменной аппаратуры приняты следующие допущения:
- теплообменник работает в стационарном режиме;
- коэффициент теплопередачи постоянен по всей поверхности;
- потери теплоты в окружающую среду или приток теплоты из среды пренебрежимо малы;
- продольным тепловым потоком можно пренебречь;
- схема движения потоков представляет собой либо чистый прямоток, либо чистый противоток;
- термические сопротивления отложений равны нулю.
В диссертации подробно рассмотрен процесс производства энергоносителя (водяного пара) и целевого продукта в трубчатом реакторе синтеза метанола. В связи с этим разработана модель реактора, основанная на законах Ньютона-Рихмана и Фурье и кинетических данных и представляющая собой следующую систему уравнений:
 dn1
= r1×dv (6)
dn1
= r1×dv (6)
dn2 = r2×dv (7)
N×cp×dT = (Q1× dn1 – Q2× dn2) - aг×dFст,вн×(Tг – Тст,вн) (8)
aг×dFст,вн×(Tг – Тст,вн)
=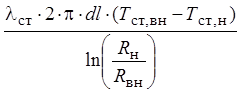 (9)
(9)
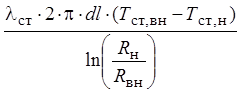 = aв×dFст,н×(Tст,н – Тв)
(10)
= aв×dFст,н×(Tст,н – Тв)
(10)
где dn1 и dn2 – соответственно количества метанола и СО2, образовавшиеся в результате реакций, моль; – количество, dv – объем слоя катализатора, м3; r1 и r2 – скорости реакций, моль/с; N – количество моль газовой смеси на входе в слой; ср – теплоемкость газовой смеси, Дж/(моль×К); dТ – изменение температуры в слое, К; Q1 и Q2 – тепловые эффекты реакций, Дж/моль; aг – коэффициент теплоотдачи от газовой смеси к стенке трубы, Вт/(м2×К); aв – коэффициент теплоотдачи от кипящей воды к стенке трубы, Вт/(м2×К); lст - коэффициент теплопроводности материала труб, Вт/(м×К); dст – толщина стенки, м; dFст,вн, dFст,н – внутренняя и наружная поверхности элемента трубы, м2; dl – высота элемента трубы, м; Rн и Rвн – наружный и внутренний радиусы трубы, м; Тг – температура газовой смеси на входе в слой, К; Тст,вн и Тст,н – температуры внутренней и наружной стенок трубы, К; Тв – температура воды, кипящей в межтрубном пространстве, К.
Уравнения (6,7) описывают материальный баланс в слое катализатора, уравнение (8) – тепловой баланс в слое, уравнения (9,10) - перенос тепла от газовой смеси к кипящей в межтрубном пространстве воде. Данную систему решали методом замены дифференциалов на конечные разности.
Далее в диссертации рассмотрены тепловые и материальные балансы на каждой стадии производства. Из балансов определяется выработка пара различного давления за счет тепла реакций и путем сжигания природного газа, потребление пара для привода турбин и проведения химических реакций, расход сырья и количество полученной продукции.
Затем в соответствии со схемой на рис. 3 производится выборка существенных показателей производства, основные из них следующие:
1) потребление природного газа на производство;
2) потребление природного газа для выработки пара высокого давления во вспомогательном котле;
3) расход электроэнергии в контуре метанола;
4) выработка пара среднего давления в реакторе метанола;
5) выработка пара низкого давления в контуре метанола;
6) расход оборотной воды в контур метанола;
7) выработка аммиака;
8) выработка метанола.
Экономическая модель построена на основе методик, изложенных в литературе, и рассчитывает следующие параметры: себестоимость продукции, текущие затраты, валовая прибыль, чистый дисконтированный доход и др.
При выборе математического аппарата для описания той или иной стадии или процесса критически обсуждаются все принятые допущения. Указывается, что при необходимости математическая модель может быть расширена и дополнена включением дополнительных блоков, описывающих те или иные процессы (например, зерно катализатора).
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.