5. У пациентов с судорогами в анамнезе кетамин может приводить к активации эпилептогенных очагов. Тем не менее, он обладает противосудорожной активностью.
6. В связи со свойством кетамина расширять бронхи, он часто рекомендуется для вводного наркоза пациентам с астмой.
a. При клинически применяемых дозах кетамина депрессия дыхания минимальная.
b. При повышенной секреции в полости рта кетамин может приводить к развитию ларингоспазма.
7. Кетамин оказывает выраженное стимулирующее действие на сердечно-сосудистую систему с повышением АД и давления в легочной артерии, учащением сердечных сокращений, вероятнее всего вследствие прямой стимуляции симпатической нервной системы. По этой причине нецелесообразно введение кетамина пациентам с ИБС. Кетамин оказывает угнетающее действие на миокард, проявляющееся только у тяжелобольных с истощением запасов катехоламинов.
F. Стероиды
1.
 |
2. Элтанолон — естественный метаболит прогестерона с сильной гипнотической активностью.
A. Применение внутривенных анестетиков для вводного наркоза (табл. 13-5)
1. Пропофол стал препаратом выбора для амбулаторных операций.
2.
 |
B. Применение внутривенных препаратов для поддержания анестезии
1. Доступность внутривенных препаратов с более быстрым началом действия и коротким периодом восстановления, как и удобные в употреблении системы внутривенного введения анестетика, облегчили поддержание анестезии путем постоянной инфузии внутривенных препаратов (техника тотальной внутривенной анестезии, ТВВА). Качество анестезии сравнимо с таковым при использовании летучих анестетиков.
2. Многие факторы влияют на оптимальный уровень дозировки внутривенных препаратов (табл. 13-6).
3. Такие клинические признаки глубины анестезии, как тонус скелетной мускулатуры, дыхание, АД, ЧСС, могут быть невыраженными при действии вспомогательных препаратов.
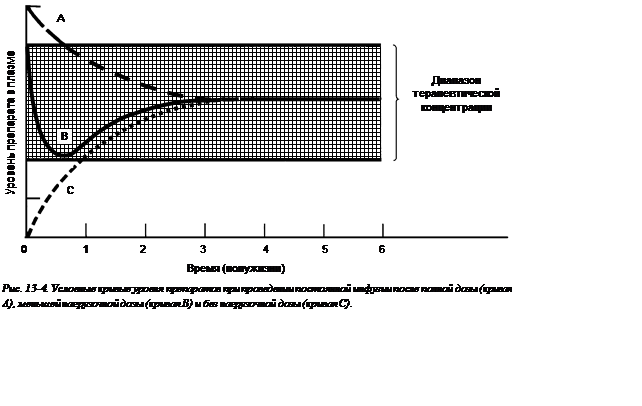
4. При использовании постоянного уровня инфузии может потребоваться промежуток времени, равный 4-5.5 периодам полувыведения, для достижения устойчивого состояния концентрации анестетика (это время можно сократить начальной загрузочной дозой) (рис. 13‑4).
a. Для метода постоянного введения лучше подходят быстро- и короткодействующие седативно-гипнотические и опиоидные препараты. Их можно точно титровать для достижения индивидуально подобранного и изменяемого эффекта.
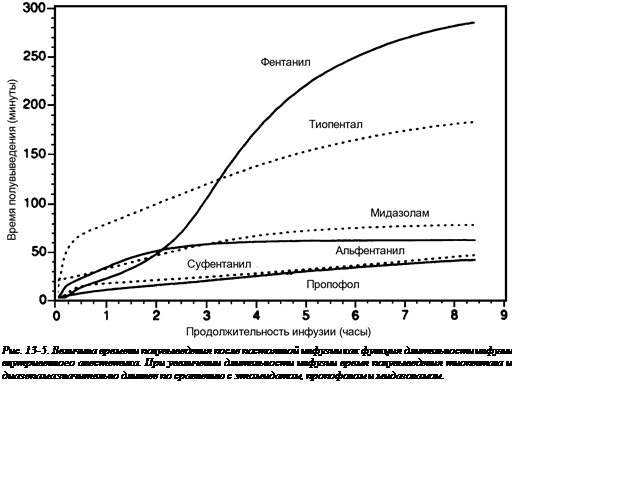
b. Время полувыведения является лучшим параметром подбора препаратов для длительного внутривенного введения (рис. 13‑5).
c.
 |
C. Применение внутривенных анестетиков для седации. Увеличивается популярность применения седативно-снотворных препаратов как части методики контролируемого анестезиологического пособия (см. гл. 47) в комбинации с местными анестетиками и для обеспечения седации при лечении пациентов в отделении интенсивной терапии.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.