Задача № 4.3
Сосуд емкостью V=40 литров содержит углекислый газ при давлении
а) Р1 = 0,5 МПа; б) Р1 = 0,8 МПа; в) Р1 = 1,0 МПа.
и температуре t1=30 оС. Определить количество теплоты, которое необходимо отдать этому газу и температуру t2, при которых давление повысилось до Р2=(1,4+0,1·n), МПа. Теплоемкость считать постоянной.
Рекомендации: для определения необходимого значения температуры использовать
соответствующее уравнение процесса (4.1, табл. 4.1), плотность ρ1
определить по удельному объему υ1=1/ ρ1,
который найти по уравнению состояния (4.7), массу газа найти через плотность и
объем сосуда ![]() . Необходимая теплота находится по
(4.5 и 4.10), где изохорная теплоемкость находится из зависимости (2.2) и табл.
2.1.
. Необходимая теплота находится по
(4.5 и 4.10), где изохорная теплоемкость находится из зависимости (2.2) и табл.
2.1.
Задача № 4.4
Определить давление Р1=Р2, плотности ρ1, ρ2 и объем V2 углекислого газа массой m = 3 кг, находящегося в баллоне объемом:
а) V1 = 1,5 м3; б) V1 = 2,5 м3; в) V1 = 3,5 МПа.
если его температура увеличилась с t1 = 0 оС до t2 = (50+10·n).
Рекомендации: плотность ρ1 находятся заданным значениям m и V1, ρ2 - по уравнениям процесса (4.1, 4.8), давление – по уравнению состояния (4.7), объем V2 по (4.9). Молекулярная масса углекислого газа рассчитывается по значениям молекулярных масс его составляющих.
Задача № 4.5
Рассчитать, при какой температуре наружного воздуха в
кислородном баллоне объемом 40 л возникает допустимое (критическое по прочности
баллона) давление Р2 = 240 ат, если первоначальная
температура внешнего воздуха составляет ![]() ,
а масса кислорода в баллоне составляет
,
а масса кислорода в баллоне составляет
а) m=9 кг; б) m=11 кг; В) m=13 кг.
Рекомендации: определить первоначальное давление Р1 по уравнению состояния (4.7) и затем по уравнению процесса (4.1) найти необходимую температуру.
Задача № 4.6
Определить температуру воздуха после адиабатического сжатия в компрессоре до давления Р2=(700+100·n), кПа, температура и давление воздуха перед сжатием равны
а) Р2=770 мм рт. ст., t1 = 20 оС;
б) Р2=4 ат, t1 = 60 оС;
в) Р2=8 ат, t1 = 100 оС.
Найти совершенную работу сжатия.
Объемный состав воздуха: кислород - 19 %, азот - 78 %, углекислый газ - 2 %.
Рекомендации: параметры состояния до и после сжатия
находятся по уравнению (4.7), а также по уравнению процесса (4.1). Показатель
адиабаты определяется по зависимости 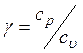 , молекулярная
масса и теплоемкость воздуха определяются по (2.13) и (2.14). Работа сжатия
находится по (4.6).
, молекулярная
масса и теплоемкость воздуха определяются по (2.13) и (2.14). Работа сжатия
находится по (4.6).
Тема 5. Реальные газы
5.1. Водяной пар
Насыщенный водяной пар – пар, получаемый при кипении воды при постоянной температуре (температуре насыщения).
Для определения характеристик насыщенного пара используют таблицы воды и водяного пара, в которых приводятся данные в зависимости только от температуры или давления (табл. 5.1 и 5.2).
Теплота, передаваемая при нагреве воды
![]() , кДж, (5.1)
, кДж, (5.1)
где энтальпия воды ![]() , кДж/кг.
, кДж/кг.
Теплота, передаваемая при парообразовании
![]() , кДж, (5.2)
, кДж, (5.2)
где m, V – масса (кг) и объем (м3) воды; ρ’ – плотность воды, кг/м3; r – теплота парообразования, кДж/кг; с’р – средняя изобарная теплоемкость воды, кДж/(кгּК).
Тепловая мощность находится из
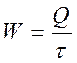 , кВт, (5.3)
, кВт, (5.3)
где τ – время, с.
Объемный расход среды определяется через скорость ее движения U (м/с) и площадь поперечного сечения канала S (м2)
Gυ=U·S, м3/с. (5.4)
Массовый расход среды находится из
Gm= Gυ · ρ, кг/с. (5.5)
Таблица 5.1
Физические свойства водяного пара на линии насыщения
(по температурам)
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.