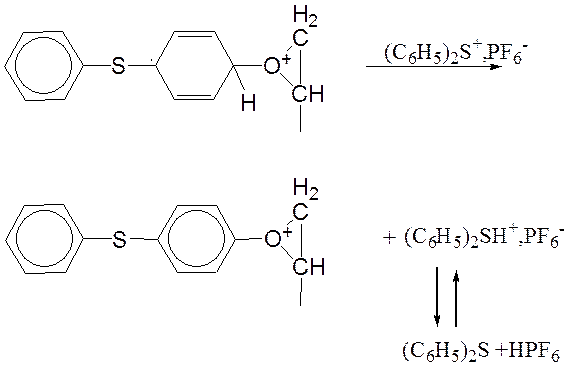
Протонна кислота ініціює подальший процес полімеризації. Арилсульфонієві солі виявилися дуже ефективними фотоініціаторами (високий квантовий вихід і термічна стабільність), у порівнянні з іншими ініціюючими системами. Фотоліз відбувається швидко навіть при Х= 300 нм за малої кількості поглинутого цими солями світла. Цей факт підтверджується тим, що фотохімічне розщеплення зв'язку C-S в триарилсульфонієвих солях спостерігається в області УФ-спектра, практично не придатному для фотолізу таких сполук [18].
Пошуки більш активних фотоініціаторів привели до синтезу ряду триарилсульфонієвих солей (ТАС) професором Крівелло [16] загальної формули:
![]()
де
![]()
Механізм фотолізу триарилсульфоніевих солей, описано в роботах [18]. Цей процес можна зобразити наступною схемою:
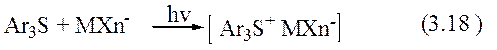 |
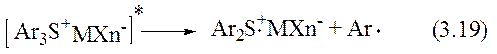 |
3) утворення кислоти Бренстеда та йон-радикала внаслідок відриву водню від молекули реагенту, або розчинника
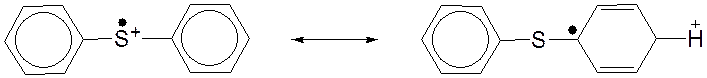
В доповнення до запропонованого механізму ініціювання катіонної полімеризації протонними кислотами Ледвіс встановив можливість прямої електрофільної атаки діарилсульфонієвого катіон-радикалу на мономер [16]:
Раніше було встановлено, що ефективними каталізаторами полімеризації e-капролактону (КЛ) та оксирану, є комплексні сполуки галогенідів Fe (КС) загальної формули R4N+FeCl4- і R4P+FeCl4- [19, 20]. Було показано, що дисоціюючи в среді лактону, КС утворює активні комплекси з мономером типу [FeCl2+ … КЛ … FeCl4- ], які при підвищених температурах перетворюються в активні центри- карбоксонійіони. Константи швидкостей таких реакцій складає ~ 10-5 л2/моль2с. При досліджені процесу було помічено, що відтворюваність відсутня, якщо реакційна суміш тривалий час знаходилась на світлі. Освітлення сонячним світлом вихідної суміші призводило до збільшення швидкості реакції в декілька разів.
В роботі [20] кінетичні данні по зміненню ММ полімерів показали, що продукти дисоціації КС в середовищі КЛ підлягають хімічним перетворенням по схемі:
2R4N+FeCl4« 2R4NCl + [FeCl2+FeCl4-]
¯
[FeCl2+FeCl3-] + Cl· (3.21)
¯
[FeCl+FeCL4-]
Зі схеми ( 21 ) видно, що під дією квантів світла в сполуках, що містять хлорне залізо, протікають окисно- відновлювані процеси перетворення Fe3+ в Fe2+ і виділення радикалу хлору.
Таким чином, в реакційній суміші спочатку опромінення присутні іони двох типів Fe3+ та Fe2+ , але при довготривалому експонуванні, згідно зі схемою, всі іони Fe3+ перетворюються в Fe2+. Цей висновок зроблен на основі УФ- спектрального аналізу вихідних сумішей до опромінення і в процесі опромінення.
За допомогою ренгенструктурного аналізу було показано, що надана сіль має будову R4P+H+FeCl42-, відкіля видно, що кристалічна решітка солі містить протон, який захоплюється із розчинника в процесі її синтеза. Очевидно, що така протоновмісна сіль забезпечує кислотний каталіз полімеризації гетеро циклу, що заключається в протонуванні лакторнного циклу. Як було експериментально встановлено, кислотний каталіз сіллю Fe2+ знижує енергію активації роззкриття лактонного циклу до 67 кДж/мольу порівнянні зі 125 кДж/моль для солей Fe3+ , що не включають протону в кристалічній решітці. Зниження активаційного бар’єру приблизно в 2 рази призводить до швидкої реакції на стадії ініціювання і, як висновок, до зниження S- подібності в кінетичних кривих, як це було встановлено на модельних реакціях [20].
Питання про використання ЕФУ як модіфікатора з метою розширення області застосування як структуроутворювача викликає особливий інтерес для дослідника. Для створення матеріалів з комплексом заданих властивостей потрібно дослідження взаємозв’язку між складом композиції, закономірностями формування тримірних покриттів, їх структурою та властивостями отверднених покриттів.
На основі аналітичного огляду робимо висновок про те, що в композиції разом з ЕФУ можуть бути використовані різні матеріали з різноманітними функціональними групами, які викликають не однаковий вплив на властивості покриттів.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.