Несмотря на то, что фосфоролиз гликогена, катализируемый гликоген-фосфорилазой легко обратим (∆ G0’= – 2,1 кДж / моль), синтез гликогена invivo происходит другим путем. Распад и синтез гликогена как пример сложного каскадного механизма регуляции с участием гормонов будут рассмотрены ниже. Общий принцип биосинтеза олиго- и полимерных сахаров (образование гликозидных связей) заключается в том, что донором глюкозильной группы является активированная форма глюкозы (или галактозы) – нуклеозиддифосфатглюкоза, синтез UDP-глюкозы представлен ниже.
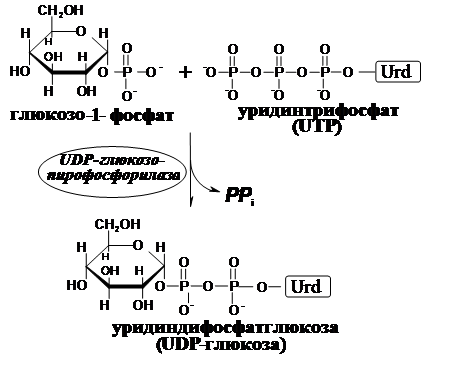 |
Сахароза синтезируется путем переноса глюкозы от
UDP-глюкозы на фруктозу, а лактоза переносом галактозы от UDP-галактозы на глюкозу:
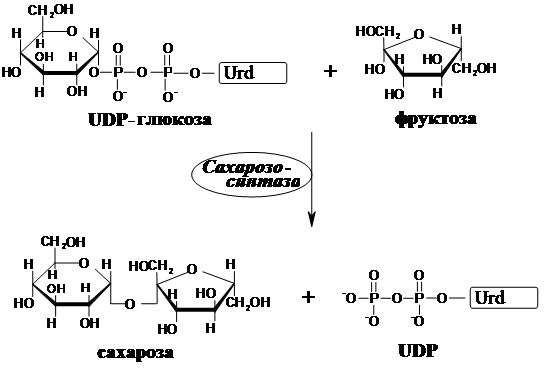 |
Представляют интерес взаимопревращения моносахаридов на уровне производных UDP. UDP-галактоза образуется из глюкозы – конфигурация ОН-группы у С-4 инвертируется UDP-глюкозо-4-эпимеразой, содержащей NAD+:
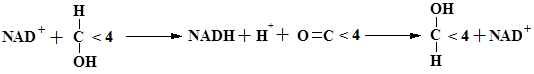
Биосинтез α-(1→4)-глюканов гликогена и амилозы, протекает по реакции, представленной ниже для гликогена (для синтеза амилозы крахмала) используется активированный мономер – АDP-глюкоза:
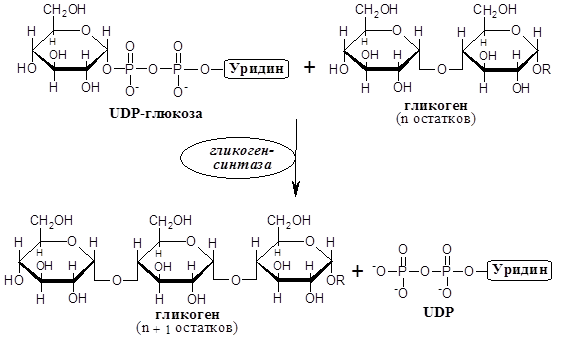
Синтез жирных кислот в цитозоле осуществляется реакциями, отличными от реакций их окисления, и начинается с карбоксилирования ацетил-СоА. Эта необратимая реакция является решающим этапом в синтезе жирных кислот. Синтез малонил-СоА катализируется ацетил-СоА-карбоксилазой, содержащей простетическую группу – биотин, и протекает в две стадии, в каждой из которых участвует одна из трех специфических субъединиц фермента.
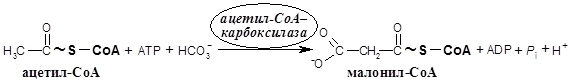
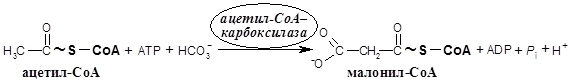 Суммарная
реакции карбоксилирования:
Суммарная
реакции карбоксилирования:
Строение ацетил-CoA–карбоксилазы представлено в таблице.
|
Первая субъединица |
Вторая субъединица |
Третья субъединица |
|
Карбоксибиотин- переносящий белок |
Биотин-карбоксилаза |
Транскарбоксилаза |
1. Карбоксилирование биотина
 |
Биотин–фермент + АТP + HCO3_ ![]() CO2 ~
Биотин–фермент + ADP + Pi .
CO2 ~
Биотин–фермент + ADP + Pi .
2. Перенос активированного СO2 на ацетил-CoA:
CO2 ~ Биотин–фермент + Ацетил-CoA ![]() Малонил-CoA + Биотин–фермент.
Малонил-CoA + Биотин–фермент.
Промежуточные продукты синтеза жирных кислот присоединены к ацилпереносящему белку (АСР, Acyl Carrier Protein). Фосфопанетеиновая группа, присоединенная в СоА к 3’,5’-аденозиндифосфату, связана с остатком Ser полипептидной цепи АСР (77 остатков), из-за чего последний можно рассматривать как гигантскую простетическую группу, «макроСоА».
Ферментная система, катализирующая синтез насыщенных жирных кислот из ацетил-СоА, малонил-СоА и NADPH, называется синтазой жирных кислот.
Цикл элонгации в синтезе жирных кислот начинается с образования ацетил-АСР и малонил-АСР:

Ацетил-CoA + АСР ![]() Ацетил-АСР
+ CoA,
Ацетил-АСР
+ CoA,
Малонил-CoA + АСР ![]() Малонил-АСР
+ CoA.
Малонил-АСР
+ CoA.
Далее цикл элонгации включает четыре последовательных реакции: конденсацию, 1-е восстановление, дегидратацию и 2-е восстановление. Восстановителем является NADPH. Образовавшийся в результате первого цикла бутирил-АСР вступает во второй цикл элонгации, начинающийся с присоединения двухуглеродного фрагмента из малонил-АСР. Для синтеза пальмитата необходимо семь циклов элонгации.
Биоэнергетический баланс синтеза пальмитата преставлен уравнением (с учетом синтеза малонил-СоА):
8 Ацетил-CoA + 7ATP + 14NADPH → Пальмитат + 14NADP+ + 8CoA + 6H2O + 7ADP + 7Pi.
У высших организмов ферменты – компоненты синтазы жирных кислот, организованы в мультиферментный комплекс. Организованная структура ферментов повышает общую эффективность процесса благодаря прямому переносу промежуточных соединений от одного фермента к другому, осуществляемому «вращающейся рукой» – гибкой и максимально длинной (2 нм) группой фосфопантетеина АСР.
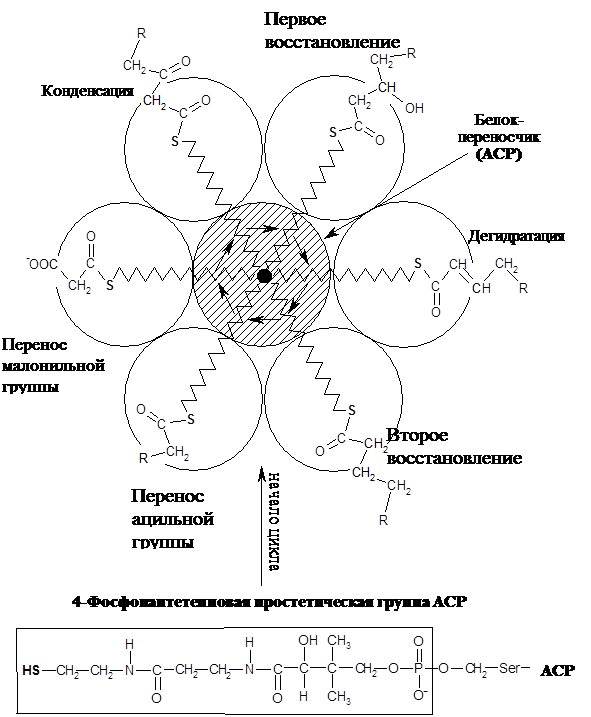
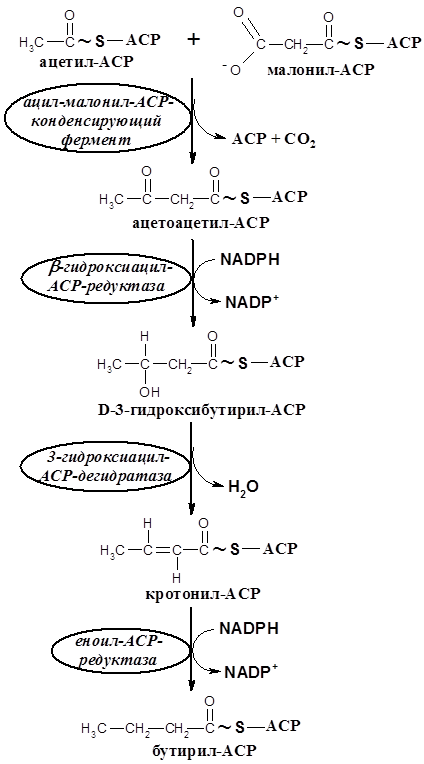
Биосинтез сложных липидов – нейтральных жиров и фосфолипидов (см. реакции на с. 102).Ацил-СоА является главным предшественником липидов и стероидов (холестерола). Фосфатидная кислота – общий промежуточный продукт синтеза липидов, образуется последовательным ацилированием глицерол-3-фосфата за счет ацил-СоА (активированных жирных кислот). Реакция катализируется глицерол-фосфат ацилтрансферазой. Гидролиз ее фосфорной группы фосфатидат фосфатазой и последующее ацилирование (1,2-диацилглицерол-О-ацилтрансферазой, триацилглицерол синтазой) приводят к образованию триацилглицерола.
Биосинтез фосфолипидов – главных компонентов клеточных мембран, может идти двумя путями. Взаимодействие фосфатидной кислоты с CТР, катализируемое фосфатидат цитидилилтрансферазой, дает активированный промежуточный продукт – CDP-диацилглицерол. Затем активированный фосфатидильный остаток переносится на гидроксильную группу какого-нибудь полярного спирта, например серина, и образуется фосфатидилсерин (кефалин), реакция катализируется фосфатидилсерин синтазой. Фосфолипид, например фосфатидилхолин (лецитин), может быть получен с использованием активированного промежуточного продукта этого пути –
CDP-холина, который получается в две стадии: сначала холин фосфорилируется с помощью АТР с образованием фосфорилхолина (фермент – холин фосфотрансфераза), который затем реагирует с СТР и образует CDP-холин (холинфосфат цитидилилтрансфераза). Остаток фосфорилхолина этой молекулы переносится фосфатидилхолин синтазой на диацилглицерол, образуя фосфатидилхолин. Лецитин может быть получен из кефалина, фосфатидилсерина, декарбоксилированием с образованием другого кефалина – фосфатидилэтаноламина, трехкратное метилирование которого S-аденозилметионином дает фосфатидилхолин.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.