![]()
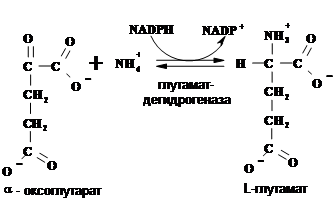
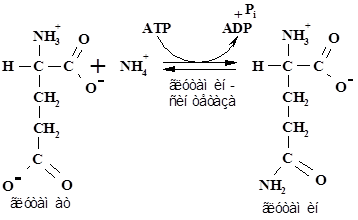
Затем соли аммония используются высшими организмами для синтеза аминокислот (нуклеотидов и др.). Основными «пунктами входа» аммония в промежуточный метаболизм являются Gln, Glu и карбамоилфосфат:
|
Аминокислоты делятся на заменимые, которые способен синтезировать человек, и незаменимые, которые обязательно должны поступать с пищей (см. ниже).
|
Заменимые |
Незаменимые |
Заменимые |
Незаменимые |
|
Аланин |
Аргинин |
Глутамин |
Лизин |
|
Аспарагин |
Валин |
Пролин |
Метионин |
|
Аспартат |
Гистидин |
Серин |
Треонин |
|
Глицин |
Изолейцин |
Тирозин |
Триптофан |
|
Глутамат |
Лейцин |
Цистеин |
Фенилаланин |
Углеродный скелет аминокислот происходит из промежуточных продуктов гликолиза, пентозофосфатного пути и цикла трикарбоновых кислот. Существует шесть биосинтетических семейств аминокислот, представленных на схеме, где в квадрате – основные метаболические предшественники, в овале – аминокислоты, из которых образуются другие аминокислоты, звездочками отмечены незаменимые аминокислоты:
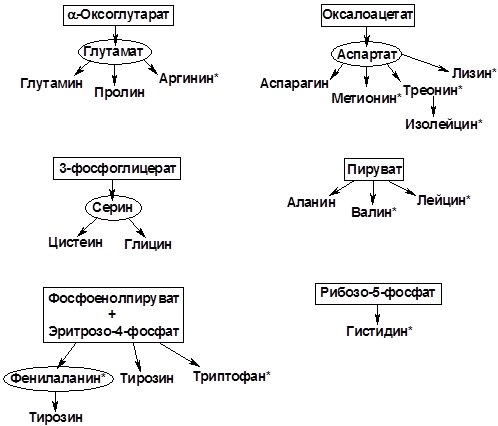
Пути биосинтеза заменимых аминокислот просты. Так, Asp и Ala получаются в одну стадию переаминированием оксалоацетата и пирувата соответственно (реакции см. на стр.78).
Asn и Gln синтезируются в одну стадию амидированием Asp и Glu (донором азота у млекопитающих при синтезе Asn является Gln), ферментами, катализирующими эти реакции, являются аспарагин и глутамин синтетазы соответственно:
Asp +Gln + ATP → Asn +AMP + PPi +Glu,
Glu +NH4+ + ATP → Gln + ADP + Pi + H+.
Пролин синтезируется из глутамата в три стадии:
г-карбоксильная группа Glu при взаимодействии с АТР и NADPH восстанавливается до альдегида, спонтанная циклизация с отщеплением воды и последующее восстановление, катализируемое пролиноксидазой (пролин дегидрогеназа, пирролин-5-карбоксилат редуктаза) дает пролин:
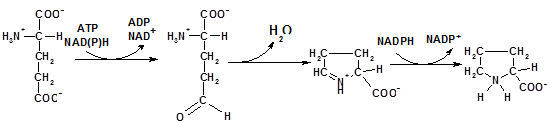
|
|||
|
|||
глутамат пролин
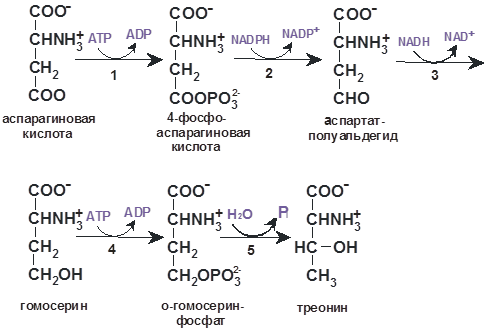
Пути биосинтеза незаменимых аминокислот гораздо сложнее, чем заменимых. В качестве примера представлен несложный биосинтез Thr – незаменимой аминокислоты, из Asp:
|
|
|
L-аспартат- β-полуальдегид:NADР+ оксидоредуктазой (фосфорилирующей) (2) и L-гомосерин: NAD+ оксидоредуктазой (3) приводит к образованию гомосерина. В результате последующего фосфорилирования гомосерина АТР:L-гомосерин-О-фосфотрансферазой (4) и гидролиза гомосеринфосфата О-фосфогомосерин фосфолиазой (5) образуется L-треонин.
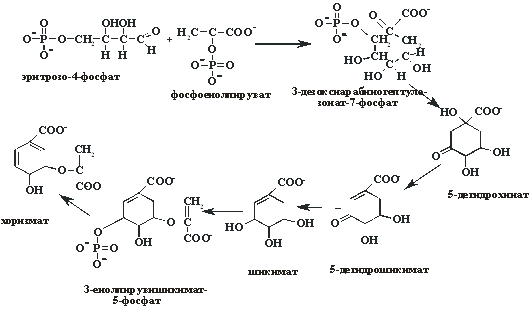
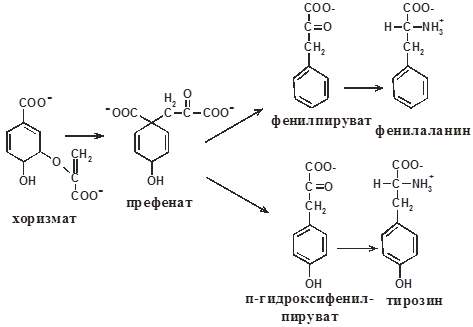
Синтез ароматических аминокислот (Phe, Tyr и Trp) идет по общему пути из фосфоенолпирувата и эритрозо-4-фосфата через образование шикимата и хоризмата. Ниже представлены схемы пути синтеза ароматических аминокислот и реакции синтезов Phe и Tyr:
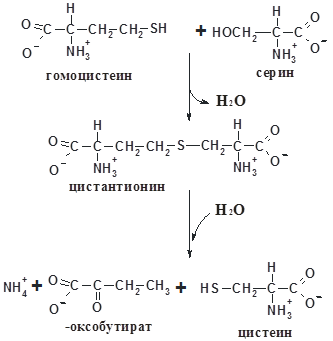
Представляет интерес превращение Met в Cys через гомоцистеин, образующийся в цикле активированной метильной группы, основным донором которой является
S-аденозилметионин:
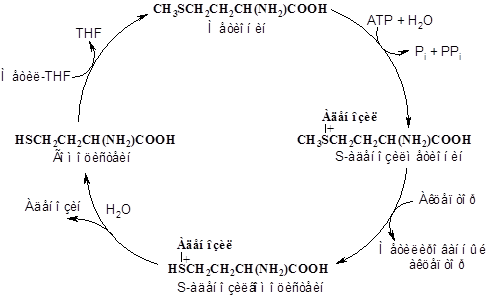
Цистеин синтезируется из серина и гомоцистеина:
|
|
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.