5-аминоимидазолрибонуклеотида (реакции 6–10). Достройка трех недостающих атомов кольца начинается с карбоксилирования (6), затем аминогруппа Asp реагирует с карбоксильной группой рибонуклеотид 5-аминоимидазол-4-карбоновой кислотой с образованием амидной связи (7). В следующей (8) реакции углеродный скелет остатка Asp отщепляется в виде фумарата. Последний углеродный атом пуринового кольца происходит из N10-формилтетрагидрофолата(9). Дегидратация рибонуклеотид-5-формамидоимидазол-4-карбоксамида и замыкание кольца дает пуриновое основание гипоксантин в образующемся нуклеотиде – инозинате (IMP). Реакции второго этапа катализируют следующие ферменты: 6 – 5-аминоимидазолрибонуклеотид карбоксилаза; 7 –
5-аминоимидазол-4-N-сукцинокарбоксамидрибонуклетид синтетаза; 8 – 5-аминоимидазол-4-N-сукцинокарбоксамид рибонуклеотид лиаза; 9 – 5-аминоимидазол-4-карбоксамидрибонуклеотид трансформилаза; 10 – инозиниказа (IMP-циклогидролаза).
Ниже представлен рисунок пуринового кольца с указанием происхождения его атомов:
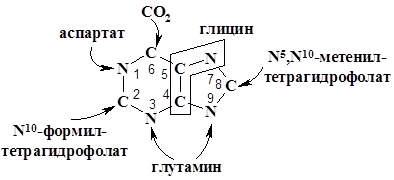
Основные пуриновые нуклеотиды, АМР и GМР, образуются из IMP.
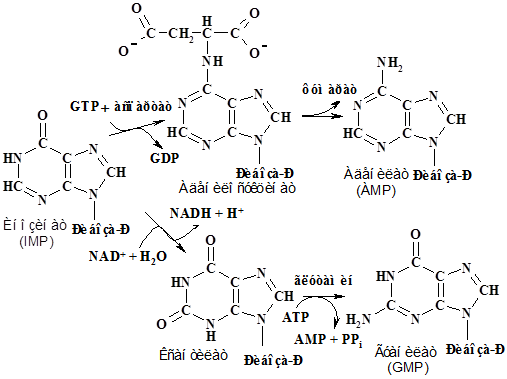
Аденилат синтезируется из инозината введением по положению С-6 аминогруппы вместо карбонильного кислорода в две стадии: вначале присоединется Asp, реакция катализируется аденилсукцинат синтетазой, затем удаляется фумарат аденилсукциназой. Гуанилат синтезируется из инозината также в две стадии: сначала он окисляется до ксантилата дегидрогеназой инозиновой кислоты, а затем вводится аминогруппа в положение
С-2 из Gln синтетазой гуаниловой кислоты:
Синтез пиримидиновых нуклеотидов. В отличие от пути синтеза пуриновых нуклеотидов de novo, пиримидиновое кольцо сначала собирается, а затем присоединяется к рибозофосфату, донором которого служит также PRibPP.
Биосинтез кольца пиримидинового основания начинается с образования карбамоилфосфата, синтез которого, в отличие от синтеза его в цикле мочевины, протекает в цитозоле, катализирует это процесс другая карбамоилфосфат синтаза и донором азота служит Gln ( а не ион аммония):
Gln + 2АТР + НСО3- → Карбамоилфосфат +2ADP + Pi +Glu.
Решающая стадия биосинтеза пиримидинов – образование
N-карбамоиласпартата:
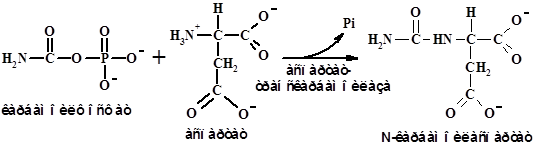
На следующей стадии после дегидратации и циклизации образуется дигидрооротат, который в результате окисления
FMN-зависимой дегидрогеназой превращается в оротат. Присоединение к оротату PRPP и последующее декарбоксилирование приводит к образованию уридилата (UMP):
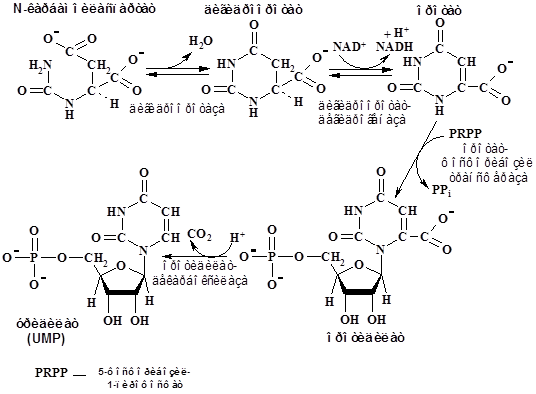
Нуклеотиды в биосинтетических реакциях и как коферменты участвуют в активной форме – дифосфатов и трифосфатов. Нуклеозидмоно-, ди- и три фосфаты способны к взаимопревращениям:

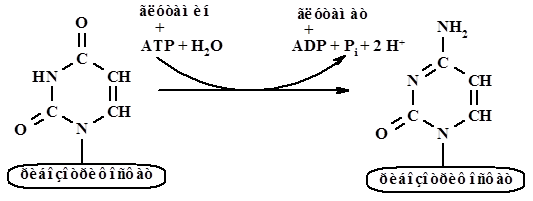
Цитидинтрифосфат, СТР, образуется из уридинтрифосфата, реакция катализируется цитидинтрифрсфат синтазой – СТР-синтаза:
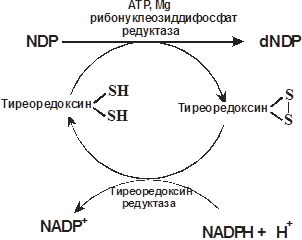
Дезоксирибонуклеотиды получаются восстановлением рибонуклеозиддифосфатов. Донорами электронов и протонов в рибонуклеотид редуктазе (рибонуклеозиддифосфат редуктазе) являются два цистеиновых остатка белка – тиоредоксина. Образующийся дисульфид белка восстанавливается тиоредоксин редуктазой, коферментом которой является NADPH.
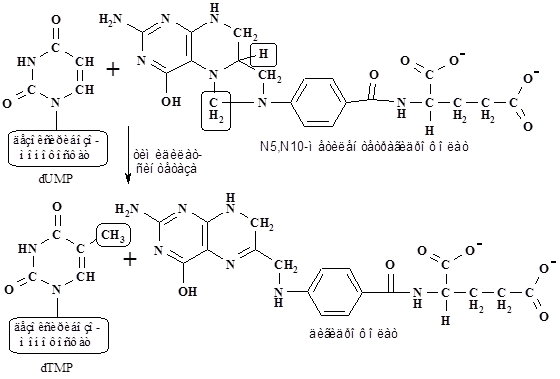
Дезоксириботимидилат образуется метилированием дезоксирибоуридилата. Коферментом тимидилат синтетазы, донором метильной группы и электронов, в этой реакции является N5,N10-метилентетрагидрофолат, который превращается в дигидрофолат (см. схему на с. 111 и реакцию на с. 112).
![]() Тиоредоксин–(SH)2
+ NDP Тиоредоксин–S2 + dNDP
Тиоредоксин–(SH)2
+ NDP Тиоредоксин–S2 + dNDP
![]() Тиоредоксин–S2 + NADPH + H+ Тиоредоксин–(SH)2
+ NADP+
Тиоредоксин–S2 + NADPH + H+ Тиоредоксин–(SH)2
+ NADP+
Тетрагидрофолат регенерируется восстановлением:
|
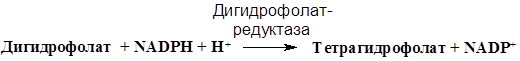
|
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.