Каким же образом координируется сложная сеть рассмотренных выше процессов, чтобы организм был обеспечен всем необходимым для жизни? Координация обеспечивается интеграцией и одновременно контролем метаболизма.
Основная цель метаболизма – это генерирование АТР, NADPH и строительных блоков для биосинтетических реакций.
Из рассмотренного выше материала видно, что общим принципом организации и координации процессов метаболизма являются цепи и циклы. На схеме, приведенной на с. 119, представлена цепь гликолиза и цикл трикарбоновых кислот, а также связь последнего с циклом мочевины.
Рассмотрим основные метаболические пути и их регуляторные стадии.
Необратимые стадии любого метаболического процесса определяют необратимость пути процесса, а ферменты, катализирующие эти стадии, регулируют весь процесс. Для гликолиза эти вопросы обсуждены в гл. 3, разд. 3.1. («Гликолиз»).
Лимитирующей реакцией цикла Кребса является синтез цитрата из оксалоацетата и ацетил-СоА. АТР – аллостерический ингибитор цитрат синтазы. Кроме того, реакции, катализируемые изоцитрат дегидрогеназой и α-оксоглутарат дегидрогеназой, – также регуляторные стадии ЦТК. Первый фермент стимулируется ADP и ингибируется NADH. Второй фермент ингибируется продуктами реакции – сукцинил-СоА и NADH и высоким энергетическим зарядом. Иначе говоря, и поступление двухуглеродных фрагментов в ЦТК, и скорость цикла снижаются при высоком содержании АТР в клетке.

К вспомогательным компонентам гликолиза относятся коферменты – АDP, NAD+, первый из них регенерируется при взаимопревращениях нуклеозидмоно-, ди- и трифосфатов, а второй – в цепи переноса электронов.
Из приведенной интеграционной схемы некоторых метаболических путей видно, что есть точки разветвления, на перекрестках которых находятся ключевые промежуточные продукты – глюкозо-6-фосфат, пируват, ацетил-СоА, которые связывают многие процессы между собой: гликолиз и глюконеогенез, пентозофосфатный путь, цикл мочевины, синтез и распад жирных кислот, расщепление и синтез углеродного скелета аминокислот, биосинтез нуклеотидов, жиров, фосфолипидов и холестерола (см. схемы на сс. 119 и 120).
Из схемы видны пути синтеза компонентов ЦТК – анаплеротические реакции, некоторые из них были рассмотрены раньше и будут проанализированы ниже.
Примером еще одного цикла взаимопревращения глюкозы и лактата является цикл Кори.
Лактат, образованный сокращающейся мышцей из пирувата вследствие высокого значения отношения [NADH] / [NAD+], диффундирует в кровь и переносится в печень, где вследствие низкого отношения [NADH] / [NAD+] превращается в пируват, из которого по пути глюконеогенеза образуется глюкоза. Таким образом печень снабжает глюкозой сокращающиеся мышцы, получающие АТР в результате гликолитического превращения глюкозы в лактат:
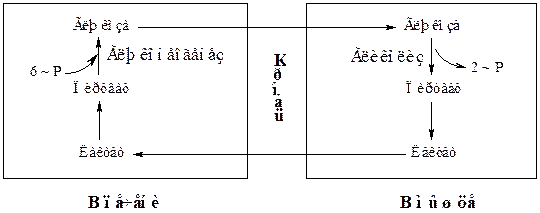 |
Важный общий принцип метаболизма состоит в следующем: пути биосинтеза и распада почти всегда разобщены. Это разобщение способствует регуляции метаболизма. У эукариот возможности метаболической регуляции и ее гибкость усиливаются благодаря наличию компартмента (компартментализация) (см. схему на с. 122).
Так судьба жирных кислот определяется тем, где они находятся – в цитозоле или в митохондриях. Это позволяет регулировать их поток через внутреннюю митохондриальную мембрану. Жирные кислоты в цитозоле, где они синтезируются, могут этерифицироваться, выделяться во внеклеточное пространство или переноситься внутрь митохондриального матрикса в виде эфиров карнитина, где они быстро расщепляются.
Наглядным примером компартментации является синтез карбамоилфосфата в цикле мочевины и при синтезе пиримидинов, что обсуждалось выше (гл. 4, разд 4.3., «Синтез пиримидиновых нуклеотидов»).
 |
Мультиферментные комплексы представляют собой примеры совершенной организации систем биохимических реакций: пируватдегидрогеназный и α-оксоглутаратдегидрогеназный комплексы, полиферментный комплекс синтеза жирных кислот. Структурное объединение ферментов-участников делает возможным координированный катализ при осуществлении многостадийного процесса. Компактность расположения ферментов увеличивает суммарную скорость процесса и сводит к минимуму побочные реакции. И, как правило, присутствует молекулярный рычаг для переноса активированных промежуточных продуктов от одного активного центра к другому.
Даже в простейшей бактериальной клетке протекает более тысячи взаимозависимых реакций. Эта сложная система требует строгой регуляции. Исследование широкого круга организмов показало, что существует много различных механизмов регуляции. Функции организма могут регулироваться посредством реакций, протекающих в клетке – метаболическая регуляция (регуляция активности ферментов), а также на уровне всего организма – гормональный и нервный контроль.
Принципиально важная особенность метаболических путей заключается в том, что их скорость определяется активностью ключевых ферментов, катализирующих лимитирующие (решающие) реакции процесса. Регуляция этих ферментов, различные типы которой будут рассмотрены ниже, и их концентрация являются определяющими тактику координации метаболизма.
Кроме того, биосинтез и расщепление органических молекул клетки почти всегда осуществляются различными путями и происходят в разных компартментах клетки.
Стехиометрическая регуляция в точках разветвления определяется соотношением концентраций компонентов. Так, если есть избыток АТР и глюкозо-6-фосфата, из последнего образуется гликоген. Если же АТР и углеродные скелеты молекул расходуются на биосинтетические реакции, глюкозо-6-фосфат вступает в реакции гликолиза. Взаимопревращение глицеральдегид-3-фосфата и дигидроксиацетонфосфата определяется соотношением
[NAD+] / NADH.
Во многих биосинтетических процессах имеет место ингибирование первой реакции конечным продуктом процесса. Эта регуляция называется ингибированием по принципу обратной связи, или ретроингибированием. Так, образовавший пальмитоил-СоА ингибирует ацетил-СоА-карбоксилазу – фермент, катализирующий первую реакцию цикла биосинтеза жирных кислот.
AMP и GMP являются ретроингибиторами ферментов четырех стадий биосинтеза пуриновых нуклеотидов: 5-фосфорибозил-1-пирофосфат синтетазы (AMP, GMP и IMP); α-5-фосфорибозил-1-пирофосфат аминотрансферазы (AMP и GMP) (лимитирующая реакция); аденилатсукциназы (АМР) и дегидрогеназы инозиновой кислоты (GMP). Две реакции биосинтеза пиримидиновых нуклеотидов также ингибируются по принципу обратной связи: лимитирующая стадия, катализируемая аспартат карбамоил трансферазой ингибируется СТР, а карбамоилфосфат синтаза ингибируется другим продуктом – UMP.
Многие метаболические реакции регулируются энергетическим
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.