технологии пластмасс Факультет VI
Курс 4
Группа 494
Химия и физика высокомолекулярных соединений
Лабораторная работа по теме:
Химический анализ стирола бромид-броматным методом
Студент: Шамордина Н. В.
Руководители: Ржехина Е. К.
Каркозов В.Г.
Санкт-Петербург
2002
Химический метод анализа стирола (Ст), основан на реакции по винильной группе, т.к. двойная связь, входящая в неё способна присоединять бром, выделяющийся при подкислении бромид-броматной смеси:
![]() KBr + KBrO3 6KCl + 3H2O +
3Br2
KBr + KBrO3 6KCl + 3H2O +
3Br2
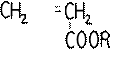
![]() +
+
![]() Br2
Br
Br2
Br
Избыток брома выделяет при добавлении йодистого калия эквивалентное количество йода, который мы оттитровывали раствором тиосульфата натрия:
![]() 2KI
+ Br2 2KBr + I2
2KI
+ Br2 2KBr + I2
![]() I2 + 2Na2S2O3 2NaI
+ Na2S4O6
I2 + 2Na2S2O3 2NaI
+ Na2S4O6
Из приведённых реакций следует, что на 1 моль мономера расходуется 2 моль Na2S2O3 и, следовательно, 1 мл 0,1 н. раствора Na2S2O3 расходуется на K граммов эфира:
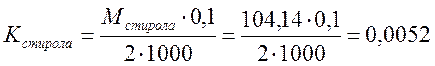
Реактивы
KBr – KbrO3, 0,1 н. раствор
Уксусная кислота, 50%-ная
HCl, ρ = 1,19
KI, 10%-ный раствор
Na2S2O3, 0,1 н. раствор
Крахмал, 1% раствор
Приборы
Колба мерная ёмкостью 100 мл
Колбы конические с пришлифованными пробками ёмкостью 500 мл
Пипетки ёмкостью 10 мл
Мерные цилиндры ёмкостью 10 мл
Бюретка ёмкостью 25 мл
Ход определения: В мерную колбу, содержащую 10 – 15 мл уксусной кислоты и взвешенную с точностью до 0,0002 г, отвешивают около 2 г мономера с точностью до 0,0002 г и добавляют уксусную кислоту до метки. В коническую колбу наливают 50 мл раствора бромид-бромата калия, 10 мл тщательно перемешанного раствора мономера (пипеткой) 10 мл соляной кислоты (цилиндром), закрывают колбу пробкой, перемешивают содержимое и выдерживают 20 мин на рассеянном свету. Затем вводят 10 мл раствора KI (цилиндром) и титруют выделившейся йод раствором Na2S2O3, добавляя в конце титрования крахмал.
Анализируют две пробы. Параллельно проводят контрольный опыт, вводя в колбу вместо раствора мономера 10 мл уксусной кислоты. Из полученных результатов принимают среднее значение.
Содержание эфира X (в %) рассчитывают по формуле:
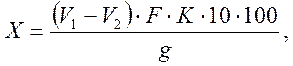 |
где: V1
– объём 0,1 н. раствора ![]() Na2S2O3,
израсходованного на титрование контрольной
Na2S2O3,
израсходованного на титрование контрольной
пробы, мл;
V2 – объём 0,1 н. раствора Na2S2O3, израсходованного на титрование рабочей пробы,
мл;
F – поправочный коэффициент 0,1 н. раствора Na2S2O3;
K – количество эфира, соответствующее 1 мл точно 0,1 н. раствора Na2S2O3, г;
g – навеска эфира, г.
В качестве значения выберем среднее арифметическое между двумя испытаниями.
![]() В
результате имеем: Xстирола=
В
результате имеем: Xстирола=
Санкт-Петербургский государственный технологический институт
(технический университет)
Кафедра химической
технологии пластмасс Факультет VI
Курс 4
Группа 494
Химия и физика высокомолекулярных соединений
Лабораторная работа по теме:
Дилатометрический метод изучения кинетики полимеризации
Студент: Шамордина Н. В.
Руководители: Ржехина Е. К.
Каркозов В.Г.
Санкт-Петербург
2002
Проведение синтеза полистирола методом полимеризации в массе
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.