В качестве носителей мы использовали три типа тонкопористых сибунита марок П669, П699, П770, П1454 с разной долей микропор (5-30%). Сибуниты подвергались обработке кислородом, водородом, паром для создания дополнительных функциональных групп, обладающих как Бренстедовскими, так и Льюисовскими кислотными и основными центрами. Использовали их как носители для активных компонентов от монослоя, до несколько монослоев, чтобы сузить поры. Использовали промышленный гамма оксид алюминия, синтезированные шпинели сложного состава, цеолит типа ZSM-5. Необходимые кислотные центры создавали фосфорной, соляной кислотами, их солями, гетерополикислотами, которые сами обладают достаточно узкими порами. Основные центры и окислительно-восстановительные центры создавали введением добавок цинка, магния, стронция, щелочных элементов, лантана, церия, хрома, марганца, никеля, молибдена, вольфрама. Перечисленные элементы являются активными компонентами катализаторов, опубликованных в статьях или патентах. Список приготовленных и испытанных каталитических систем прилагается ниже.
Эксперименты проводили в проточном кварцевом реакторе объемом 5см3 с внутренней термопарой. Температура Т = 200 – 4500С. Расход метанола варьировали в пределах 10 – 2см3/г час жидкого метанола. Лучшие результаты получались при времени контакта ~2с.
Проведены также эксперименты по влиянию различных добавок к метанолу, с помощью которых пытались сместить термодинамическое равновесие: вода, метан, ДМЭ, водород, аргон. Пытались получить дополнительные продукты введением, например, этилена. Эксперименты показали, что реакционная система кинетически чрезвычайно чувствительна к любым добавкам. Они влияли на степень превращения и на распределение продуктов, но только в рамках, благоприятных по термодинамике. Показано, что катализаторы как с основными центрами так и кислотными центрами преимущественно ускоряют реакции синтеза парафинов С1 - С3, водорода и оксидов углерода. При больших степенях превращения увеличивается вклад парового риформинга с образующейся водой: увеличивается выход водорода и оксидов углерода. Существенных результатов по МТО нами не получено.
При конверсии метанола на катализаторе фосформолибденовая гетерополикислота, нанесенная на оксид алюминия, марки А1, при Т= 4000С и времени контакта 2с были получены лучшие результаты по выходу олефинов:
метан - 10 моль%; этан – 12,5; пропан – 2,4; этилен – 5,3; пропилен -3,2; бутен – 2,5; водород 21; СОх -12; ДМЭ -30, остальное – кокс. Эти результаты получаются только на свежем катализаторе, быстро происходит его дезактивация, и далее получаются только парафины, оксиды углерода и водород. В соответствии с термодинамикой. По данным РФА, ИКС и КР гетерополикислота остается без изменений, только появляется углерод, который не выжигается при регенерации. Возможно, он и закрывает доступ к активным центрам внутри полостей ГПК, ведущим синтез олефинов. При больших степенях превращения происходит дополнительная паровая конверсия метанола с образующимся водяным паром, что приводит к увеличению содержания водорода и диоксида углерода в продуктах. Модификация этого катализатора оксидами цинка, церия, иттрия, циркония не приводила к улучшению результатов или же снижала выход олефинов до следовых количеств.
На рис.1 показана зависимость потенциалов Гиббса для разных реакций метанола от температуры, при которой проводились испытания. По термодинамике выход парафинов С1, С2 более выгоден, чем, например этилена. Но когда имеется такой широкий спектр возможных продуктов, все определяет кинетика.
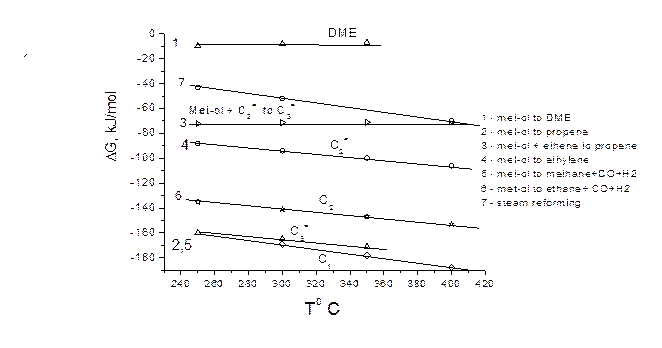
Рис.1
Мы научились, например, превращать метанол в ДМЭ с выходом 98%, например на оксиде алюминия марки А1. В таблице приведен состав газовой смеси при разных температурах на катализаторе кремний вольфрамовая ГПК/Al2O3. Этот катализатор испытывали для получения олефинов, но получили хороший выход ДМЭ. Хотя ДМЭ менее термодинамически выгоден, чем синтез парафинов СОх и водорода, очевидно, что кинетика в данном случае благоприятствует именно ему. Расход метанола 4 мл/час г катализатора. Степень превращения метанола в ДМЭ близка 99%. Оптимальная температура 2800С. Процесс требует регенерации. Катализатор: SiWгпк/Al2O3.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.