Для кристаллических веществ описывают способ их очистки с указанием взятой для перекристаллизации массы вещества и растворителя. Если вещество перекристаллизовывали из смеси растворителей, необходимо указать их соотношение. Обязательно указывают температуру плавления вещества до и после каждой перекристаллизации. Для всех выделенных веществ приводят физические константы, подтверждающие их чистоту в сравнении с соответствующими литературными данными. Можно также привести внешний вид синтезированных веществ, их запах, растворимость (качественно) в важнейших растворителях, устойчивость при хранении.
Если в реакции образуется смесь нескольких соединений, то необходимо стремиться к тому, чтобы выделить и охарактеризовать как можно больше индивидуальных веществ, в том числе не вошедшие в реакцию исходные соединения, как указано выше.
Если несколько соединений синтезировано по общей методике, то можно подробно описать получение только одного вещества, а в дальнейшем ссылаться на этот опыт. Например: «Аналогично опыту 12 из 2.8 г (0.23 моль) анилина и 5.6 г (0.1 моль) акрилонитрила получено…». При такого рода сокращенных описаниях обязательно надо сохранять данные о массовых и молярных количествах реагентов, даже если они совпадают с указанными в типовой методике.
Физические константы, спектральные или аналитические характеристики, а также выходы синтезированных веществ можно обобщать в таблицах или давать в тексте экспериментальной части по форме:
т.пл. 22-23 °С, т.кип. 58 °С (2мм), nD20 1.5156, d20 0.980.
В брутто-формулах соединений первым приводится углерод, затем водород, символы остальных элементов располагаются в алфавитном порядке.
Пример 1. 2-Метил-6-бром-4-хинолинкарбоновая кислота.
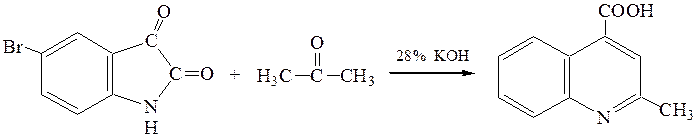
М.м. 226,03 М.м. 58,08 М.м. 266,09
Смесь 8 г (0.035 моль) 5-бромизатина и раствор 16 г (0.28 моль) КОН в 32 мл воды перемешиваем 5 мин при комнатной температуре, добавляем 38.23 мл ацетона и кипятим 8 ч на водяной бане. Реакционную массу нейтрализуем 10%-ной НСl до слабокислой среды (рН 5 – 6), выпавший осадок отфильтровываем, промываем теплой водой и высушиваем. Выход кислоты 12.65 г (93%), т. пл. 259 – 260°С.
Пример 2. 2-Йодтиофен.
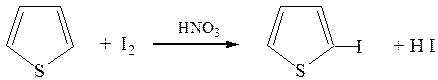
М.м. 84,14 М.м. 253,80 М.м. 210,04
Работа проводится в вытяжном шкафу!
В трехгорлую колбу, снабженную механической мешалкой, водяным холодильником и капельной воронкой, помещают 19 г (0.15 моль) йода, 40 мл этилового спирта.
К полученной суспензии добавляют 21 г (19.3 мл, 0.25 моль) тиофена и медленно прикапывают 14 мл азотной кислоты (d = 1.4), разбавленной равным объемом воды. После прибавления азотной кислоты смесь постепенно нагревают и кипятят 30 мин на водяной бане.
Охлажденную реакционную смесь нейтрализуют 10% NaOH до рН 8, разбавляют водой. Масляный слой отделяют, перегоняют с водяным паром. Тяжелое желтое масло экстрагируют эфиром, промывают 10%-ным раствором тиосульфата натрия, водой и сушат безводным сульфатом натрия. Эфир отгоняют на водяной бане, остаток перегоняют под вакуумом. Выход 2-йодтиофена составляет 23.1 г (44% от теории), т. кип. 73°С / 15 мм рт. ст.
Выводы
В выводах формулируют основные результаты работы.
Библиография
Список литературы, использованной при выполнении курсовой работы, приводится в конце отчета после выводов и оформляется следующим образом.
КНИГИ
1. Пакетт Л. Основы современной химии гетероциклических соединений. М.: Мир, 1971. 352 с.
2. Ингольд К., Робертс Б. Реакции свободнорадикального замещения. М.: Мир, 1974. 255 с.
СБОРНИКИ, СПРАВОЧНИКИ
1. Химия и биологическая активность синтетических и природных … / Под ред. доктора хим. наук В.Г. Карцева и акад. Г.А. Толстикова. Т.1, Т.2. – М.: Иридиум-пресс 2001, Т.1 601с. Т.2 472 с.
ТЕЗИСЫ ДОКЛАДОВ
1. Моисеев И.К., Калиничев А.О., Долгов В.А. // Тезисы докладов XVI Международной научно-технической конференции по химическим реактивам, реагентам и процессам малотоннажной химии. Уфа, 2003 г. С. 17.
2. Подковыров А.И., Баев А.К., Козыркин Б.И. // Тезисы докладов VI Всесоюзной конференции по термодинамике органических соединений. Минск, 1990. С. 73.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.