Эта теория справедлива для некоторых частных случаев, например при
кристаллизации лимонной кислоты ![]() из водных растворов и
ортохлординитробензола из его растворов в эфире. Однако диффузионная теория не
позволяет объяснить особенностей роста кристаллов, например, их огранку плоскостями
или влияние на скорость роста кристаллов органических примесей и не всегда
применима даже для наиболее простого случая – процесса растворения. Также
экспериментально установлено, что для одной и той же соли изменение пересыщения
при различной температуре может по-разному влиять на скорость роста.
из водных растворов и
ортохлординитробензола из его растворов в эфире. Однако диффузионная теория не
позволяет объяснить особенностей роста кристаллов, например, их огранку плоскостями
или влияние на скорость роста кристаллов органических примесей и не всегда
применима даже для наиболее простого случая – процесса растворения. Также
экспериментально установлено, что для одной и той же соли изменение пересыщения
при различной температуре может по-разному влиять на скорость роста.
Молекулярно-кинетическая теория послойного роста рассматривает рост кристаллов как последовательное образование слоев элементарных частиц кристаллизуемого вещества на гранях растущего кристалла. При переходе в этот слой частицы теряют только часть своей энергии и поэтому, подобно газу сохраняют значительную свободу передвижения по поверхности кристалла. Между отдельными частицами в адсорбционном слое возможны неупругие соударения, в результате которых образуются двухмерные кристаллы, присоединяющиеся к кристаллической решетке в виде нового слоя. Процесс наслоения не является непрерывным, а сопровождается паузами, поэтому появление каждого нового слоя на кристалле напоминает процесс возникновения новой фазы. Для образования слоя требуется определенное конечное пересыщение раствора, при котором возникает устойчивый двухмерный зародыш, разрастающийся по всей грани. При росте кристаллов выделяется поверхностная энергия, количество которой зависит от условий присоединения элементарных частиц вещества к грани.
Дальнейший рост двухмерного зародыша происходит путем присоединения к нему целых периферийных рядов – одномерных зародышей. Если оседающий одномерный зародыш не в состоянии заполнить все ребро двухмерного зародыша, на нем образуется трехмерный угол, который является наиболее активным местом растущего кристалла (рис. 41.6).
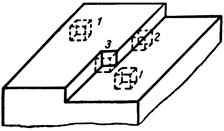
Рисунок 41.6 – Схема роста грани кристалла.
К трехгранным углам (положение 3) из пересыщенного раствора могут непосредственно присоединяться уже отдельные ионы, молекулы или атомы, так как при этом выделяется большее количество энергии, чем в случае, когда частица попадает в двугранный угол (положение 2) или садится на плоскую поверхность (положение 1). Осевшая в трехгранный угол частица уничтожает его, но рядом возникает точно такой же новый, куда и стремится попасть следующая частица и т.д., пока цепочка не дойдет до края кристалла и трехгранный угол не исчезнет. После застройки всей грани на ней возникает следующий зародыш и процесс повторяется.
Эта теория, называемая также теорией идеального роста кристалла в качественных выводах, хорошо подтверждается экспериментальными данными. Однако реальные кристаллы, которые имеют различные дефекты строения, способны расти при значительно меньших переохлаждениях с образованием спиральных фронтов роста на поверхности кристаллов.
В итоге следует отметить, что каждая из теорий имеет недостатки. Так, современные теории объясняют конечные формы кристаллов, исходя только из особенностей их структуры и механизма отложения вещества на гранях без учета свойств среды и ее взаимодействия с растущим кристаллом. Диффузионные теории, наоборот, основное внимание уделяют влиянию среды (скорости подвода вещества к граням) в процессе роста кристаллов, не рассматривая при этом механизма перехода вещества из раствора в кристаллическую решетку. Поэтому в реальном процессе при рассмотрении механизма роста кристаллов приходится полагаться на результаты экспериментальных исследований.
41.5.3. Влияние условий кристаллизации на рост кристаллов и качество продукта
Основной характеристикой кристаллического продукта являются размер и форма кристаллов, фракционный состав, а также химическая чистота. Эти параметры зависят от большого числа факторов: физико-химических свойств компонентов системы, метода и скорости создания пересыщения, перемешивания, наличия примесей, и т.д.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.