Кислород, присутствующий в растворе (насыщенный воздухом – 2,7.10-4М) оказывает существенное влияние на РХВ, поскольку в его отсутствии РХВ почти в 2 раза ниже (8,2 ион\100эВ). Поэтому по мере расходования кислорода РХВ будет уменьшаться. Проявляется это при дозах более 0,8 кГр. К этому моменту расходуется примерно 70 – 80 % кислорода.
При повышении концентрации Fe 2+ и кислорода РХВ несколько возрастает ( до 16 ионов/100 эВ). При концентрациях Fe 2+ менее 10-4М РХВ снижается. Т.е. рабочий диапазон концентраций по железу – от10-4М до 10-2М , а по серной кислоте – от 0,4М до 2,5М.
Влияние температуры
С ростом температуры РХВ несколько увеличивается, но в диапазоне 18 – 30 С – остается постоянным.
Влияние примесей
Органические примеси (спирты, кислоты, фенолы и др.) оказывают значительное влияние на РХВ, как правило в сторону его увеличения. Именно для того, чтобы избежать влияния небольших количеств неконтролируемых примесей органических соединений в систему и вводят хлорид натрия.
Влияние неорганических примесей, таких как ионы брома, меди, церия, азотной кислоты также влияет на РХВ. Для устранения этого влияния рекомендуют соль Мора или сернокислого железа использовать с квалификацией «х.ч.» или «ч.д.а.» и перед приготовлением дозиметрического раствора перекристаллизовывать из трижды перегнанной подкисленной дистиллированной воды, а серную кислоту перегонять под вакуумом. Саму воду рекомендуют очищать тройной перегонкой.
Методы определения РХВ
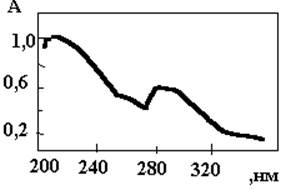 Трехвалентное железо можно
определять методом потенциометрического титрования облученного раствора
растворами перманганата калия или бихромата калия, колориметрически или
спектрометрически с орто-фенантралиновым комплексом, но самый распространенный
метод – прямое спектрофотометрическое определение в ультрафиолетовой области
спектра при 304 нм (ε = 2205 ±3 л/ моль. см).
Трехвалентное железо можно
определять методом потенциометрического титрования облученного раствора
растворами перманганата калия или бихромата калия, колориметрически или
спектрометрически с орто-фенантралиновым комплексом, но самый распространенный
метод – прямое спектрофотометрическое определение в ультрафиолетовой области
спектра при 304 нм (ε = 2205 ±3 л/ моль. см).
Погрешность такого определения составляет ±2%.
Чувствительность метода может быть увеличена почти в 2 раза, если регистрацию проводить при 224нм, где ε = 4480 л/моль . см).
Границы применимости дозиметра Фрикке
Нижний предел измеряемых доз – 30 Гр определяется возможностью измерить оптическую плотность А = 0,1 ( примерно 90% пропускания по отношению к необлученному раствору).
Верхний предел, как мы уже обсуждали, определяется процессом расходования растворенного кислорода – 0,4 кГр. Поэтому по международной классификации этот дозиметр называется ДФС – 0,04 / 0.4, т.е. от 0,04 до 0,4 кГр.
Расчет дозы очевиден: Д = 2,797.102 ((А – А0) (Гр). Подробнее вы ознакомитесь при выполнении лабораторного практикума по РХ.
Модифицированные дозиметры Фрике
Для расширения диапазонов измеряемых доз, что порой бывает весьма важным, приходится использовать модифицированные дозиметры Фрике. Так, например, когда гамма-облучательная установка МРХ-гамма-20 работает сразу после перезагрузки кобальтовых источников, отдозиметрировать центральный канал обычным дозиметром Фрикке практически невозможно, поскольку погрешности, связанные с операцией «спуск – подъем» резко возрастают.
Ферросульфатно - медный дозиметр
Расширение диапазона измеряемых доз по сравнению с дозиметром Фрикке достигается уменьшением РХВ Fe3+ за счет введения в систему ионов меди Cu+2.
Они вступают в конкуренцию с ионами железа за сольватированные электроны и атомы водорода предотвращают реакции 1 и 2.
е-aq+ Н+→ Н* (1) О2 + Н*→ НО2* (2)
Cu+2 + е-aq → Cu+
Cu+2 + Н*→ Cu+ + Н+
Cu+2 + НО2*→ Cu+ + Н+ + О2
___________________________
Cu+ + Fe3+ → Fe 2+ + Cu+2
В результате G(Fe3) = G (ОН*) +2G(Н2О2 ) - G (Н* ) -G (е-aq )
G(Fe3) = 0,8 = 2,85 + 2 . 0,75 - 2,85 - 0,6, хотя в реальных условиях РХВ = 0,66 ионов/100 эВ
Т.о. измеряемый диапазон доз - от 0,4 кГр до 100 кГр
Стандартная рецептура – 6.10-3М FeSO4 , 6.10-2CuSO4 и 5.10-2 H2SO4. Правда, по неко торым данным G(Fe3) в этой системе = 0,56 ионов / 100 эВ.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.