e-- + CCl4 → Cl-- + CCl*3
CCl*3 + CH3OH → CCl3H + *CH2OH
*CH2OH + CCl4→ HCl + CH2O
При 77К реакция происходит весьма медленно. С ростом температуры скорость возрастает. В области расстекловывания матрицы (в метаноле около 100К) механизм реакции меняется, поскольку из-за «размораживания» подвижности СР резко увеличивается их подвижность, а значит, и вероятность обрыва цепи. Логично предположить, что последняя реакция осуществляется не путем диффузии гидроксиалкильного СР, а представляет собой процесс дальнего тунельного переноса электрона, поскольку основной отличительной особенностью подобных «подбарьерных» процессов является отклонение температурной зависимости их констант скорости от уравнения Аррениуса. Почему их называют «подбарьерными»? Дело в том, что это квантово-механическое явление, состоящее в преодолении электроном потенциального барьера, отделяющего исходное состояние от конечного, когда полная энергия электрона меньше высоты барьера.
Другие, менее экзотические, но не менее важные цепные процессы фиксируются при изучении радиолиза ряда органических кристаллов.
Так, например, еще в 1953 году было обнаружено, что при облучении твердого хлористого холина при комнатной температуре выход его разложения достигает 55000 мол-л/100 эВ.
[(CH)3N+CH2CH2OH]Cl-- → (CH)3N+HCl-- + СН3СНО
Интересно, что если облучение проводить при температуре, превышающей температуру фазового перехода в кристалле ( +78С), то цепного разложения не наблюдается.
Подобный процесс происходит и в бромистом холине (РХВ-1000 мол-л/100 эВ) и также прекращается при достижении температуры фазового перехода (+90С).
Эти наблюдения заставляют задуматься о роли кристаллической структуры облучаемого объекта, о том как развивается цепной процесс в кристаллической решетке.
В работах, проводимых на нашей кафедре, этим вопросам уделялось большое значение. Мы занимались изучением цепных радиационно-инициированных реакций в кристаллических углеводах.
Дело в том, что еще до наших исследований было обнаружено, что при облучении моногидрата глюкозы образуется глюконовая кислота (РХВ-13 мол-л/100 эВ), в лактозе РХВ 2-дезоксилактобионовой кислоты около 50мол-л/100 эВ, в 2-дезокси-Д-рибозе молекулярный продукт образуется с выходом около 700 мол-л/100 эВ. Про фруктозу было известно, что в ней тоже происходит цепное образование разрушение кристаллов с выходом 40 молекул на 100 эВ . Для выяснения механизма образования 6-дезокси-D-трео-гексодиулозы во фруктозы авторы работы исследовали зависимость РХВ этого продукта от температуры облучения образца (рис. 1.1).
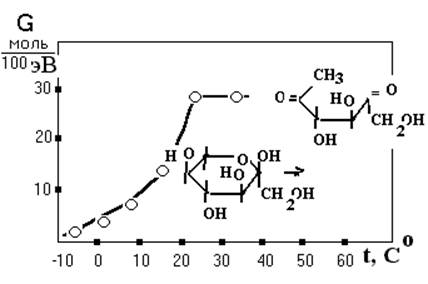
Рисунок 1.1
РХВ (6-дезокси-D-трео-2.5-гексодиулозы) как функция температуры облучения. D = 7.5 × 10 кГр. Мощность дозы: 0.71 Гр × сˉ¹ /32/.
Однако, не имея данных о реакциях СР в этом температурном интервале, они не смогли предложить убедительной схемы цепного процесса в изученном УВ и объяснить полученную зависимость.
Исследуя пострадиационные твердофазные РИП методом ЭПР мы идентифицировали более 20 видов СР в объектах исследования в температурном диапазоне 77 – 360 К и изучили кинетики их взаимопревращений при комнатной температуре (рис. 1 – 4).
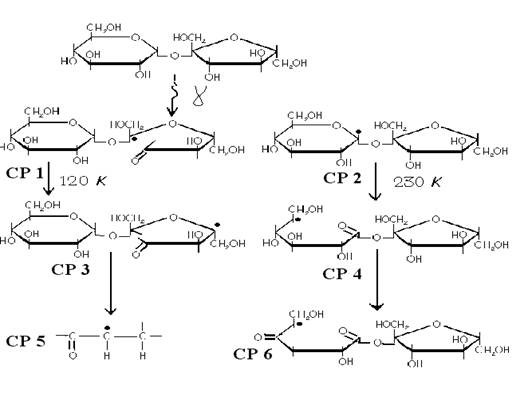
Дополнив эти данные результатами, полученными оптическими метода-ми (табл.2, мы установили температурные условия при которых в кристаллах всех 5 УВ (включая арабинозу и ксилозу) начинается образование МП. В большинстве случаев удалось определить и кинетические закономерности этих процессов.
В облученных кристаллах сахарозы и ксилозы образование карбонилсодержащих соединений (КСС) подчиняется формальным закономерностям реакций первого порядка. С = Со exp (kt) (13)
Энергии активации – около 80 кДж/моль-1 и примерно 50 кДж/моль-1, соответственно.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.