1). Физическое тепло твердой шихты.
Твердая шихта поступает в отражательную печь из обжиговой печи нагретой. Принимаем температуру нагретой шихты при загрузке в отражательную печь 4000. Количество тепла, вносимое твердой шихтой
![]() ккал
ккал
2). Физическое тепло жидкого конвертерного шлака.
Температуру жидкого конвертерного шлака при заливке его в печь принимаем равной 11500. Теплосодержание конвертерного шлака при этой температуре примерно 325 ккал/кг. Количество тепла, вносимое конвертерным шлаком:
![]() ккал.
ккал.
3). Физическое тепло штейна.
Температура плавления отвального шлака 11200.Учитывая перегрев, тепмературу отвального шлака принимаем 12000. Температура штейна обычно на 50-700 ниже температуры шлака. Принимаем ее 11500. При этой температуре теплосодержание 30%-ного медного штейна составляет 230 ккал/кг. Количество тепла, уносимое штейном:
![]() ккал.
ккал.
4). Физическое тепло отвального шлака.
Для шлака,
содержащего по основным шлакообразующим 45% FeO; 40% SiO2; 15% ![]() Al2O3,MgO,CaO, по диаграмме находим
теплосодержание ~ 270 ккал/кг. Учитывая присутствие в шлаке Fe3O4 , а также Al2O3 и MgO, замещающих CaO и
ухудшающих свойства шлака принимаем теплосодержание 300 ккал/кг. Количество
тепла, уносимое отвальным шлаком:
Al2O3,MgO,CaO, по диаграмме находим
теплосодержание ~ 270 ккал/кг. Учитывая присутствие в шлаке Fe3O4 , а также Al2O3 и MgO, замещающих CaO и
ухудшающих свойства шлака принимаем теплосодержание 300 ккал/кг. Количество
тепла, уносимое отвальным шлаком:
![]() ккал.
ккал.
5). Физическое тепло пыли.
Температура отвального шлака равна ~ 12000. Исходя из этого температуру отходящих газов в хвосте печи принимаем 13000. Температура пыли, покидающей печь, равна температуре отходящих газов. Количество тепла, уносимое пылью:
![]() ккал.
ккал.
6). Тепло отходящих газов.
Объем отходящего SO2 равен 0,966 нм3. Температура газа 13000. При этой температуре теплосодержание SO2 составляет 715,3 ккал/нм3. Тепло, уносимое SO2:
![]() ккал
ккал
7). Тепло экзотермических и эндотермических реакций.
Тепловые эффекты экзотермических и эндотермических реакций рассчитываем по закону Гесса на основании значений теплот образования отдельных компонентов.
а). Реакция 10 Fe2O3+FeS=7 Fe3O4+SO2.
Количество окисляющегося по этой реакции FeS-0,313 кг. Теплоты образования компонентов реакции, ккал/моль: FeS-22720; Fe2O3-196500; Fe3O4-267000; SO2-70960.
Тепловой эффект реакции
Q=(1869000+70960)-(22700+1965000)=-23260 ккал.
По реакции
образуется тепла ![]() -83 ккал.
-83 ккал.
б).Реакция 3Fe2O3+FeS=7FeO+SO2.
Количество окисляющегося по этой реакции FeS 3,48 кг. Теплота образования FeO-63700 ккал/моль:
Q=![]() ккал.
ккал.
По реакции
расходуется тепла 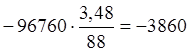 ккал.
ккал.
в).Реакция 2 FeO+SiO2=2FeO SiO2.
В конвертерном шлаке содержится 14,37 кг FeO, в отвальном шлаке 42,482 кг FeO. Количество FeO, реагирующее с SiO2 в отражательной печи: 42,482-14,37=28,112 кг.
Теплоты образования компонентов реакции, ккал/моль: SiO2-205400; 2FeO SiO2-343700;
Q=![]() ккал.
ккал.
По реакции
выделится тепла 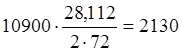 ккал.
ккал.
г).Реакция 2 ZnO+SiO2=2ZnO SiO2.
В отвальном шлаке содержится 1,737 кг ZnO, в конвертерном шлаке 0,95 кг ZnO. Количество ZnO, реагирующее с SiO2 в отражательной печи: 1,737-0,95=0,787 кг.
Теплоты образования компонентов реакции, ккал/моль: ZnO-83170; 2ZnO SiO2-349400;
Q=![]() ккал.
ккал.
По реакции
расходуется тепла 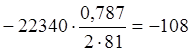 ккал.
ккал.
д).Реакция CaO+SiO2=CaO SiO2.
Учитываем только CaO, поступающий в печь с известняком. В известняке содержится 2,446 кг CaO.
Теплоты образования компонентов реакции, ккал/моль: CaO-151900; CaO SiO2-377000;
Q=![]() ккал.
ккал.
По реакции
выделится тепла 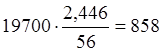 ккал.
ккал.
Общее количество тепла, выделившееся в результате экзотермических реакций:
2130+858![]() ккал.
ккал.
Общее количество тепла, поглотившееся в результате эндотермических реакций:
83+3860+108![]() ккал.
ккал.
Составляем уравнение теплового баланса процесса плавления шихты.
Приход тепла.
1. Тепло извне, идущее на покрытие теплопотребления шихты, qплав, ккал/т.
Количество твердой шихты 124,309 кг, или 0,124309 т.
Теплопотребление твердой шихты 0,124309 qплав.
2. Физическое тепло твердой шихты 9750 ккал.
3. Физическое тепло жидкого конвертерного шлака 13000 ккал.
4. Тепло экзотермических реакций 2990 ккал.
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.