4.1.Тепловой эффект реакций кислого конвертирования.
DfH°Т=DН°298+а(Т-298)+в/2(Т2-2982)
Fe3Si + 2FeO → SiO2 +5Feмет
DfH°1550(Fe3Si)=-177,40×103+74,81(1550-298)+5,52×103/2(15502-2982)=
-177400+74,81×1252+5,52×1156,8=-177400+93662,12+6385,81=-77,352 кДж/моль
DfH°1550(FeO)=-264,85×103 +50,80(1550-298)+8,61×103 /2(15502-2982)=
=-264850+50,80×1252+8,61×1156,85=-264850+63601,6+9960,48=-191,287 кДж/ моль
DfH°1550(SiO2)=-910,94×103 +46,99(1550-298)+34,31×103 /2(15502-2982)=
=-910940+46,99×1252+34,31×1156,85=-910940+58831,48+39691,52=-812,42 кДж/ моль
DfH°1550(Fe)=17,24(1550-298)+24,77×103 /2(15502-2982)=
=17,24×1252+24,771×1156,85=21584,48+28655,17=50,24 кДж/ моль
åDfH°1550=(-812,42+5×50,24)-(2×(-191,287)+(-77,352))=-101,294 кДж/ моль
Такое количество тепла выделится при образовании 5 молей железа.В результате реакции образовалось 47,7 кг железа.
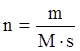
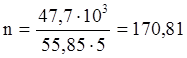
Q=170,81×(-101,294)=-17302,02 кДж
2FeO + SiO2 →Fe2SiO4
DfH°1550(FeO)=-264,85×103 +50,80(1550-298)+8,61×103 /2(15502-2982)=
=-264850+50,80×1252+8,61×1156,85=-264850+63601,6+9960,48=-191,287 кДж/ моль
DfH°1550(SiO2)=-910,94×103 +46,99(1550-298)+34,31×103 /2(15502-2982)=
=-910940+46,99×1252+34,31×1156,85=-910940+58831,48+39691,52=-812,42 кДж/ моль
fH°1550(Fe 2 SiO4)=-1117,13×103 +86,27(1550-298)+208,92×103 /2(15502-2982)=
=-117130+86,27×1252+208,92×1156,85=-111730+108010,04+241689,1=-767,43 кДж/ моль
åDfH°1550=-767,43-(-191,287×-812,42)=427,07 кДж/ моль
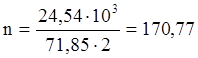
Q=170,77×427,07=72931,8 кДж
2Fe3C +4O2 → 6FeO + 2CO2
DfH°1550(Fe3С)=-738,15×103 +48,66(1550-298)+112,13×103 /2(15502-2982)=
=-738150+48б66×1252+112,13×1156,85=-738150+60922,32+129717,9=-547,51кДж/ моль
DfH°1550(O2)=31,46(1550-298)+3,39×103 /2(15502-2982)=
=31,46×1252+3,39×1156,85=393,88+3921,72=4,31кДж/ моль
DfH°1550(FeO)=-191,287 кДж/ моль
DfH°1550(CO2)=-393,51×103 +44,14(1550-298)+9,04×103 /2(15502-2982)=
=-393510+44,14×1252+112,13×1156,85=-393510+10458+55263,28=-327,788 кДж/ моль
DfH°1550=(-191,287×2+(-327,778×2))-(-547,51×2)+4×4,31)=1134,73 кДж/ моль
Такое количество тепла потребуется для вступления 2 молей Fe3С. m=10,92 кг
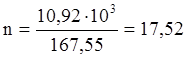
Q=1134,78×30,42=34518,5 кДж
2Cr+ 3FeO → Cr2O3 + 3Feмет
DfH°1550(Cr)= 24,43(1550-298)+9,87×103 /2(15502-2982)=
=24,43×1252+9,87×1156,85=42,0 кДж/ моль
DfH°1550(FeO)=-191,287 кДж/ моль
DfH°1550(Cr 2O3)=-1140,56×103 +119,34(1550-298)+9,2×103 /2(15502-2982)=
=-1140560+119,34×1252+9,2×1156,85=-1140560+149413,7+10643,02=-980,5 кДж/ моль
DfH°1550(Fe)=17,24(1550-298)+24,77×103 /2(15502-2982)=
=17,24×1252+24,771×1156,85=21584,48+28655,17=50,24 кДж/ моль
DfH°1550=(50,24×3+(-980,5))-(42×2)+3×(-191,287)=-339,94 кДж/ моль
В результате реакции образовалось 2,945 кг железа
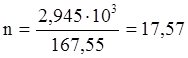 моль
моль
Q=-339,94×17,57= -5972,74кДж
Сr2O3 + FeO→ FeCr2O3
DfH°1550(Cr 2O3)=-1140,56×103 +119,34(1550-298)+9,2×103 /2(15502-2982)=
=-1140560+119,34×1252+9,2×1156,85=-1140560+149413,7+10643,02=-980,5 кДж/ моль
DfH°1550(FeO)=-191,287 кДж/ моль
fH°1550(Fe 2 SiO4)=-1117,13×103 +86,27(1550-298)+208,92×103 /2(15502-2982)=
=-117130+86,27×1252+208,92×1156,85=-111730+108010,04+241689,1=-767,43 кДж/ моль
DfH°1550=(-767,43-(-980,5)+(-767,43)=980,5 кДж/ моль
Такое количество тепла потребуется для вступления в реакцию 1 моля Cr 2O3. m=2,67кг
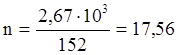 моль
моль
Q=980б5×17,56=17217,58кДж
2Fe + O2 →2FeO
DfH°1550(Fe)=17,24(1550-298)+24,77×103 /2(15502-2982)=
=17,24×1252+24,771×1156,85=21584,48+28655,17=50,24 кДж/ моль
DfH°1550(O2)=31,46+(1550-298)+3,39×103 /2(15502-2982)=
=31,46×1252+3,39×1156,85=393,88+3921,72=4,31кДж/ моль
DfH°1550(FeO)=-191,287 кДж/ моль
DfH°1550=(-191,287×2)-50,24×2+4,31=-487,36 кДж/ моль
Такое количество тепла выделяется при образовании 2 молей FeO, m=45б12 кг
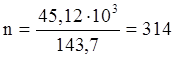 моль
моль
Q=-487,36×314=-153031,04 кДж.
2Ni2P + 5FeO +3CaO → (Ca3PO4)2+5Feмет+4Niмет
DfH°1550(Ni 2P)=-79,50×103 +38,7(1550-298)+26,78×103 /2(15502-2982)=
=-79500+38,7×1252+26,78×1156,85=-79500+48452,4+30980,44=-0,067 кДж/ моль
DfH°1550(FeO)=-191,287 кДж/ моль
fH°1550(СaO)=-635,09×103 +49,62(1550-298)+4,52×103 /2(15502-2982)=
=-635090+49,62 ×1252+4,52×1156,85=-635090+62124,24+5228,96 =-567,73 кДж/ моль
fH°1550(Сa3PO4)2=-4120,82×103 +201,84(1550-298)+166,02×103 /2(15502-2982)=
=-4120820+201,84 ×1252+166,02×1156,85=-4120820+252703,7+192060,24= =-3676,05кДж/ моль
DfH°1550(Fe)=17,24(1550-298)+24,77×103 /2(15502-2982)=
=17,24×1252+24,771×1156,85=21584,48+28655,17=50,24 кДж/ моль
fH°1550(Ni)=16,82(1550-298)+37,82×103 /2(15502-2982)=
=16,82×1252+37,82×1156,85=21058,64+43752,07=64,81 кДж/ моль
DfH°1550=(64,81×4)+50,24×5+(-3676,05)-(3∙(-567,73)+(-191,287∙5+(-0,067∙2))=-505,81 кДж/ моль
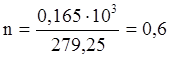 моль
моль
Q=-505.81×0,6=-303,48 кДж.
2Fe3P + 5FeO +3CaO →(Ca3PO4)2 +11Feмет
DfH°1550(FeO)=-191,287 кДж/ моль
fH°1550(СaO)=-635,09×103 +49,62(1550-298)+4,52×103 /2(15502-2982)=
=-635090+49,62 ×1252+4,52×1156,85=-635090+62124,24+5228,96 =-567,73 кДж/ моль
fH°1550(Сa3PO4)2=-4120,82×103 +201,84(1550-298)+166,02×103 /2(15502-2982)=
=-4120820+201,84 ×1252+166,02×1156,85=-4120820+252703,7+192060,24= =-3676,05кДж/ моль
DfH°1550(Fe)=17,24(1550-298)+24,77×103 /2(15502-2982)=
=17,24×1252+24,771×1156,85=21584,48+28655,17=50,24 кДж/ моль
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.