При охлаждении жидкость, прежде чем начать кристаллизоваться, должна переохладиться ниже равновесной температуры кристаллизации, поскольку существует энергетический барьер для образования зародыша кристаллической фазы. Степень переохлаждения расплава зависит от нескольких факторов, включающих первоначальную вязкость расплава, скорость ее возрастания по мере снижения температуры, температурную зависимость разности свободных энергий переохлажденного расплава и кристаллической фазы, энергию границы между жидкой фазой и кристаллом, объемную плотность и эффективность центров гетерогенного зародышеобразования и, наконец, используемую скорость охлаждения. Расплавы переходных металлов (Fe, Ni, Со), из которых путем хорошего раскисления удалены частицы, способствующие гетерогенному зарождению кристаллов, могут переохлаждаться в слитке более чем на 200 К даже в условиях медленного охлаждения. Аналогично, если металлический расплав разделить на отдельные капли очень малого размера, находящиеся в жидкой фазе, то по крайней мере некоторые из капель не смогут кристаллизоваться по гетерогенному механизму, и зарождение будет происходить гомогенно при относительных переохлаждениях, равных »0,2-0,3Тm, где Tm – равновесная температура стеклования. Однако скорость роста кристаллов в металлических расплавах очень высока, и если скорость отвода тепла в окружающую среду не очень большая, то происходит быстрое заполнение матрицы кристаллической фазой.
Однако, если расплав охладить быстро, обеспечив эффективный теплоотвод, влияние источников гетерогенного зарождения кристаллов значительно затруднится по чисто кинетическим причинам, а в случае дальнейшего увеличения скорости охлаждения переохлаждение еще больше возрастет и склонность к кристаллизации снизится. Таким образом, температурный интервал, в котором может протекать процесс кристаллизации становится существенно уже, что приводит к изменению формирующейся в процессе охлаждения структуры. Сначала измельчается микрокристаллическая структура, а затем в зависимости от состава сплава – расширяется растворимость в твердом растворе и формируются метастабильные кристаллические фазы. Если скорость охлаждения очень высока, вследствие недостатка времени кристаллизация полностью подавляется, причем замедляется не только процесс роста кристаллов, но и их зарождение. В этом случае сдвиговая вязкость h расплава при охлаждении непрерывно растет (рисунок 18).
Хотя движущие силу кристаллизации постоянно увеличиваются, они тем не менее компенсируются быстро снижающейся подвижностью атомов, которая доминирует при очень больших переохлаждениях. В окончательном виде атомная конфигурация, присущая жидкости, удаляется от равновесия и при температуре стеклования Tg оказывается гомогенно замороженной. На практике не бывает так, чтобы данному сплаву соответствовала только одна аморфная структура, поскольку и температура, и структура, при которой происходит отклонение от состояния конфигурационного равновесия, зависит от скорости охлаждения. Следовательно, Tg и аморфная структура зависит от скорости охлаждения. Изменение последней приводит к различному характеру поведения сплава на стадии структурной релаксации при последующем нагреве. При значении температуры, равном Tg, температурная зависимость объема и энтальпии изменяется скачкообразно. Заметное снижение теплоемкости Ср свидетельствует о более низкой степени беспорядка в расположении атомов относительно первоначально замороженного состояния (рисунок 19). Разность теплоемкостей переохлажденной жидкости и кристалла DСр растет с падением температуры, но при осуществлении процесса стеклования она становится очень малой величиной. По модели свободного объема стеклования соответствует уничтожению большей части свободного объема.
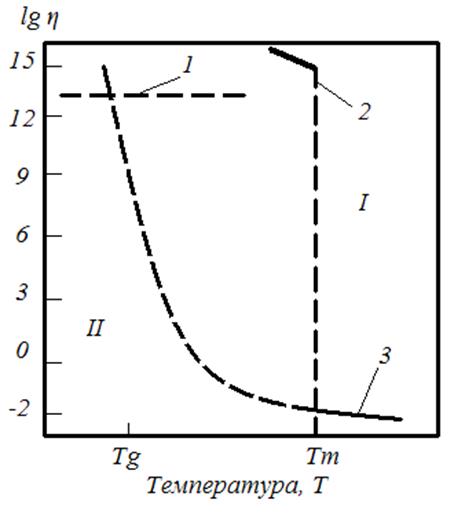
1 – аморфное состояние; 2 – кристалл; 3 – жидкость
Рисунок 18 – Зависимость вязкости η от температуры T в случае кристаллизации (I) и аморфизации (II) металлического расплава
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.