Лекция 14. ТЕПЛОЕМКОСТЬ. МОЛЯРНАЯ ТЕПЛОЕМКОСТЬ. УРАВНЕНИЕ МАЙЕРА.

Теплоемкостью называется количество теплоты, необходимое для изменения температуры системы на 1 К.



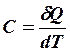 (1);
(1); 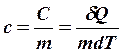 (2) – удельная теплоемкость
(2) – удельная теплоемкость
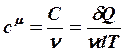 (3)
– молярная теплоемкость
(3)
– молярная теплоемкость
![]()
Теплоемкость зависит от способа передачи теплоты.
Вычислим молярную теплоемкость идеального газа при различных процессах.
1)
 изохорный V=const,
изохорный V=const,
![]() ,
, ![]() ,
, 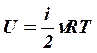 ,
, 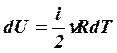 (4),
(4),

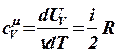 (5) и является функцией состояния системы.
(5) и является функцией состояния системы.
2)
изобарный р = const, ![]() ,
,
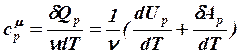 ,
, 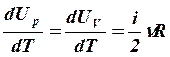 ,
,

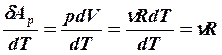 , где
, где ![]()
![]() изобарная молярная теплоемкость:
изобарная молярная теплоемкость: 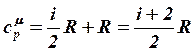 (6) является
функцией состояния идеального газа.
(6) является
функцией состояния идеального газа. ![]() (7) - уравнение Майера.
(7) - уравнение Майера.

Молярные теплоемкости в явном виде не зависят от температуры, но число степеней свободы зависит от температуры.
ПОЛИТРОПИЧЕСКИЙ ПРОЦЕСС. УРАВНЕНИЕ ПУАССОНА. РАБОТА ПРИ ИЗОПРОЦЕССАХ.

Политропическим называется процесс, в котором теплоемкость является постоянной величиной.
![]()
![]() (8). Запишем (8) в виде:
(8). Запишем (8) в виде: ![]() (9)
(9)
![]() Выразим dT из ур. Клапейрона-Менделеева
Выразим dT из ур. Клапейрона-Менделеева
![]() (10),
подставим в (9) и рассмотрим выражение для
(10),
подставим в (9) и рассмотрим выражение для ![]() :
:![]() (11).
(11).

![]() Используем
Используем ![]() , обозначим
, обозначим 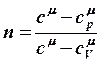 (12) и получим
(12) и получим

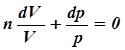 (13)- уравнение политропического процесса
(политропы) в
(13)- уравнение политропического процесса
(политропы) в
![]() дифференциальной
форме.
дифференциальной
форме.
После интегрирования ![]() (14)- уравнение политропы в интегральной форме,
n – показатель политропы.
(14)- уравнение политропы в интегральной форме,
n – показатель политропы.

ЦИКЛЫ. РАБОТА ЦИКЛА. КПД ЦИКЛА. ЦИКЛ КАРНО.

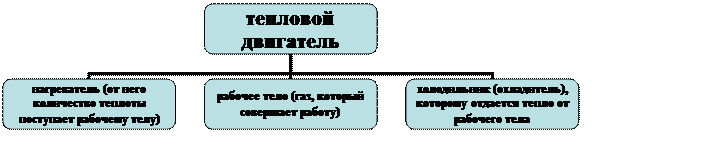
Тепловым двигателем называется любое устройство, совершающее механическую работу за счет поступающего в это устройство количества теплоты.
К тепловым двигателям относятся: двигатели внутреннего сгорания, дизельные двигатели, реактивные двигатели, любое оружие.

Циклом (круговым процессом) называется процесс, при котором система возвращается в исходное состояние (рис. 1).
 а)
а) ![]() - температура
нагревателя,
- температура
нагревателя,
![]() - температура холодильника
- температура холодильника
Участок 1а2: ![]() , А1 >0, по
I началу Q1>0.
, А1 >0, по
I началу Q1>0.
Участок 2б1: ![]() , А2 < 0, Q2<0.
, А2 < 0, Q2<0.
За цикл ![]() ,
, ![]() ,
, ![]()

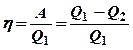 (1) КПД цикла
(1) КПД цикла
теплового двигателя

Коэффициентом полезного действия теплового двигателя называется отношение полной работы за цикл к полученному от нагревателя за цикл количеству теплоты.
Цикл 1а2б – обратим. Тогда 1б2а1 – в обратном направлении Q2>0, Q1<0, А<0 – цикл холодильной машины – перенос теплоты от холодильника к нагревателю за счет А < 0.
б) Цикл Карно (1 моль идеального газа).

Циклом Карно называется циклический процесс, состоящий из двух изотерм и двух адиабат (рис. 2).

1-2 изотермический ![]() ,
, 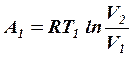 (2)
(2)
2-3 адиабатический ![]() ,
, ![]() ,
, ![]()
3-4 изотермический ![]() ,
, 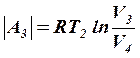 (3)
(3)
4-1 адиабатический ![]() ,
, ![]() ,
,![]() .
.
 Частные случаи
политропического процесса:
Частные случаи
политропического процесса:
1)
![]() изотермический: Т=const,
dТ=0 ,
изотермический: Т=const,
dТ=0 , 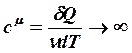 , n=1,
, n=1, ![]() (1)- уравнение
(1)- уравнение
изотермы,
![]()
 работа газа
работа газа 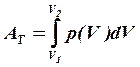
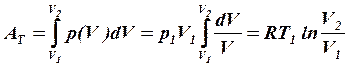 (2)
(работа одного моля газа);
(2)
(работа одного моля газа);
2)
![]()
 изохорический:
V=const,
изохорический:
V=const, ![]() ,
, ![]() ,
, 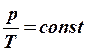 (3)-
уравнение изохоры,
(3)-
уравнение изохоры,
работа газа А=0 (4);
3)
![]()
![]() изобарический:
р=const,
изобарический:
р=const, ![]() , n=0,
, n=0, 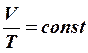 (5)
- уравнение изобары, работа газа
(5)
- уравнение изобары, работа газа ![]() (6) ;
(6) ;
4)
![]() адиабатический:
адиабатический:![]() ,
, ![]() ,
, 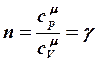
![]() (7)- уравнение адиабаты или уравнение Пуассона,
(7)- уравнение адиабаты или уравнение Пуассона,
 |
 где
где 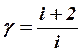 (8)-
показатель адиабаты.
(8)-
показатель адиабаты.
Работа при адиабатическом процессе:
 |
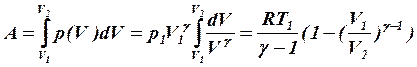 (9)
(9)

Полная работа газа за цикл А=А1+А2+А3+А4=
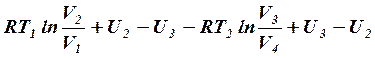 .
.
 КПД цикла Карно:
КПД цикла Карно: 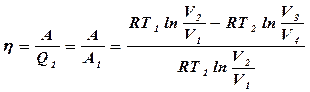 (4)
(4)
Чтобы получить соотношение между объемами преобразуем уравнение Пуассона:
![]()
![]()
![]() (5) , заменив в нем pV,
учитывая
(5) , заменив в нем pV,
учитывая ![]() . Тогда (5) имеет вид
. Тогда (5) имеет вид
![]()
![]() (6) . Запишем (6) для процессов 2-3 и 4-1:
(6) . Запишем (6) для процессов 2-3 и 4-1:
![]()
![]() ,
,
![]()
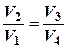 (7)
(7)

![]()
Отсюда КПД обратимого цикла Карно: 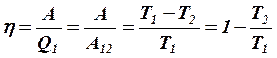 (8).
(8).
![]()
Устройство, работающее по обратному циклу, называется холодильной машиной.
Для холодильной машины необходим внешний источник энергии (домашний холодильник получает энергию из электрической сети).
в) Теоремы Карно:

I. КПД цикла Карно не зависит от рода рабочего вещества и конструкции теплового двигателя, а определяется лишь температурами нагревателя Т1 и холодильника Т2.

II. КПД любого
другого цикла, проводимого в одинаковых предельных температурных условиях с
циклом Карно не может быть больше КПД цикла Карно: ![]() ,
, 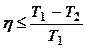 (9).
(9).
ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ. ЭНТРОПИЯ. ЗАКОН ВОЗРАСТАНИЯ ЭНТРОПИИ.
Вторым началом термодинамики называются постулаты (утверждения), сформулированные различными учеными на основании экспериментальных данных и теории идеальных двигателей.

 Постулат Клаузиуса: тепловая энергия
самопроизвольно не может передаваться от более холодного тела к более
нагретому телу.
Постулат Клаузиуса: тепловая энергия
самопроизвольно не может передаваться от более холодного тела к более
нагретому телу.При изучении тепловых процессов, происходящих при переходе системы из одного состояния в другое удобно использовать физические величины, которые являются функциями состояния (являются полными дифференциалами), т.е. не зависят от процесса.
 |
|
Для идеального газа уже обсуждались функции состояния: внутренняя
энергия U(V,T), изохорная молярная теплоемкость ![]() , изобарная молярная теплоемкость
, изобарная молярная теплоемкость ![]() и т.д.
и т.д.

Энтропией называется функция состояния идеального газа, дифференциал
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.