Лабораторная работа №15
ИЗУЧЕНИЕ ИЗОХОРИЧЕСКОГО ПРОЦЕССА
Цель работы: изучить зависимость давления воздуха от температуры при постоянном объёме, найти плотность воздуха.
Приборы и принадлежности: баллон, манометр, термометр, нагреватель.
1. ОБЩИЕ СВЕДЕНИЯ
Состояние системы в термодинамике характеризуется набором термодинамических параметров, то есть физических величин, измеряемых на опыте. Например, состояние газа удобно характеризовать массой m, объёмом V, давлением Р и температурой Т. Некоторые параметры имеют как термодинамический, так и механический смысл (m, Р), другие - только термодинамический (Т).
Давлением называется физическая величина, численно равная силе F, действующей на единичную площадку по нормали к ней
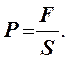
Температура характеризует степень нагретости тела. В термодинамике используется абсолютная шкала температур (шкала Кельвина), связанная со шкалой Цельсия соотношением:
T = t + 273, (1) где t - температура газа по шкале Цельсия, °С.
Температура t измеряется термометром.
Функциональная зависимость, связывающая термодинамические параметры, называется уравнением состояния.
Простейшей термодинамической системой является идеальный газ.
Идеальным называется газ, молекулы которого имеют исчезающе малый объем и не взаимодействуют друг с другом. Уравнение состояния называется уравнением Клапейрона - Менделеева
PV = ![]() RT,
(2)
RT,
(2)
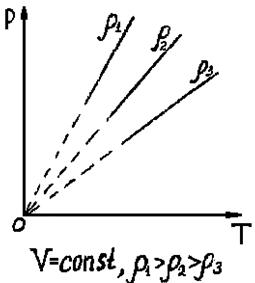 где
R = 8,31 Дж/(моль·К) - универсальная газовая постоянная; μ - молярная
масса, кг/моль.
где
R = 8,31 Дж/(моль·К) - универсальная газовая постоянная; μ - молярная
масса, кг/моль.
Воздух является смесью газов, для него вычисляется значение μ = 29 · 10-3 кг/моль.
Изохорическим называется процесс, при котором объем
системы остается постоянным. Из формулы (2) при V = const получаем:
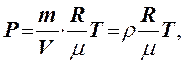 (3)
(3)
![]() то есть давление прямо пропорционально температуре.
Здесь ρ - плотность газа. Зависимость давления от температуры при различных
значениях плотности изображена на рис. 1.
то есть давление прямо пропорционально температуре.
Здесь ρ - плотность газа. Зависимость давления от температуры при различных
значениях плотности изображена на рис. 1.
Термический коэффициент давления γ определяется по формуле
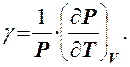 (4)
(4)
Он характеризует относительное изменение давления при.
изменении температуры на 1 К.. Используя (3), нетрудно найти 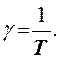
2. ОПИСАНИЕ УСТАНОВКИ
Установка для изучения изохорического процесса изображена на рис. 2. Исследуемый газ (воздух) находится в баллоне Б, помещенном в кастрюлю с водой К. Давление в баллоне измеряется манометром М. Кран Кр позволяет установить атмосферное давление в баллоне. В рабочем положении кран должен быть закрытым. Насосом Н через клапан устанавливается начальное давление. Установка помещается на нагреватель Пл - электрическую плитку. Температура воды и, следовательно, воздуха в баллоне измеряется термометром Т.
![]() При проведении экспериментов следует помнить, что
термометр измеряет температуру по шкале Цельсия, манометр - избыточное
(превышение над атмосферным) давление. При переводе измеренных давлений в СИ
можно пользоваться следующими соотношениями
При проведении экспериментов следует помнить, что
термометр измеряет температуру по шкале Цельсия, манометр - избыточное
(превышение над атмосферным) давление. При переводе измеренных давлений в СИ
можно пользоваться следующими соотношениями
1 ат =1,013 · 105 Па,
1 кгс/см2 = 0,981·105 Па,
1мм рт. ст. = 133Па,
1мм вод. ст. = 9,81 Па.
3. ПОРЯДОК ВЫПОЛНЕНИЯ РАБОТЫ
 1) Налейте в кастрюлю воды, измерьте термометром
начальную температуру t0, по формуле (1) найдите
абсолютную температуру Т0. Измерьте барометром
атмосферное давление P0.
Переведите измеренное значение в СИ.
1) Налейте в кастрюлю воды, измерьте термометром
начальную температуру t0, по формуле (1) найдите
абсолютную температуру Т0. Измерьте барометром
атмосферное давление P0.
Переведите измеренное значение в СИ.
2) Перекройте кран Kр (рис. 2), насосом Н накачайте воздух в баллон Б до давления, указанною преподавателем. Поместите установку на нагреватель.
![]() 3) Изучите зависимость давления от температуры.
3) Изучите зависимость давления от температуры.
а) Через равные интервалы времени измеряйте избыточное давление Р и соответствующую ему температуру t . Сделайте 8 - 10 измерений. Измеренные значения записать в табл. 1.
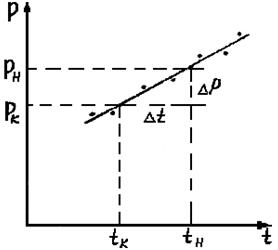
б) По результатам измерений постройте график зависимости избыточного давления от температуры (рис. 3). По графику определите отношение
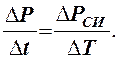
Переведите полученный результат и СИ.
в) Определите по формуле (4) коэффициент γ. Для этого разделите отношение ΔР/ΔT на начальное давление, в качестве которого взять сумму Р0 + ΔР. Сравнить полученное значение с обратной температурой 1/T0.
Таблица 1.
Изучение зависимости давления от температуры г) Определить плотность воздуха по формуле: 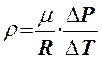 и по формуле (3). Сравните полученные результаты
между собой.
и по формуле (3). Сравните полученные результаты
между собой.
4. КОНТРОЛЬНЫЕ ВОПРОСЫ
1) Что называется термодинамическими параметрами?
2) Какие параметры используются для характеристики состояния газа?
3) Что называется давлением?
4) Какой термодинамический и статистический смысл абсолютной температуры?
5) Что называется уравнением состояния?
6) Какой газ называется идеальным?
7) Как записать уравнение Клапейрона - Менделеева?
8) Какой процесс называется изохорическим? Как выглядят графики этого процесса в различных диаграммах?
9) Что называется термическим коэффициентом давления?
Уважаемый посетитель!
Чтобы распечатать файл, скачайте его (в формате Word).
Ссылка на скачивание - внизу страницы.